Trombosis de eje porto-espleno-mesentérico por síndrome de trombosis con trombocitopenia inducida por la vacuna COVID-19 AstraZeneca ChAdOx1nCov-19: reporte de caso
Porto-espleno-mesenteric thrombosis for thrombosis with thrombocytopenia syndrome (TTS) following AstraZeneca ChAdOx1 nCoV-19 COVID-19 vaccination: case report
Lusich B; Portillo Salazar IC
brunilusich@hotmail.com
Palabras claves: vacuna ChAdOx1 nCov-19 (AstraZeneca),
trombosis,
trombocitopenia.
Keywords: vaccine ChAdOx1 nCov-19 (AstraZeneca),
thrombosis,
thrombocytopenia.
Resumen
La trombosis venosa y la trombocitopenia después de la vacunación con la vacuna COVID-19 transmitida por adenovirus ChAdOx1 nCov-19 (AstraZeneca) se han relacionado con anticuerpos séricos contra el factor plaquetario 4 (PF4)-complejos polianión. Reportamos aquí un caso de síndrome de trombosis con trombocitopenia inducida por esta vacuna. Se presentan los hallazgos de laboratorio e imagen, las decisiones de tratamiento y el resultado de este caso.
Abstract
Venous thrombosis and thrombocytopenia after vaccination with the adenovirus vectored COVID-19 vaccine ChAdOx1 nCov-19 (AstraZeneca) have been linked to serum antibodies against platelet factor 4 (PF4)-polyanion complexes. We here report a thrombosis with thrombocytopenia syndrome (TTS) vaccine induced case. Laboratory and imaging findings, treatment decisions and outcome of this case are presented.
Introducción
El programa mundial de vacunación contra el SARS-CoV-2 se ha visto obstaculizado por la aparición inesperada, e inicialmente inexplicable, de trombosis asociada a la vacuna. El síndrome de trombosis con trombocitopenia (STT) es una complicación de las vacunas vectorizadas por adenovirus, incluida la vacuna COVID-19 AstraZeneca ChAdOx1 nCoV-19 que comienza entre 4 y 42 días después de la vacunación. El síndrome es similar al inducido por la heparina y no parece ser inducido por la vacuna, sino que está relacionado a la vacunación con vectores de adenovirus. Se asocia con trombosis, especialmente accidentes cerebrovasculares, del territorio venoso en sitios inusuales como trombosis del seno venoso cerebral y trombosis en venas esplácnicas, así como trombosis del lecho arterial. Estos efectos secundarios trombóticos infrecuentes recuerdan a la infección natural por SARS-CoV-2. Sin embargo, la infección natural por SARS-CoV-2 está mediada por un virus de ARN monocatenario, mientras que la inmunotrombosis asociada a la vacuna está vinculada a las vacunas vectorizadas por adenovirus de ADN.
Los vectores de adenovirus pueden unirse a las plaquetas. Se han asociado con trombocitopenia y pueden desencadenar una coagulación intravascular diseminada, por lo que existe un mecanismo plausible de causalidad. Un modelo para comprender los mecanismos de la infección natural por SARS-CoV-2 y la inmunotrombosis asociada a las vacunas de proteína espiga de ADN es vital y éste es especialmente el caso debido a las interacciones reportadas entre la proteína espiga y el sistema vascular. La inmunotrombosis natural relacionada con la infección por SARS-CoV-2 y los mecanismos inmunotrombóticos posteriores a la vacunación con ADN comparten fuertes similitudes con la condición autoinmune conocida como trombocitopenia inducida por heparina (TIH), que se debe a la formación de anticuerpos contra el complejo heparina factor plaquetario 4 (anti-PF4/HEP), que secundariamente activa las plaquetas y la coagulación y finalmente produce un aumento en la formación de trombina.
La trombosis venosa / hemorragia del territorio venoso en el COVID-19 grave puede estar relacionada con los efectos trombóticos del ARN viral circulatorio y una miríada de factores de hipercoagulabilidad relacionados con la activación inmune sistémica, incluida la activación de plaquetas y células inmunitarias. Para el STT, la rareza extrema probablemente se refiere a mecanismos bien establecidos de tolerancia inmunológica a las proteínas propias, siendo la tolerancia comparativamente difícil de romper. Otros factores incluyen el pequeño tamaño de los inóculos de ADN en las vacunas relevantes con una combinación inadecuada de ADN-PF4 para romper la tolerancia. Las posibilidades de que el ARN o el ADN -en las magnitudes que actualmente suministran los inóculos de vacunas- accedan a la circulación sistémica en cantidades suficientes para desencadenar una inmunopatología similar parecen insignificantes. Las vacunas de ARN utilizan varios receptores de reconocimiento de patrones, incluido el TLR7, mientras que las vacunas de ADN utilizan casi exclusivamente TLR9, relacionado con el desarrollo de la inmunidad humoral y celular contra la proteína espiga. Proponemos que la interacción viral ADN-PF4 puede ser un componente de la inmunidad innata antiviral, similar a este concepto de inmunidad innata intravascular bacteriana. La inyección de adenovirus y la microhemorragia pueden unir el ADN viral y el PF4 en el espacio extracelular, seguido de la captación de células presentadoras de antígeno (APC) y, en raras ocasiones, provocar una enfermedad autoinmune, especialmente en sujetos más jóvenes.
Reporte de caso
Paciente de sexo masculino de 34 años sin antecedentes patológicos conocidos, derivado por dolor abdominal, plaquetopenia severa, con diagnóstico positivo para COVID-19 con inicio de síntomas hace 8 días.
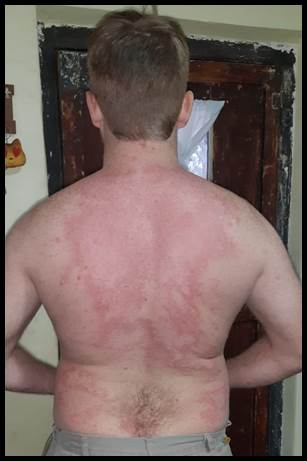
Refiere haberse aplicado la 1ª dosis de la vacuna AstraZeneca hace 18 días y a los 2 días postvacunación intercurre con eritema urticariano y reacción anafiláctica (Figura 1), que requiere administración de corticoide y antihistamínicos en la guardia del hospital de la zona. El paciente evoluciona con dolor abdominal generalizado, fiebre, mialgias a los 10 días postvacunación, por lo que es hisopado para test rápido de COVID-19 con resultado positivo y se indica aislamiento. Por empeoramiento del cuadro abdominal reconsulta en la zona 3 días antes de su derivación a nuestro nosocomio, donde se evidencia plaquetopenia de 22000/mm3, aumento de las transaminasas con TGO: 191 UI/L, TGP: 344 UI/L, FAL: 316 UI/L y bilirrubinas en rango normal. Para encontrar la causa de la plaquetopenia se realiza interconsulta con Hematología, descartándose la producida por fármacos (como la heparina). Se decide administrar prednisona 80 mg/día por sospecha de trombocitopenia inmune.
|
|
||||
|
Figura 1. Lesión cutánea de bordes irregulares con realce periférico, eritematoso, rubicundez y de distribución extensa en la región dorsal, compatible con erupción cutánea. |
||||
|
|
||||
|
|
|
|
||
|
|
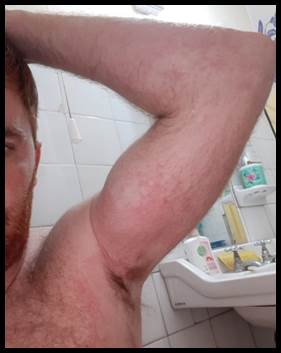
Figura 2. Extensión de la erupción cutánea a nivel del miembro superior izquierdo |
|
||
|
|
|
|
||
|
|
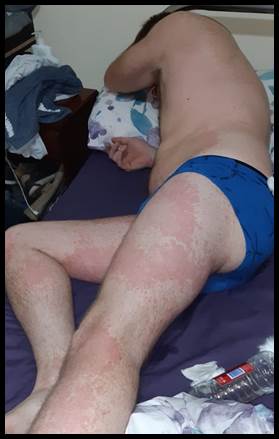
Figura 3. Erupción cutánea en miembros inferiores |
|
||
Por evolución desfavorable se deriva a nuestro nosocomio. Al examen físico se evidencia leve palidez mucocutánea, a nivel abdominal dolor a la palpación profunda de forma generalizada sin defensa ni signos de reacción peritoneal. Los resultados de laboratorio al ingreso son Hto: 32%, Hb; 10.6 g/dL, GB: 11000/ mm3, plaquetas: menos de 10000/mm3, TP: 20 seg (50%), TTP: 32.3, RIN: 1.48, urea: 0.29 g/L (con rango normal: 0.15 - 0.40 g/L) y creatinina: 9.2 mg/L (con rango normal: 7.0 - 13.0 mg/L), TGO: 90 UI/L, TGP: 264 UI/L, FAL: 276 UI/L, bilirrubina total: 1.3 mg%, directa: 0.8 mg% e indirecta: 0.5 mg%. Se realiza ecografía abdominal que evidencia barro biliar y liquido libre en cantidad moderada. Es evaluado por el servicio de Cirugía que decide no tomar conducta quirúrgica por el momento. Se realiza frotis sin presencia de esquistocitos, prueba de Coombs negativa. Se inician pulsos de meltilprednisolona.
Por aumento del dolor y distensión abdominal se realiza tomografía de tórax y abdomen sin contraste, donde se observa derrame pleural escaso y líquido libre perihepático, periesplénico y peripancreático. Además presenta descenso leve en Hto: 30%, Hb: 10 g/dL y plaquetas: menos de 10000/mm3, TP: 17.8 seg (67%), TTP: 32.3 seg, RIN: 1.32, fibrinógeno: 1.20 mg/L, dímero D: 14300 ng/mL (valor normal: < 250 ng/mL), urea 0.58 g/L y creatinina 9.4 mg/L.
Al segundo día de internación se realiza una nueva pantomografía con doble contraste donde se observa incremento del calibre de la vena porta con defecto extenso de repleción en su interior, que se extiende hacia vena esplénica y mesentérica inferior, hallazgos sugestivos de trombosis venosa. Además se visualiza edema periportal, hiporrealce esplénico y engrosamiento del colon derecho con edema submucoso y liquido libre intrabdominal abundante.
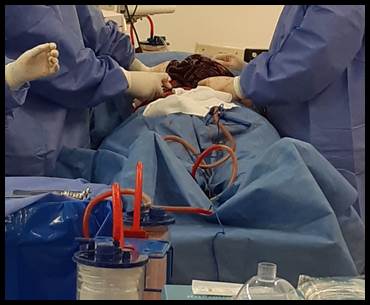
El servicio de Cirugía decide tomar conducta quirúrgica para exploración por videolaparoscopía, donde se identifica hemoperitoneo en los 4 cuadrantes. Se realiza conversión a laparotomía, con lavado y drenaje de aproximadamente 2 litros de hemoperitoneo. Se identifica hematoma de pared intestinal de todo intestino delgado y colon derecho. Se constata vitalidad del órgano con peristaltismo, se coloca drenaje, y es derivado a terapia intensiva intubado con asistencia respiratoria mecánica. Se transfunden 2 unidades de glóbulos rojos y 8 unidades de plaquetas. Diagnóstico postoperatorio de trombosis de eje porto espleno-mesentérico (Figura 4), con sospecha de STT inducida por vacuna AstraZeneca asociado a coagulación intravascular diseminada.
|
|
|
Figura 4. Proceso quirúrgico de urgencia. Se visualiza necrosis del colon con trombosis de la vena mesentérica y extracción de 2 litros de contenido hemático libre en peritoneo. |
En su estadía en el Servicio de Cuidados Intensivos se administra gammaglobulina, plaquetas y crioderivados, además de anticoagulación con heparina de bajo peso molecular. A nivel de laboratorio hay leve mejoría en los parámetros de coagulación y plaquetopenia que se puede observar en la tabla 1, pero en días posteriores el paciente evoluciona con falla renal con requerimiento de diálisis, con posterior falla multiorgánica. Se solicitaron anticuerpos antifactor plaquetario 4, fibrinógeno, producto de degradación del fibrinógeno, que son reportados en diferido. Se reporta la detección de anticuerpos IgG anti factor plaquetario 4 por método ELISA con resultado positivo con más de 12%.
|
Fecha |
25/07 |
26/07 |
26/07 |
27/07 |
27/07 |
28/07 |
29/07 |
|
Hto (%) |
32% |
30% |
21% |
|
17% |
|
|
|
Hb (g/dL) |
10.6 |
10.1 |
7.2 |
|
6 |
|
|
|
GB (/mm3) |
11000 |
16000 |
|
|
19800 |
|
|
|
Neutrófilos (%) |
78% |
78% |
|
|
62% |
|
|
|
Plaquetas (/mm3) |
< 10000 |
< 10000 |
|
|
49000 |
|
|
|
TP (seg)/[TP] (%) |
20 (50%) |
17.8 (67%) |
|
26.1 (38%) |
23.1 (1.73%) |
18.8 (67%) |
|
|
TTP (seg) |
28 |
32.3 |
|
37 |
50 |
33.3 |
|
|
RIN |
1.48 |
1.32 |
|
1.93 |
1.73 |
1.32 |
|
|
Gluc (mg/dL) |
121 |
127 |
408 |
215 |
156 |
137 |
140 |
|
PCR (mg/L) |
57.6 |
|
|
|
|
|
|
|
LDH (UI/L) |
559 |
|
|
1446 |
|
|
|
|
Fibrinógeno (g/L) |
|
1.2 |
|
|
|
1.2 |
|
|
< 250 |
|
14300 |
|
|
4800 |
|
|
|
Urea (g/L) |
0.29 |
0.58 |
|
0.88 |
1.3 |
1.3 |
2.02 |
|
Creatinina (mg/L) |
9.2 |
9.4 |
|
23.4 |
31 |
35.1 |
43.9 |
|
TGO (UI/L) |
90 |
|
|
203 |
|
635 |
1519 |
|
TGP (UI/L) |
264 |
|
|
339 |
|
538 |
1070 |
|
FAL (UI/L) |
276 |
|
|
259 |
|
198 |
233 |
|
Bil. total mg% |
1.3 |
|
|
2 |
|
4 |
5.3 |
|
Bil. directa mg% |
0.8 |
|
|
1.3 |
|
2.3 |
3.2 |
|
Bil. indirecta mg% |
0.5 |
|
|
0.7 |
|
1.7 |
2.1 |
|
Lactato (mmol/L) |
|
2.3 |
13.7 |
4.8 |
4.5 |
3.5 |
3.7 |
|
Tabla 1. Resultados de laboratorio |
|||||||
Discusión
En este caso clínico se pueden plantear las causas de trombocitopenia, entre ellas las producidas por factores inmunológicos abarcados dentro de las microangiopatías trombóticas (MAT) como SHU y PTT, trombocitopenia inmune, reacción a la heparina y los producidos por hiperesplenismo. Luego de descartar estas causas probables se plantean los efectos adversos de la vacuna AstraZeneca como probable causa de dicha patología, debido a que es un fármaco en fase III de experimentación y puede presentar efectos adversos en la sociedad, los cuales escasamente fueron descriptos en la bibliografía. Luego de la inmunización con la vacuna SARS-CoV-2 ChAdOx1-S recombinante de AstraZeneca, se ha observado con muy baja frecuencia una combinación de trombosis con trombocitopenia, en muchos casos acompañada de sangrado. La trombosis venosa esplácnica es un evento muy raro. Aunque la incidencia es muy baja, la tasa de mortalidad es alta, no se ha asociado con anterioridad a la vacunación, pero sí como una complicación de la COVID-19. Fisiopatológicamente explicado como tromboinflamación: daño endotelial que genera activación del complemento y activación plaquetaria mediada por anticuerpos. En la literatura se describe que aproximadamente el 10 % de los individuos vacunados desarrollaran anticuerpos IgG contra los complejos PF4/polianión dentro de los 14 días posteriores a la primera vacunación; sin haber estado expuestos a heparina en los últimos 100 días. Los adultos jóvenes tienen 10 veces más riesgo de padecerla que la población pediátrica, con excepción de la población neonatal de riesgo, que representa 43%. Los eventos presentados con la vacuna de AstraZeneca fueron, en su mayoría, en mujeres menores de 55 años de edad. Sin embargo, esta situación puede reflejar el mayor uso de esta vacuna en dicha población, por lo que no está establecido que exista una relación con una edad o sexo determinados. Algunos casos han tenido desenlace fatal. La tasa de notificación varía entre 1 y 2 casos por 100.000 dosis. En Alemania, por ejemplo, informan de 1/100.000, pero en el Reino Unido es de 1/600.000. La causa subyacente de este síndrome no se ha confirmado, sin embargo, el patrón y mecanismo que ha sido sugerido en estos casos es el de la trombocitopenia inducida por heparina (HIT). Dada la semejanza clínica con la HIT, en la cual el síntoma principal es una trombocitopenia brusca, con una caída del 50% en el recuento plaquetario con respecto a los valores basales, y/o complicaciones trombóticas que aparecen 5 a 14 días tras el comienzo del tratamiento con heparina, era un diagnóstico diferencial importante a descartar. En el caso de nuestro paciente no tuvo nunca exposición a la heparina, por lo que el diagnóstico se inclinó para STT por el antecedente de la vacunación.
Como consecuencia de la trombosis de eje porto-espleno-mesentérico por STT desarrollado por el paciente se presenta la isquemia mesentérica venosa, la cual es poco frecuente (10%) y de diagnóstico tardío en comparación con la isquemia arterial (30%) que presenta manifestaciones agudas. Entre ellas se puede observar que la caída del hematocrito y hemoglobina, junto con las plaquetas se da de forma progresiva y por último se genera la trombosis isquemizante, responsable del drenaje al peritoneo de líquido de sufrimiento, el cual repercute de forma dolorosa en el paciente generando semiología de abdomen agudo quirúrgico por hemoperitoneo. La trombosis extensa de la vena portomesentérica puede requerir intervenciones agresivas y progresivas. La tromboaspiración temprana con fibrinólisis parece segura y eficaz y puede considerarse como una opción para tratar el VITT portomesentérico.
A modo de conclusión, la posibilidad de diagnósticos diferenciales de coagulación intravascular diseminada vs coagulopatía inducida por sepsis (CIS) en el reporte de caso se debe realizar, resaltando que la CIS se provoca por la coagulopatía asociada al COVID 19 con marcadores específicos. Estos últimos son: aumento del dímero D, menor disminución de las plaquetas, menos consumo de factores e inhibidores, suele haber valores de fibrinógeno elevados, si el fibrinógeno desciende al día 10 entonces se puede determinar agravamiento de coagulopatía, rara vez presenta manifestaciones hemorrágicas y los pacientes sufren trombosis.
Por otra parte, se comprende dentro de los diagnósticos diferenciales a la trombocitopenia inducida por la vacuna, la cual presenta criterios específicos. En función del paciente descripto se analiza que éste cuenta con todos los criterios para el diagnóstico para STT: inicio de los síntomas entre 5-30 días posteriores a la vacunación para COVID 19, trombosis en sitios inusuales, trombocitopenia < 150.000/mm3, dímero D elevado > 4000 FEU y anticuerpo antifactor plaquetario 4 por método ELISA. Las contraindicaciones de evitar la transfusión de plaquetas, evitar el uso de heparina, utilizar inmunoglobulinas endovenosas, alternativas de anticoagulación con anticoagulantes orales de acción directa, evaluar plasmaféresis.
Se realizó tratamiento con gammaglobulina y la cirugía desobstructiva para drenaje con transfusión previa de unidades plaquetarias, que, si bien son contraindicadas en los casos de VITT, eran necesarios para la intervención quirúrgica.
Bibliografía
- Aladdin Y, Algahtani H, Shirah B. Vaccine-Induced immune thrombotic thrombocytopenia with disseminated intravascular coagulation and death following the ChAdOx1 nCoV-19 vaccine. J Stroke Cerebrovasc Dis. 2021;30(9):105938.
- Al Rawahi B, BaTaher H, Jaffer Z et al. Vaccine-induced immune thrombotic thrombocytopenia following AstraZeneca (ChAdOx1 nCOV19) vaccine-A case report. Res Pract Thromb Haemost. 2021;5(6):e12578.
- Althaus K, Möller P, Uzun G et al. Antibody-mediated procoagulant platelets in SARS-CoV-2-vaccination associated immune thrombotic thrombocytopenia. Haematologica. 2021;106(8):2170-2179.
- American Society of Hematology. Thrombosis with thrombocytopenia syndrome (also termed vaccine-induced thrombotic thrombocytopenia). 2021. Accessed April 30, 2021. https://www.hematology.org/covid-19/vaccine-induced-immune-thrombotic-thrombocytopenia
- Barral M, Arrive L, El Mouhadi-Barnier S et al. Thromboaspiration and fibrinolysis infusion for portomesenteric thrombosis after AstraZeneca COVID-19 vaccine administration. Intensive Care Med. 2021;47(9):1034-1036.
- Bayas A, Menacher M, Christ M et al. Bilateral superior ophthalmic vein thrombosis, ischaemic stroke, and immune thrombocytopenia after ChAdOx1 nCoV-19 vaccination. Lancet. 2021;397(10285):e11.
- Bersinger S, Lagarde K, Marlu R et al. Using nonheparin anticoagulant to treat a near-fatal case With multiple venous thrombotic lesions during ChAdOx1 nCoV-19 vaccination-related vaccine-induced immune thrombotic thrombocytopenia. Crit Care Med. 2021;49(9):e870-e873.
- Blauenfeldt RA, Kristensen SR, Ernstsen SL et al. Thrombocytopenia with acute ischemic stroke and bleeding in a patient newly vaccinated with an adenoviral vector-based COVID-19 vaccine. J Thromb Haemost. 2021;19(7):1771-1775.
- Bourguignon A, Arnold DM, Warkentin TE et al. Adjunct immune globulin for vaccine-induced thrombotic thrombocytopenia. N Engl J Med. 2021;385(8):720-8.
- Castelli GP, Pognani C, Sozzi, C et al. Cerebral venous sinus thrombosis associated with thrombocytopenia post-vaccination for COVID-19. Crit Care. 2021;25(1):1-2.
- MacIntyre CR, Veness B, Berger D, Hamad N, Bari N. Thrombosis with Thrombocytopenia Syndrome (TTS) following AstraZeneca ChAdOx1 nCoV-19 (AZD1222) COVID-19 vaccination - A risk-benefit analysis for people < 60 years in Australia. Vaccine. 2021 Aug 9;39(34):4784-4787.
- Cuker A. Management of the multiple phases of heparin-induced thrombocytopenia. Thromb Haemost. 2016;116(5):835-842.
- D’agostino V, Caranci F, Negro A et al. A rare case of cerebral venous thrombosis and disseminated intravascular coagulation temporally associated to the COVID-19 vaccine administration. J Pers Med. 2021;11(4):285.
- Dhoot R, Kansal A, Handran C et al. Thrombocytopenia and splanchnic thrombosis after Ad26.COV2.S vaccination successfully treated with transjugular intrahepatic portosystemic shunting and thrombectomy. Am J Hematol. 2021;96(9):1180-1182.
- Gangi A, Mobashwera B, Ganczakowski M et al. Imaging and hematologic findings in thrombosis and thrombocytopenia after ChAdOx1 nCoV-19 (AstraZeneca) vaccination. Radiology. 2021:211546.
- George G, Friedman KD, Curtis BR et al. Successful treatment of thrombotic thrombocytopenia with cerebral sinus venous thrombosis following Ad26.COV2.S vaccination. Am J Hematol. 2021;96(8):E301-E3E3.
- Gras-Champel V, Liabeuf S, Baud M et al. Atypical thrombosis associated with VaxZevria®(AstraZeneca) vaccine: data from the French network of regional pharmacovigilance centres. Therapie. 2021;76(4):369-373.
- Greinacher A, Thiele T, Warkentin TE, Weisser K, Kyrle PA, Eichinger S. Thrombotic Thrombocytopenia after ChAdOx1 nCov-19 Vaccination. N Engl J Med. 2021;384(22):2092-2101.
- Greinacher A, Thiele T, Warkentin TE, Weisser K, Kyrle P, Eichinger S. A prothrombotic thrombocytopenic disorder resembling heparin-induced thrombocytopenia following coronavirus-19 vaccination. Research Square. 2021;1-8.
- Jamme M, Mosnino E, Hayon J et al. Fatal cerebral venous sinus thrombosis after COVID-19 vaccination. Intensive Care Med. 2021;47(7):790-791.
- Jones M, Boisvert A, Landry J et al. Limb ischemia and pulmonary artery thrombosis after the ChAdOx1 nCoV-19 (Oxford-AstraZeneca) vaccine: a case of vaccine-induced immune thrombotic thrombocytopenia. CMAJ. 2021;193(24):E906-EE10.
- Mehta PR, Mangion SA, Benger M et al. Cerebral venous sinus thrombosis and thrombocytopenia after COVID-19 vaccination - a report of two UK cases. Brain Behav Immun. 2021; 95:514-517
- Mohanty E, Nazir S, Sheppard JAI et al. High-dose intravenous immunoglobulin to treat spontaneous heparin-induced thrombocytopenia syndrome. J Thromb Haemost. 2019;17(5):841-844.
- Muster V, Gary T, Raggam RB et al. Pulmonary embolism and thrombocytopenia following ChAdOx1 vaccination. Lancet. 2021;397(10287):1842.
- Öcal O, Stecher SS, Wildgruber M. Portal vein thrombosis associated with ChAdOx1 nCov-19 vaccination. Lancet Gastroenterol Hepatol. 2021;6(8):676.
- Oldenburg J, Klamroth R, Langer F et al. Diagnosis and management of vaccine-related thrombosis following AstraZeneca COVID-19 vaccination: guidance statement from the GTH. Hamostaseologie. 2021;41(3):184-189.
- Schultz NH, Sørvoll IH, Michelsen AE et al. Thrombosis and Thrombocytopenia after ChAdOx1 nCoV-19 Vaccination. N Engl J Med. 2021;384(22):2124-2130.
- Scully M, Singh D, Lown R et al. Pathologic Antibodies to Platelet Factor 4 after ChAdOx1 nCoV-19 Vaccination. N Engl J Med. 2021;384(23):2202-2211.
- Umbrello M, Brena, N Vercelli R et al. Successful treatment of acute spleno-porto-mesenteric vein thrombosis after ChAdOx1 nCoV-19 vaccine. A case report. J Crit Care. 2021;65:72-75.
- Vayne C, Rollin J, Gruel Y et al. PF4 Immunoassays in vaccine-induced thrombotic thrombocytopenia. N Engl J Med. 2021;385(4):376-378.
- Voysey M, Clemens SAC, Madhi SA et al. Safety and efficacy of the ChAdOx1nCoV-19 vaccine (AZD1222) against SARS-CoV-2: an interim analysis of four arandomised controlled trials in Brazil, South Africa, and the UK. Lancet. 2021;397(10269):99-111.
- Warkentin TE. High-dose intravenous immunoglobulin for the treatment and prevention of heparin-induced thrombocytopenia: a review. Expert Rev Hematol. 2019;12(8):685-698.
- Zanferrari C, Fanucchi S, Liberato NL et al. Excellent response to high-dose intravenous immunoglobulin in anti-PF4 positive cerebral thrombosis following ofxord-AstraZeneca AZD1222 vaccine. 2021. Updated April 12, 2021. Accessed May 24, 2021. https://www.researchsquare.com/article/rs-399801/v1.