¿Otros linfomas?: enfermedad de Castleman y virus herpes humano 8
Other lymphomas?: Castleman disease and human herpesvirus 8
Melchiori P1, Risau E2, Rodríguez-Zubieta M3, García L4, Real A4, Trucco J5, Romano V6.
- Bioquímica. Jefa de residentes en Bioquímica Clínica y Microbiología. Hospital Universitario Austral, Pilar, Buenos Aires, Argentina.
- Jefa de residentes en Anatomía Patológica. Hospital Universitario Austral, Pilar, Buenos Aires, Argentina.
- Médica Especialista en Anatomía Patológica. Hospital Universitario Austral, Pilar, Buenos Aires, Argentina.
- Bioquímica. Área de Biología Molecular- Laboratorio Central, Hospital Universitario Austral, Pilar, Buenos Aires, Argentina.
- Servicio de Hematología. Hospital Universitario Austral, Pilar, Buenos Aires, Argentina.
- Bioquímica. Coordinadora del Área de Biología Molecular- Laboratorio Central, Hospital Universitario Austral, Pilar, Buenos Aires, Argentina.
|
Melchiori Paulina |
0009-0001-4215-4345 |
|
Garcia María Ludmila |
0009-0007-3626-199X |
|
Real Alejandrina |
0009-0002-2669-4779 |
|
Romano Vanesa |
0000-0001-5239-7247 |
|
Trucco José |
0000-0003-3657-0470 |
|
Risau Estefanía |
0009-0002-7964-3190
|
|
Rodríguez Zubieta Mariana |
0009-0004-9875-8887 |
Palabras claves: desórdenes linfoproliferativos,
hiperplasia linfoide,
virología.
Keywords: lymphoproliferative disorders,
lymph hyperplasia,
virology.
Resumen
La enfermedad de Castleman constituye un grupo heterogéneo de desórdenes linfoproliferativos de baja frecuencia. Se clasifica según el número de áreas nodales afectadas en diferentes variantes: unicéntrica (UCD) o multicéntrica (MCD). A su vez, puede ser idiopática o estar relacionada con infecciones por el virus de inmunodeficiencia humana (VIH) y/o el virus herpes humano 8 (VHH8, también llamado herpes virus asociado al sarcoma de Kaposi). Ésta última se presenta con una frecuencia estimada de 1/100.000 personas. La enfermedad puede tener un curso clínico indolente o agresivo, con presentaciones, en casos graves, de falla multiorgánica. El diagnóstico se realiza mediante la identificación de alteraciones morfológicas en el ganglio afectado y técnicas de inmunohistoquímica (IHQ) con marcación del antígeno LANA-1 para evidenciar la presencia del VHH8. La detección del genoma viral en muestras de sangre se ha propuesto como un biomarcador para predecir el riesgo de recurrencia de la enfermedad y así instaurar un tratamiento precoz. Describimos el caso clínico de un paciente masculino de 65 años, HIV negativo que presentó en 2018 síntomas B, sumado a debilidad muscular y poliadenomegalias. Rápidamente el cuadro clínico progresó a falla multiorgánica. Fue diagnosticado con enfermedad de Castleman multicéntrica asociada a VHH8, para la cual recibió tratamiento, logrando la remisión completa. En 2021 presentó una primera recaída que, después de recibir un tratamiento diferente, condujo a una segunda remisión. Durante su seguimiento mediante diferentes parámetros bioquímicos, hacia fines de 2023 y principios del 2024, se detectó un aumento sostenido de la carga viral de VHH8. Debido a que el paciente no presentó síntomas adicionales ni nuevos hallazgos en los estudios de imágenes, se decidió una conducta expectante y monitoreo estricto. Existen reportes que sugieren que la reactivación viral podría predecir la recaída clínica de la enfermedad, incluso planteándose posibles estrategias preventivas tempranas frente a este evento, pero actualmente no hay un consenso sobre su aplicación sistemática en la práctica clínica.
Consideramos que podría ser relevante el seguimiento de la carga viral de VHH8 en pacientes con enfermedad de Castleman a lo largo de su tratamiento. Sin embargo, dada la baja prevalencia de la enfermedad, es necesario el estudio de un número mayor de casos para poder establecerlo.
Summary
Castleman disease constitutes a heterogeneous group of low-frequency lymphoproliferative disorders. It is classified based on the number of affected nodal areas into different variants: unicentric (UCD) or multicentric (MCD). In turn, it can be idiopathic or associated with infections by the human immunodeficiency virus (HIV) and/or human herpesvirus 8 (HHV-8, also known as Kaposi's sarcoma-associated herpesvirus). The latter has an estimated frequency of 1 in 100,000 people. Castleman disease can exhibit an indolent or aggressive clinical course, with severe cases leading to multi-organ failure. Diagnosis is based on identifying morphological abnormalities in the affected lymph node and immunohistochemistry (IHC) techniques using LANA-1 antigen staining to confirm the presence of HHV-8. Detection of the viral genome in blood samples has been proposed as a biomarker to predict disease recurrence risk, enabling early treatment initiation. We present the clinical case of a 65-year-old male patient, HIV-negative, who in 2018 developed B symptoms along with muscle weakness and generalized lymphadenopathy. The clinical picture rapidly progressed to multiorgan failure. He was diagnosed with HHV-8-associated multicentric Castleman disease, for which he received treatment, achieving complete remission. In 2021, the patient experienced his first relapse, which, after receiving a different treatment, led to a second remission. During follow-up through various biochemical parameters, a sustained increase in HHV-8 viral load was detected between late 2023 and early 2024. Since the patient did not exhibit additional symptoms or new findings on imaging studies, a decision was made to adopt a watchful waiting approach with strict monitoring. Reports suggest that viral reactivation could predict clinical relapse of the disease, with potential early preventive strategies being proposed for this event. However, there is currently no consensus on its systematic application in clinical practice. We believe that monitoring HHV-8 viral load in patients with Castleman disease throughout their treatment could be relevant. However, given the low prevalence of the disease, a larger number of cases needs to be studied to establish this.
Introducción
La enfermedad de Castleman constituye un grupo heterogéneo de desórdenes linfoproliferativos de baja frecuencia, actualmente agrupados bajo la categoría “Lesiones tipo tumorales con predominio de células B”. Se clasifica en diferentes variantes según el número de áreas nodales afectadas: unicéntrica (UCD) o multicéntrica (MCD)(1,2). A su vez, puede ser idiopática o estar relacionada con infecciones por el virus de inmunodeficiencia humana (VIH) y/o el virus herpes humano 8 (VHH8, también llamado herpes virus asociado al sarcoma de Kaposi). Ésta última se presenta con una frecuencia estimada de 1/100.000 personas(3,4).
El VHH8 infecta a las células B y plasmoblastos, donde persiste en estado de latencia. Los principales síntomas clínicos son mediados por el aumento de IL-6, asociados al mimetismo molecular de vIL-6 (interleuquina 6 viral). Durante la infección lítica (o fase replicativa), y en menor grado durante la infección latente, las células B infectadas por VHH8 segregan vIL-6 que activa al receptor IL-6 humano (gp130) sin necesitar de su correceptor (gp80), a diferencia de la IL-6 humana. Se ha observado que, en algunos casos, las células infectadas con HHV-8 son altamente proliferativas y pueden fusionarse para formar los llamados "microlinfomas" o dar lugar a un linfoma difuso de células B grandes o linfoma primario de efusiones (4).
Clínicamente esta entidad se caracteriza por la presencia de adenomegalias, hepatoesplenomegalia, falla renal, reactantes de fase aguda aumentados (principalmente proteína C), anemia, hipergammaglobulinemia policlonal y síntomas B (fiebre, sudoración y pérdida de peso). La enfermedad de Castleman unicéntrica es de curso benigno y su pronóstico es bueno, a diferencia de la multicéntrica, la cual suele requerir tratamientos más agresivos. En casos graves puede observarse falla multiorgánica de rápida instauración.
El diagnóstico anatomopatológico se realiza mediante la identificación morfológica en el ganglio afectado de hiperplasia folicular y/o vascular, regresión de los centros germinales, capilares hialinizados, así como expansión y distribución concéntrica de las células en la zona del manto(5). Mediante técnicas de inmunohistoquímica (IHQ) con marcación del antígeno LANA-1 (latent nuclear antigen) es posible detectar presencia o ausencia del VHH8. Aproximadamente el 30% de los linfocitos B alrededor del centro germinal suelen estar infectados con VHH8, que están restringidos a la expresión de cadena liviana IgMλ(6). La detección del genoma viral en muestras de sangre se ha propuesto como un biomarcador para predecir el riesgo de recurrencia de la enfermedad y así instaurar un tratamiento precoz o preventivo(7,8).
Caso clínico
Paciente masculino de 65 años, HIV negativo, oriundo de Bolivia, que presentó en julio de 2018 síntomas B como astenia, pérdida de peso, fiebre y sudoración nocturna, sumado a debilidad muscular y poliadenomegalias. Presentó una evolución rápida que progresó a falla multiorgánica, por lo que fue evaluado en un centro médico en Chile, arribando al diagnóstico de enfermedad de Castleman multicéntrica (MCD) asociada a VHH8. Realizó tratamiento con metilprednisolona, rituximab y etopósido, logrando remisión completa de la enfermedad.
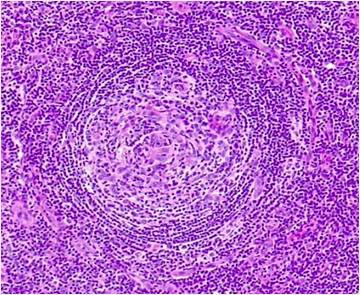
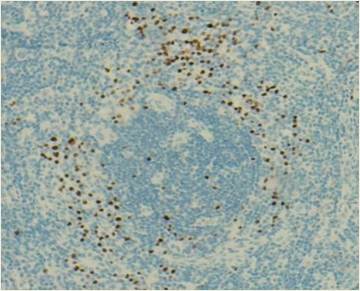
En febrero de 2019 decidió continuar el seguimiento médico de su enfermedad en nuestra institución. En dicho momento se encontraba asintomático, sin parámetros de actividad de la enfermedad y con carga viral de VHH8 no detectable. En diciembre de 2020 presentó recaída de la enfermedad con síntomas B, citopenias y valores de ferritina elevados. Se realizó una nueva biopsia escisional, en la cual se confirmó el diagnóstico mediante morfología e IHQ, evidenciando alteraciones en el tejido y células LANA-1 positivas en la zona del manto (Figuras 1 y 2). Adicionalmente, se realizaron estudios complementarios y de laboratorio para la evaluación del estado de la enfermedad. En estudios por imágenes se observaron ganglios linfáticos aumentados en zona infra y supra diafragmática, hepato-esplénicos y mediastinales. Recibió tratamiento con rituximab y doxorrubicina liposomal, logrando una segunda remisión completa.
|
Figura 1
|
Figura 2
|
|
Biopsia de ganglio axilar derecho. Corte histológico teñido con hematoxilina eosina (40x). Se observa un folículo linfoide con centro germinal atrófico e hiperplasia de la zona del manto con linfocitos dispuestos en capas concéntricas. |
Biopsia de ganglio axilar derecho. Inmunomarcación para LANA-1 (40x). Se observa positividad en células de la zona del manto. |
Durante el período comprendido entre diciembre 2020 y abril 2024, se realizó el seguimiento con carga viral (CV) de VHH8 plasmática por PCR en tiempo real (TIB MOLBIOL-Roche) y parámetros inflamatorios como eritrosedimentación (VSG), proteína C reactiva (PCR), hemoglobina (Hb), lactato deshidrogenasa (LDH) y ferritina (Tabla 1).
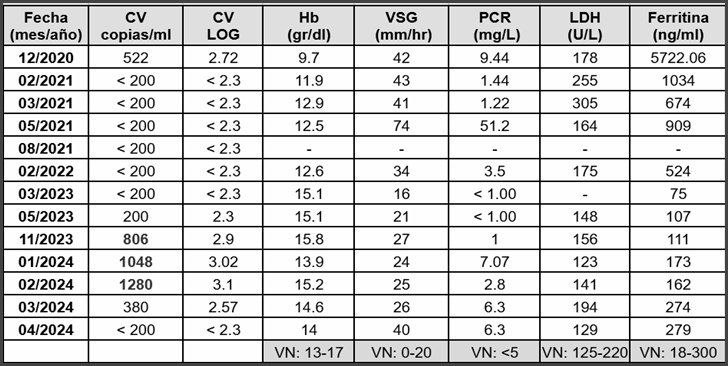
Tabla 1. Parámetros bioquímicos de seguimiento.
*Cv<200 o no detectable.
Abreviaturas. CV: carga viral, Hb: hemoglobina, VSG: velocidad de sedimentación globular, PCR: proteína C reactiva, LDH: lactato deshidrogenasa.
Estos parámetros se mantuvieron no detectables o dentro de los valores de referencia hasta fines de 2023, cuando se observó un aumento de CV: 806 (2.9 log) copias/ml (11/2023), 1048 (3,02 log) copias/ml (01/2024) y 1280 (3,1 log) copias/ml, lo que podría asociarse a una reactivación viral. Ante estos resultados, se discutió el inicio precoz del tratamiento. Sin embargo, debido a que el paciente no presentaba ningún otro síntoma o signo de actividad de la enfermedad, y valores normales de PCR, se decidió una conducta expectante y seguimiento estricto. En estudios posteriores se evidenció descenso de CV: 380 (2,57 log) copias/ml (03/2024) y <200 (<2,3 log) copias/ml (04/2024).
Discusión y conclusiones
Debido a la baja prevalencia del VHH8, su detección es poco frecuente en laboratorios clínicos, pero es relevante considerar el seguimiento de la CV en pacientes con enfermedad de Castleman asociada a este virus, de manera tal de monitorizar la respuesta al tratamiento.
Se plantea la hipótesis de que el estado hiperproliferativo inducido por el VHH8 puede generar la acumulación de mutaciones en los genomas de las células B infectadas, que permite su supervivencia y, con el tiempo, pueden llegar a convertirse en un linfoma manifiesto.
Existen reportes que sugieren que la reactivación viral puede preceder a la actividad manifiesta de la enfermedad. Recientemente se publicó un trabajo en el cual el aumento de 3 log en la CV del VHH8, un nivel sérico de PCR ≥ 20 mg/L, y el status negativo de HIV se asociaron de manera independiente al riesgo de recaída de la enfermedad en los 2 siguientes años, si bien alrededor del 50% de los pacientes no progresaron(8). En la actualidad no existe un consenso sobre la conducta médica a tomar frente a la evidencia de reactivación viral en pacientes asintomáticos y sin enfermedad manifiesta. La conducta debe ser individualizada en cada caso particular, pudiéndose plantear el uso de rituximab monoterapia como estrategia preventiva en pacientes que presentan aumento sostenido de la carga viral de VHH8, sin enfermedad clínicamente manifiesta. Sin embargo, es necesario contar con mayor evidencia para comprender mejor el seguimiento y tratamiento de los pacientes con esta entidad.
Bibliografía
- Alaggio R, Amador C, Anagnostopoulos I et al. The 5th edition of the World Health Organization Classification of Hematolymphoid Tumors: Lymphoid Neoplasms. Leukemia. 2022;36(7):1720-1748. doi:10.1038/s41375-022-01620-2.
- Pertusa Mataix R, Loaiza Cabello D, García Morillo JS. Castleman's disease, pathophysiology, advances in diagnosis and treatment. Med Clin (Barc). 2024;162(6):283-290. doi:10.1016/j.medcli.2023.10.013.
- Fajgenbaum DC, Uldrick TS, Bagg A et al. International, evidence-based consensus diagnostic criteria for HHV-8-negative/idiopathic multicentric Castleman disease. Blood. 2017;129(12):1646-1657. doi:10.1182/blood-2016-10-746933.
- HHV-8/KSHV-associated multicentric Castleman disease - UpToDate. Agosto 2024.
- www.castleman.fr/diagnostic-et-classification-de-la-maladie.
- Carbone A, Borok M, Damania B et al. Castleman disease. Nat Rev Dis Primers. 2021;7:84. https://doi.org/10.1038/s41572-021-00317-7.
- Stebbing J, Adams C, Sanitt A et al. Plasma HHV8 DNA predicts relapse in individuals with HIV-associated multicentric Castleman disease. Blood. 2011;118(2):271-275. doi:10.1182/blood-2011-02-335620.
- Rasmussen C, Gérard L, Fadlallah J et al. Higher rate of progression in HIV- than in HIV+ patients after rituximab for HHV8+ multicentric Castleman disease. Blood Adv. 2023;7(18):5663-5669. doi:10.1182/bloodadvances.2023010316.