Leucemia aguda con cambio de linaje: reporte de caso clínico y revisión bibliográfica
Acute leukemia with lineage switch: a clinical case report and comprehensive literature review
Fernández D1; Maymó D1; Bandin M1; Oliveira N1; Benegas M2; Villalba D1
1 Servicio Hematología-Hospital Nacional Profesor Alejandro Posadas.
2 Servicio Citometría de Flujo-Hospital Nacional Profesor Alejandro Posadas.
Colaboración del equipo de Citometría de Flujo: Vázquez M, Verónica.
-Daiana Fernández 0009-0004-5981-1809
-Mariana Bandin 0009-0008-7462-0196
-Natalia Oliveira 0009-0004-0183-4506
-Juan Carlos Villalba 0009-0004-7702-1552
-Belén Venegas 0000-0003-2781-6096
-Daniela Maymo 0000-0001-6821-031X
Palabras clave: cambio de linaje,
leucemia aguda,
epigenética,
mieloide,
linfoblástica.
Keywords: lineage switch,
acute leukemia,
epigenetics,
myeloid,
lymphoblastic.
Resumen
Las leucemias agudas son enfermedades neoplásicas caracterizadas por la proliferación de blastos en la médula ósea y/o en los órganos linfoides y presentan una mayor frecuencia en la edad pediátrica(1,2). Aunque el pronóstico de estas patologías ha mejorado en los últimos años gracias a nuevas estrategias terapéuticas, diversos factores pueden afectar la posibilidad de recaída o refractariedad al tratamiento, como es el caso del cambio de linaje(3). Éste último, en particular, está asociado con un pronóstico desfavorable. En el presente reporte se describe un caso clínico con transición de leucemia linfoblástica aguda a leucemia mieloide aguda, destacando las implicancias terapéuticas y pronósticas de este fenómeno.
Abstract
Acute leukemias are neoplastic disorders characterized by the proliferation of blasts in the bone marrow and/or lymphoid organs, with a higher incidence in the pediatric population(1,2). Despite recent advances in therapeutic strategies that have improved the prognosis of these conditions, several factors can adversely affect the likelihood of relapse or treatment resistance, including lineage switch(3). This phenomenon, in particular, is associated with a poor prognosis. This report presents a clinical case of lineage switch from acute lymphoblastic leukemia to acute myeloid leukemia, emphasizing the therapeutic and prognostic implications of a lineage switch.
Introducción
Según la Organización Mundial de la Salud (OMS), en los últimos años se han registrado 18.1 millones de casos nuevos de cáncer, constituyéndose las leucemias como el décimo cáncer más frecuente, con 437 mil casos nuevos y 211 mil muertes a nivel mundial(4). Las leucemias agudas, según la OMS, se clasifican como neoplasias de tejidos hematopoyéticos y linfoides, y de acuerdo al linaje se corresponden a linfoides o mieloides(5).
En cuanto a la incidencia y pronóstico, existen diversos factores que pueden considerarse, ya sean inherentes al paciente o relacionados con la enfermedad, tales como el tipo de leucemia, alteraciones moleculares, citogenéticas y la respuesta al tratamiento. Aunque los avances en las estrategias terapéuticas han mejorado el pronóstico, factores como el cambio de linaje, de linfoide a mieloide o viceversa, pueden tener un impacto adverso significativo en el pronóstico, especialmente en términos de recaídas y refractariedad(6,7). Los mecanismos subyacentes a este fenómeno infrecuente de cambio de linaje son diversos, aún no completamente comprendidos, y están en constante investigación(3). En este reporte, presentamos el caso de un paciente que experimentó un cambio de linaje de leucemia linfoblástica aguda (LLA) a leucemia mieloide aguda (LMA).
Presentación de caso clínico
Paciente masculino de 20 años, sin antecedentes previos de relevancia. Ingresa con cuadro de astenia, adinamia; laboratorio que reporta tricitopenia. En extendido de sangre periférica y medula ósea se constata 80% de células inmaduras de características linfoides (Figura 1), llegando al diagnóstico mediante citometría de flujo de médula ósea, de leucemia linfoblástica B (LLA B) fenotipo común, con el siguiente inmunofenotipo: 16% células de pequeño tamaño y complejidad citoplasmática: CD45(-), CD19+, CD38-/+d, CyCD79a+, CyCD3(-), CD3(-), CyMPO(-), CD7(-), CD34+, CD20(-), CD10+, CD66c/CD123+, CD81++, CD73/CD304(-), CD58++, CD33(-), CD13-/+v, CD22+, CD24+, CD9+, nuTDT+, CD15/CD65(-), NG2(-), CD123+v, CyIgM(-), IgM(-), kappa(-), lambda (-). 72% células de mediano a gran tamaño y complejidad citoplasmática: CD45+d, CD19+, CD38+, CyCD79a+, CyCD3(-), CD3(-), CyMPO(-), CD7(-), CD34+, CD20(-), CD10++, CD66c/CD123+, CD81++, CD73/CD304(-), CD58++, CD33(-), CD13-/+v, CD22+, CD24+, CD9+, nuTDT+, CD15/CD65(-), NG2(-), CD123+v, CyIgM(-), IgM(-), kappa(-), lambda (-) (Figura 2). Se realiza cariotipo de médula ósea y biología molecular sin alteraciones en panel linfoide. No se evidencia compromiso de sistema nervioso central. Se inicia esquema GATLA-AYA(8), fase IA, con enfermedad medible residual (EMR) día +33 negativa. Inicia fase IB, evolucionando con tricitopenia persistente, por lo que se realiza punción aspirativa de médula ósea: células patológicas 5% de mediano a gran tamaño CD45++, cyMPO+d, cyCD79a(-), cyCD3(-), CD34+, HLA-DR++, CD117-/+d, CD123-/+, CD13++, CD33++, CD15(-), CD16(-), CD11b-/+v, CD64(-), CD14(-), CD35+d, CD71-/+, CD56(-), CD7(-), CD36(-), IREM2(-), CD105(-), fenotipo vinculable a blastos mieloides. No se observan blastos linfoides B en 200.000 eventos analizados (muestra de médula ósea hipocelular). (Figura 3). Se reevalúa cariotipo y biología molecular en médula ósea, sin alteraciones en panel mieloide. Se interpreta como cambio de linaje y se decide rotar tratamiento a esquema para LMA: MAE (mitoxantrona/citarabina/etopósido) – HAM (altas dosis citarabina/mitoxantrona) con persistencia de EMR positiva, por lo que se plantea realizar esquema rescate con FLAGIDA + gemtuzumab. Recibe únicamente FLAGIDA por falta de disponibilidad de gemtuzumab, alcanzando EMR negativa. Inicia mantenimiento con azacitidina +
 |
venetoclax, a la espera de trasplante alogénico no relacionado, dado que no cuenta con hermanos histocompatibles.
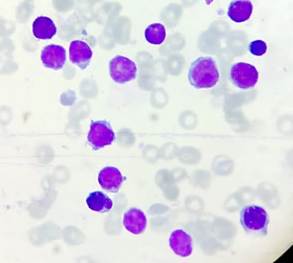
Figura 1
Figura 1. Células de tamaño pequeño a mediano, citoplasma escaso, núcleo con cromatina laxa, con presencia de nucléolos (extendido de médula ósea x 100).
 Figura
2
Figura 3
Figura
2
Figura 3
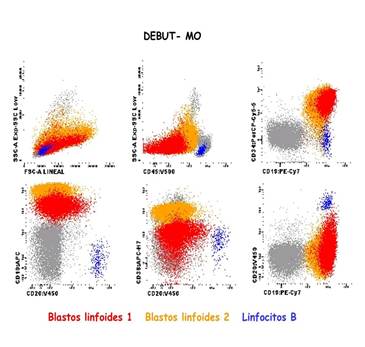
Figura 2. Citometría de flujo de médula ósea, al debut: leucemia linfoblástica B.
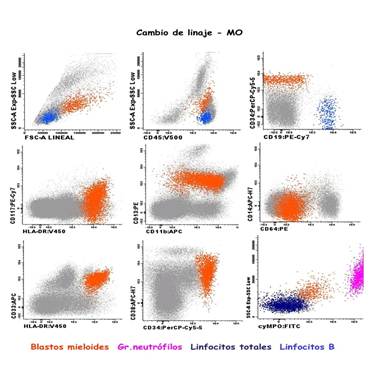
Figura 3. Citometría de flujo de médula ósea, a la recaída: cambio de linaje a leucemia mieloide aguda.
Discusión
Presentamos el caso de un paciente con diagnóstico inicial LLA de tipo B que experimentó un cambio de linaje a LMA, un fenómeno extremadamente infrecuente. Actualmente existe evidencia que documenta cambio de linaje en la evolución de las leucemias agudas. Aunque la patogénesis exacta aún no está completamente esclarecida, se han propuesto varias teorías para explicar la plasticidad y multidireccionalidad de las células leucémicas(3,7).
Entre estas teorías, se destaca el papel de una red de factores de transcripción que guían la diferenciación celular. En el desarrollo mieloide los factores involucrados incluyen RUNX1, SCL, Ikaros y GFI-1; mientras que el desarrollo linfoide B está regulado por PU.1, E2A, EBF y Pax5. Por otra parte, el desarrollo T parece depender del silenciamiento de Pax5 y de la expresión de GATA-3 y Notch(9,10).
Se ha propuesto que las células progenitoras bipotenciales u oligopotenciales tempranas, con sus variados perfiles de expresión génica, podrían ser el origen de translocaciones leucemogénicas y, por ende, del cambio de linaje(11). Los cambios epigenéticos también podrían desempeñar un papel crucial en este fenómeno, ya que activan genes esenciales para la pluripotencialidad y la reprogramación celular. Las modificaciones en la cromatina son fundamentales para la dirección y diferenciación celular(12).
Rossi y col. destacan la importancia de los genes de fusión MLL en la leucemia aguda, remarcando su asociación con cambios de linaje. Las características biológicas y clínicas distintivas de MLL-AL, incluyendo perfiles de marcadores únicos en casos infantiles como la negatividad para CD10 y la co-expresión de antígenos mieloides (CDw65 y CD15), apoyan aún más el argumento de que las leucemias positivas para MLL representan una entidad distinta. La alta frecuencia de cambios de linaje en leucemias MLL-positivas, en comparación con otras leucemias, sugiere que MLL-AL se origina a partir de un precursor inmaduro(13). Es importante destacar que nuestro caso no presentaba este perfil de expresión fenotípico mencionado.
Las alteraciones recurrentes en EZH2 y KMT2A subrayan el papel de la disfunción epigenética en el cambio de linaje leucémico. Algunos factores de riesgo para este cambio incluyen pacientes pediátricos, fusiones 11q23/KMT2A, LLA B con mutaciones en EZH2 o RUNX1 o con otras anomalías genéticas asociadas con neoplasias mieloides. La presencia de estos factores de riesgo requiere una evaluación inmunofenotípica detallada de varios linajes celulares, especialmente tras el tratamiento o en caso de recaída, para detectar de manera oportuna un cambio de linaje(14). Cabe mencionar que en nuestro caso dichas alteraciones no fueron detectadas al debut como tampoco en la recaída con el cambio de linaje, ya que no tenemos disponible la evaluación por NGS (Next-generation sequencing).
Además, la selección clonal es otro mecanismo potencialmente implicado en la expansión de subclones leucémicos con fenotipos diferentes en las recaídas. Por ejemplo, en pacientes con un clon preleucémico/leucémico TEL/AML1+, se observa una gran variabilidad en los reordenamientos a lo largo de la evolución de la leucemia. Esto sugiere que la quimioterapia puede erradicar el clon leucémico inicial, permitiendo la expansión de un subclon con un fenotipo diferente en la recaída. Otra posible explicación fisiopatológica podría ser la “selección” de una población minoritaria de células preexistentes, insensibles a la quimioterapia y de un linaje diferente al de la población mayoritaria al diagnóstico (leucemias bifenotípicas o bilineales), con la consiguiente aparición de un “subclon” resistente que expresa un repertorio diferente de antígenos(15). Este último ejemplo se menciona en reportes de casos de cambio de linaje con el uso de blinatumomab, en los que tras la supresión de CD19, las células pasarían por una reprogramación nuclear, con adquisición de un fenotipo mieloide(16).
Finalmente, las señales en el microambiente medular pueden influir en la determinación del destino celular, dado que existe una relación estrecha entre el desarrollo de la hematopoyesis y el microambiente. Estas señales modificarían la comunicación entre las células madre y su nicho en la médula ósea, lo que podría tener un impacto en el cambio de linaje y la evolución de la leucemia(17).
El cambio de linaje en leucemia aguda conlleva implicancias terapéuticas significativas. La transición de un tipo de leucemia a otro puede alterar el perfil fenotípico y genético de las células neoplásicas. Esta reprogramación puede resultar en una resistencia a los regímenes terapéuticos previamente utilizados, que a menudo están dirigidos a características específicas de un linaje leucémico particular. Como consecuencia, es imperativo ajustar las estrategias terapéuticas en respuesta al nuevo perfil celular, con implementación de esquemas de tratamiento alternativos o terapias dirigidas o trasplante de células madre hematopoyéticas, adaptados al nuevo fenotipo leucémico. Es importante destacar que este fenómeno está asociado con un pronóstico desfavorable, lo que subraya la necesidad de una vigilancia rigurosa de la EMR y un manejo proactivo para controlar las posibles recaídas y la refractariedad al tratamiento.
Conclusión
El presente reporte de caso ilustra las implicancias biológicas y terapéuticas asociadas con el cambio de linaje en leucemias agudas, ejemplificado por la transición de leucemia linfoblástica aguda (LLA) de tipo B a leucemia mieloide aguda (LMA). Este fenómeno infrecuente puede modificar de manera drástica el perfil fenotípico y genético de las células leucémicas, lo que conlleva consecuencias importantes para el manejo terapéutico. La identificación y abordaje precoz de estos cambios son cruciales para la optimización de las estrategias de tratamiento. Es relevante señalar que el cambio de linaje está asociado con un pronóstico desfavorable, subrayando la necesidad de una vigilancia estricta de enfermedad residual medible y una intervención temprana para manejar de manera eficaz las recaídas y la refractariedad al tratamiento. La investigación continua de los mecanismos biológicos subyacentes al cambio de linaje es esencial para el desarrollo de estrategias terapéuticas más efectivas y para la mejor supervivencia de los pacientes. Este caso enfatiza la importancia de adoptar un enfoque multidisciplinario con técnicas de citometría de flujo, biología molecular y genética, con el objetivo de facilitar un diagnóstico temprano y un tratamiento adecuado de estos pacientes.
Bibliografía
1. Alaggio R, Amador C. Anagnostopoulos I et al. The 5th edition of the World Health Organization Classification of Haematolymphoid Tumours: Lymphoid Neoplasms. Leukemia. 2022; 36:1720-1748.
2. NCCN Clinical Practice Guidelines in Oncology (NCCN Guidelines®) Acute Lymphoblastic LeukemiaVersion1.2023 NCCN.
3. Dorantes E, Pelayo R. Cambio de linaje en leucemias agudas: ¿una consecuencia de la plasticidad de las células madre? Bone Marrow Research. 2012.
4. Organización Mundial de la Salud (OMS). Últimos datos mundiales sobre el cáncer. https://www.who.int/cancer/PRGlobocanFinal.pdf [consultado el 10 de enero de 2020].
5. Organización Mundial de la Salud (OMS). CIE-11 para estadísticas de mortalidad y morbilidad. https://icd.who.int/browse/2024-01/mms/es#460184638. (Consultado en enero 2024).
6. T. Hao, T. Li, MA Buck, A. Buck, W. Chen. Una tendencia emergente es el rápido aumento de la leucemia, pero no de todos los cánceres, en la población que envejece en los Estados Unidos. Sci Rep. 2019;9:12070.
7. Pandit S, Wasekar N, Badarje G et al. De leucemia linfoblástica aguda a leucemia mieloide aguda: informe de un caso inusual de cambio de linaje. Asociación Brasileña de Hematología, Hemoterapia y Terapia celular. 2022;44(1):112-115.
8. Guía de tratamiento protocolizada por GATLA 11-LLA Ph(-)-20 AYA, adultos, adultos mayores.
9. Baba Y, Pelayo R, Kincade PW. Relaciones entre células madre hematopoyéticas y progenitores de linfocitos. Tendencias en Inmunología. 2004; 25(12):645-649.
10. Perez-Vera P, Reyes-Leon A, Fuentes-Panana EM. Proteínas de señalización y factores de transcripción en el desarrollo temprano de células B normales y malignas. Bone Marrow Research. 2011; 2011 502751.
11. Pui CH, Raimondi SC, Behm FG. Cambios en el fenotipo y cariotipo de las células blásticas en la recaída de la leucemia linfoblástica infantil. Blood. 1986;68 (6):1306-1310.
12. Zardo G, Cimino G, Nervi C. Plasticidad epigenética de la cromatina en células madre/progenitoras embrionarias y hematopoyéticas: potencial terapéutico de la reprogramación celular. Leucemia. 2008;22(8):1503-1518.
13. GJ Ruiz-Delgado, AK Nuñez-Cortez et al. Cambio de linaje de leucemia linfoblástica aguda a leucemia mieloide. Medicina Universitaria. 2017;19(74):27-31.
14. Zhou T, Curry CV, Khanlari M et al. Genetics and pathologic landscape of lineage switch of acute leukemia during therapy. Blood Cancer J. 2024 Jan 25;14(1):19. doi: 10.1038/s41408-024-00983-2..
15. Panzer-Grümayer ER, Cazzaniga G, Van Der Velden VHJ et al. Los cambios en el inmunogenotipo prevalecen en las recaídas de niños pequeños con leucemia linfoblástica aguda TEL-AML1-positiva y derivan principalmente de la selección clonal. Clinical Cancer Research. 2005;11(21):7720-7727.
16. Haddox CL, Mangaonkar AA, Chen D et al. Blinatumomab-induced lineage switch of B-ALL with t(4:11)(q21;q23) KMT2A/AFF1 into an aggressive AML: pre- and post-switch phenotypic, cytogenetic and molecular analysis. Blood Cancer J. 2017 Sep 15;7(9):e607. doi: 10.1038/bcj.2017.89.
17. Purizaca J, Meza I, Pelayo R. Desarrollo linfoide temprano y señales microambientales en la leucemia linfoblástica aguda de células B. Archives of Medical Research. 2012;43(2):89-101.