Linfoma de células T intestinal asociado enteropatía y enfermedad celíaca
Intestinal T-cell lymphoma associated to enteropathy and celiac disease
María Fernanda Cueva Urbina1, Joselyn Sánchez2, Juan Rosero2, Carlos Martin3, Teófilo de Luca2, Alicia Enrico2, Carlos Ponzinibbio2
1. Hospital Nacional Dos de Mayo, Lima, Perú,
2. Hospital Italiano, La Plata, Argentina,
3. Consultorio de Hematopatología, La Plata, Argentina
María Fernanda Cueva Urbina: https://orcid.org/0000-0002-4815-7854
Joselyn Sánchez: https://orcid.org/0009-0000-1764-4951
Alicia Enrico: https://orcid.org/0000-0002-1983-6145
Carlos Ponzinibbio: https://orcid.org/0000-0003-4610-916X
Teófilo De Luca: https://orcid.org/0009-0009-7003-7718
Carlos Martin: https://orcid.org/0000-0001-9501-2028
Juan Ronsero: https://orcid.org/0009-0001-3416-2644
Palabras clave: linfoma de células T,
enteropatía
enfermedad celíaca,
enfermedad celíaca refractaria.
Keywords: T cell lymphoma,
enteropathy,
celiac disease,
refractory celiac disease.
Resumen
El linfoma de células T asociado a enteropatía es un tipo agresivo y raro de linfoma T periférico, frecuentemente asociado a la enfermedad celíaca. La ingesta inadvertida y prolongada de gluten es la principal causa de falta de respuesta a la dieta, con probabilidad de desarrollo del estado refractario conocido como enfermedad celíaca refractaria (ECR). La ECR se divide en 2 tipos: I y II, considerándose actualmente la ECR tipo II como un estado pre-linfomatoso. La ingesta continua de gluten en el paciente celíaco constituye un estímulo inflamatorio persistente, determinando una perturbación de la homeostasis linfocitaria intestinal que puede ser considerada como origen de este linfoma. Se considera a un linfocito T intraepitelial aberrante como blanco de la transformación neoplásica, al adquirir en este proceso la capacidad de proliferación clonal y escape de las principales vías apoptóticas. Se presenta un caso ilustrativo de un paciente de 62 años cuyo diagnóstico de enfermedad celíaca se realizó conjuntamente con el de la neoplasia maligna, y se analizan elementos que coinciden en la relación patogénica de ambas entidades.
Abstract
Enteropathy-associated T-cell lymphoma is a rare and aggressive type of peripheral T-cell lymphoma, frequently associated with celiac disease. Refractory celiac disease (RCD), the main cause of lack of response to the diet may be developed after the inadvertent and prolonged ingestion of gluten. Two types of RCD are recognized: type I and type II, while type II is currently considered a pre-lymphomatous state. The persistence of an inflammatory stimulus posed by the continuous intake of gluten in celiac patients determine a disturbance of intestinal lymphocyte homeostasis, raising the possibility to evolve to a lymphoma. The target of malignant transformation appears to be an intraepithelial lymphocyte developing increased proliferation potential and apoptosis escape. A 62-year-old male case is presented as illustration of the possible relationship between these two entities as the mechanisms intertwined between.
Introducción
La enfermedad celíaca (EC) es una enfermedad autoinmune del intestino delgado mediada por linfocitos T, causada por la exposición a la gliadina del gluten en pacientes genéticamente susceptibles. La susceptibilidad genética está dada por la presencia de alelos específicos clase II del sistema HLA, más frecuentemente DQ2, aunque en una frecuencia mucho menor, se puede asociar a DQ8. Los casos raros que son negativos para estos alelos pueden ser positivos para HLA-DQ7.5. La EC afecta aproximadamente al 1% de la población, y se puede desarrollar a cualquier edad, aunque la mayoría de los casos se diagnostican en niños y adultos jóvenes. La clínica de presentación de la EC es amplia y variada, y comprende desde casos oligosintomáticos hasta estados mórbidos severos por el déficit de absorción de nutrientes esenciales. Así mismo, se puede observar la afectación de sitios extra-intestinales, con expresión de síntomas neurológicos, endócrinos, cutáneos, óseos y/o cambios en la función reproductiva. Dado el daño inflamatorio crónico de la mucosa intestinal, la persistencia de esta injuria puede conducir al desarrollo de complicaciones graves, como el adenocarcinoma intestinal o formas agresivas de linfomas T.
La enfermedad celíaca refractaria (ECR), descrita por Trier et al en 1978 en pacientes con atrofia vellositaria y diarrea persistente, se define como la ausencia de mejoría clínica y/o histológica tras al menos 6 a 12 meses de dieta con restricción en gluten(5). Tiene una frecuencia menor del 5% en los pacientes con diagnóstico de EC y se divide en 2 tipos: enfermedad celíaca refractaria tipo I (ECR-I) y la enfermedad celíaca refractaria tipo II (ECR-II), acorde a la presencia de linfocitos intestinales intraepiteliales (LIE) normales (tipo I) o la presencia de LIE aberrantes (tipo II)(5). La primera se caracteriza por una población normal de linfocitos intraepiteliales sin atipía, con expresión del receptor de células T de superficie normal, expresión positiva de CD3 y CD8(7) y patrón policlonal. La enfermedad celíaca refractaria tipo II (ECR-II) presenta LIE aberrantes que expresan CD103, sin expresión de CD3 ni CD8 en su superficie, y mantienen expresión de CD3 intracelular con reordenamiento clonal de los genes del receptor de células T. Por estas características es denominado como “linfoma críptico intestinal de células T”, entidad considerada como un linfoma T de bajo grado. Es poco probable que la ECR-I progrese a linfoma de células T asociado a enteropatía o EATL (denominado así por sus siglas en inglés), mientras que la ECR-II es considerada como una lesión precursora del mismo. Sin tratamiento adecuado, entre el 60-80% de los pacientes con ECR-II desarrollan un EATL en un plazo de cinco años(1).
El EATL es un tipo de LNH agresivo e infrecuente, anteriormente denominado erróneamente “histiocitosis maligna del intestino”(17). Considerado como la complicación neoplásica más frecuente, se asocia a la enfermedad celíaca y encuentra su origen en la transformación maligna de linfocitos intestinales intraepiteliales (LIE). Si bien anteriormente era clasificado en 2 subtipos: EATL tipo 1, asociado a enfermedad celíaca y EATL tipo 2, de novo, actualmente, este último se reconoce como una entidad separada y ya no como una variante del linfoma de células T asociado a enteropatía (EATL). Dadas sus características clínico-patológicas, a partir de 2016, la clasificación de la World Health Organization (WHO) designa a esta entidad como linfoma de células T intestinal monomórfico epiteliotrópico (MEITL por sus siglas en inglés)(4).
Caso clínico
Se presenta el caso de un paciente varón de 62 años de edad al momento del ingreso al Hospital, sin antecedentes patológicos de importancia. Entre los antecedentes familiares, se destacó la referencia de una sobrina con enfermedad celíaca, con diagnóstico establecido a los 20 años. El cuadro clínico del paciente inició aproximadamente 6 meses antes de recibir atención médica, caracterizado por pérdida progresiva de peso de unos 20 kilos, diaforesis profusa, hiporexia y dolor abdominal , tipo cólico, asociado a distensión abdominal. Cabe resaltar que el paciente, al momento de la consulta al Hospital, negó molestias gastrointestinales en años anteriores. Al ingreso al Hospital el paciente portaba estudios hechos en otra institución, alrededor de 5 meses posteriores al inicio de los síntomas, entre los cuales se destacaron una ecografía abdominal sin alteraciones, un hemograma con anemia moderada y endoscopías alta y baja. El estudio histopatológico de la biopsia de duodeno reportó discreta atrofia vellositaria subtotal multifocal, con hiperplasia críptica, linfocitos intraepiteliales >30/enterocitos, moderado incremento de la celularidad de lámina propia (grado IIIa de la clasificación de MARSH). La biopsia de colon no tuvo resultados patológicos. Se investigaron los anticuerpos anti transglutaminasa IgA y péptido deaminado de gliadina IgG, con resultados positivos (22.9 UL/ml, VR: hasta 8 UI/ml y 20 UL/ml, VR: hasta 10 UI/ml respectivamente), mientras que los anticuerpos anti endomisio IgG, IgA y péptido deaminado de gliadina IgA resultaron negativos. Una tomografía computarizada (TC) de tórax, abdomen y pelvis con contraste no evidenció adenomegalias retroperitoneales, mesentéricas, inguinales ni pelvianas. Tanto el hígado como el bazo tenían tamaño conservado y no presentaban lesiones focales. Ante la persistencia de la sintomatología y el deterioro del paciente, 2 meses después se indicó una resonancia magnética, en donde se reconoció una lesión orgánica con aumento del número de válvulas conniventes a nivel de íleon, engrosamiento parietal circunferencial de 7 cm de extensión y 1.5 cm de espesor a nivel de asa de yeyuno, con signos de restricción de la difusión, sin realce significativo. Fue intervenido por abdomen agudo quirúrgico con una laparotomía exploradora más resección de intestino delgado por tumor en yeyuno, cuya muestra se envió a anatomía patológica. Aproximadamente un mes después de la cirugía, con los estudios anteriormente descritos, acudió a nuestra institución. En sangre periférica no se vieron alteraciones significativas y se repitieron los estudios de laboratorio, en los que se evidenció hipoalbuminemia 27 g/L (VN 35-52 g/L), beta-2 microglobulina de 3.33 mg/L y LDH 145 UI/L (VN 135-225 UI/L). El estudio histopatológico de la muestra de la lesión yeyunal, remitida en la cirugía descrita, describió sectores de pared de intestino delgado con áreas de mucosa preservada que exhibía aplanamiento vellositario completo e incremento de linfocitos intraepiteliales (MARSH 3c). Además, presencia de infiltrados linfoides densos que comprometían toda la submucosa del órgano y en forma laxa la muscular propia y serosa con patrón de crecimiento difuso y microfocos de necrosis. La celularidad se componía de células linfoides de tamaño mediano predominantes, con núcleos de cromatina granular abierta, algunos nucléolos visibles y escasos citoplasmas basófilos, además de numerosos linfocitos intersticiales. La inmunohistoquímica fue positiva para cCD3, CD2, CD7, granzime B y negativa para CD4, CD8, CD5 y CD56. El índice de proliferación (Ki67 nuclear) fue del 50%, con una presencia de reactividad muy dispersa para CD30. A finales del mismo mes, el estudio PET-TC con DFG puso en evidencia engrosamientos hipermetabólicos multifocales de asas intestinales delgadas en flanco derecho (SUV Max: 10.72), fosa ilíaca izquierda (SUV Max: 18.69) y a nivel de centro pelviano (SUV Max: 11.52), asociados a adenomegalias a nivel mesentérico hipermetabólicas (SUV Max; 10.94). No se identificaron adenomegalias hipermetabólicas retroperitoneales, ilíacas ni inguinales. Así mismo, no se observaron lesiones focales a nivel del hígado ni bazo. Luego de 15 días inició tratamiento con esquema CHOP, requiriendo hospitalización en el día +10 del primer ciclo por cuadro febril, asociado a intolerancia oral y dolor abdominal intermitente. Se planteó nutrición enteral por sonda nasoyeyunal. Sin embargo, en el día +15 presentó signos peritoneales asociados a dolor abdominal intenso, náuseas y vómitos. Fue evaluado por el servicio de Cirugía General, y se estableció el diagnóstico de perforación intestinal, por lo que fue nuevamente intervenido por abdomen agudo quirúrgico. Se le realizó una ileostomía por perforación del íleon terminal. El paciente falleció un día posterior a la cirugía, aproximadamente 1 año después del inicio de los síntomas.
Características histológicas e inmunohistoquímica de la masa yeyunal
A: Mucosa de epitelio intestinal con aplanamiento vellositario completo e incremento de linfocitos intraepiteliales.
B: Proliferación de células linfoides medianas y grandes, con núcleos de cromatina granular abierta, algunos nucleolos visibles y escasos citoplasmas basófilos.
Reactividad citoplasmática heterogénea para CD3.
Positividad para CD7 en membrana.
Negatividad para CD4, CD56, CD8 y CD20, con testigos internos positivos.
Intensa reactividad citoplasmática para granzime B.
Índice de proliferación (Ki67 nuclear) del 50% aproximadamente.
Enfermedad celíaca y linfoma asociado a enteropatía: una relación estrecha y peligrosa
El linfoma T asociado a enteropatía es un tipo de linfoma de células T periféricas raro, agresivo y de mal pronóstico, cuyo origen se encuentra fuertemente relacionado con la enfermedad celíaca, en la que el ambiente inflamatorio intestinal prolongado puede conducir, a través de un estrés genotóxico, a la transformación neoplásica de linfocitos T intraepiteliales. Representa menos del 5% de los linfomas GI y menos del 1% de los LNH, siendo considerado el subtipo de linfoma primario intestinal T más común en los países occidentales(7), con una incidencia mayor en el norte de Europa y una supervivencia a 2 años del 15-20%. Los factores de riesgo más frecuentemente asociados a este tipo de linfoma son: susceptibilidad para el desarrollo de enfermedad celíaca (genotipo HLA-DQ2 o DQ8), el sexo masculino y la edad avanzada(7), aunque la edad promedio al diagnóstico es de 50 años. Anteriormente se relacionaba la introducción temprana de una dieta rica en gluten en lactantes con una mayor incidencia de esta enfermedad, sin embargo, no hay estudios que muestren evidencia de esto, incluso en infantes con susceptibilidad genética potencial para el desarrollo de la enfermedad.
La clínica de presentación es variada y puede afectar desde el tracto gastrointestinal, predominantemente a nivel del íleon o yeyuno proximal (en un 90% de los casos como yeyunitis), con menor frecuencia el estómago (8%) o el colon (16%); hasta zonas extra-intestinales como ganglios linfáticos mesentéricos/intraabdominales (35%), ganglios linfáticos paraaórticos/ilíacos (11%) y ganglios inguinales/femorales (6%). Con mucha menor frecuencia puede afectar los pulmones, la piel, tejidos blandos y médula ósea(2). Los síntomas sistémicos B como fiebre sin causa evidente, diaforesis nocturna y pérdida de peso corporal superior al 10%, ocurren en menos del 30% de los casos de EATL.
La patogénesis de esta enfermedad no está bien establecida. Se conoce que puede desarrollarse a partir de una EC, de una ECR o de novo. El diagnóstico de EC siempre debe ser confirmado por biopsia, independientemente del estado serológico. Las características histológicas clásicas son: incremento de linfocitos intraepiteliales (>25 - 40 por cada 100 células epiteliales), hiperplasia de criptas y atrofia de vellosidades(16). Estas características no son específicas de la EC y pueden presentarse en otras patologías, como la enteropatía autoinmune, giardiasis, esprúe colágeno, tuberculosis intestinal, enteropatía por VIH, intolerancia a alimentos aparte del gluten, entre otras. Se han propuesto diferentes clasificaciones histopatológicas para la EC, siendo las más relevantes la clasificación de MARSH, modificada posteriormente por Oberhuber en 1999, y la clasificación de Corazza, publicada en el 2007, la cual considera sólo tres categorías. La principal causa de falta de respuesta a la dieta sin gluten y evolución a enfermedad celíaca refractaria es la ingestión continua y generalmente inadvertida de éste.
Es posible que la acumulación de mutaciones, como resultado de reordenamientos clonales en células ubicadas en un ambiente de estrés genotóxico y la inflamación crónica prolongada asociada al entorno rico en citoquinas, formen parte del proceso de linfomagénesis. Las mutaciones genómicas conducentes a la transformación maligna, la estimulación de la proliferación y la inhibición de la apoptosis de los linfocitos intestinales intraepiteliales (LIE) serían los determinantes del desarrollo del EATL.
La enfermedad celíaca se desarrolla a partir de la desviación de una respuesta inmune adaptativa cuando epitopes derivados de péptidos del gluten se unen firmemente a moléculas HLA DQ2/8 en células presentadoras de antígenos (CPA) constituyentes del sistema de vigilancia inmune en la lámina propia intestinal. El gluten contenido en algunos cereales es rico en gliadina y glutaminas -denominadas en conjunto, prolaminas- a partir de cuya digestión insuficiente por las enzimas del ribete en cepillo de las células epiteliales se pueden formar péptidos inmunogénicos potentes. Las prolaminas constituyen un sustrato apropiado para la enzima transglutaminasa tisular (tTG), que se expresa en forma constitucional en la lámina propia del intestino. Esta enzima tiene la capacidad de desaminar los residuos de glutamina presentes en el ácido glutámico, facilitando la unión a moléculas HLA DQ2/8. Se ha observado que la tTG ligada a epitopes del gluten puede ser reconocida como hapteno y estimular la producción de anticuerpos IgA, así como que los péptidos negativos unidos a la enzima pueden unirse a residuos de carga positiva de moléculas HLA DQ2/8 de las CPA. Esta unión determina la formación de complejos estables reconocibles por las células T CD4+, cuya diferenciación a fenotipo Th1 estimula la producción de interferón gamma (IFNg). Las células T CD4+ TCR αβ están presentes típicamente en la enfermedad celíaca, mientras que las células CD8 TCRαβ convencionales se encuentran notablemente expandidas y activadas, pero no parecen ser específicas a la exposición al gluten(11). En individuos sanos, estas células T CD8αβ convencionales expresan receptores inhibidores de células NK (CD94/NKGA)(9), mientras que en pacientes con enfermedad celíaca, los niveles elevados de IL-15 inducen en LIE la expresión de receptores activadores de células NK (NKG2C/NKG2D) y regulan positivamente la expresión de moléculas de clase I del sistema HLA en las células del epitelio intestinal, lo que promueve en los LIE CD8αβ innatos la secreción de moléculas (granzima, perforina) efectoras del daño citotóxico sobre los enterocitos(2,3). La expresión en superficie de NKG2D requiere de la unión a una proteína adaptadora, DAP 10. Cuando se une el ligando al receptor NKG2D, se fosforila un residuo de tirosina en la proteína DAP 10, fosforilación que activa tres vías posibles de citólisis: PLCg2, JNK y PI3K, promoviendo la fosforilación de proteínas quinasas activadas por mitógenos (MAPK)(7,9). Sería entonces la evolución fenotípica de los LIE a células de carácter citotóxico lo que conduce al daño epitelial independiente de TCR. El efecto citolítico potencial de los LIE CD8+TCRαβ se ve contrabalanceado en condiciones normales por un efecto inhibitorio de LIE TCRγδ. Este efecto antagonista está regulado por la transcripción del factor TGF-β que utiliza el factor de transcripción Smad3 como intermediario de la acción transcripcional. En pacientes con enfermedad celíaca activa, la producción aumentada de IL-15 inhibe la actividad transcripcional de Smad3, potenciando de este modo el daño epitelial. Además, al activar la vía de PI-3K aumenta la resistencia de las células T efectoras a la regulación ejercida por las células T reg (CD4+ FoxP3+), confiriendo una tolerancia alterada a los antígenos dietéticos y permitiendo la supervivencia de células T autorreactivas.
Los linfocitos intestinales intraepiteliales de tipo innato cCD3+ derivan de células inmaduras precursoras hematopoyéticas que migran al epitelio intestinal. Estos linfocitos muestran fenotípicamente las mismas características que los LIE aberrantes observados en ECR-II y EATL, lo que sugiere que constituirían las células de origen, tanto de ECR tipo II como de EATL(2). En humanos sanos, siguiendo a la exposición a IL-15, estos LIE se diferencian a células NK y células T en presencia de señales NOTCH1 y expresan CD103 en respuesta a TGF-β(2,3). En pacientes con ECR-II, los LIE cCD3+ aberrantes se caracterizan por la ausencia de expresión de los antígenos de superficie CD3, CD8, CD56 y CD4, mientras que son positivos para CD103 y CD3 citoplasmático (cCd3+). Además, carecen de capacidad para diferenciarse y no llegan a completar su desarrollo (desarrollo incompleto o desregulado), conservando características de células NK (marcador NKp46+)(7) y de células T (cCD3+). Estas células pueden presentar características genotípicas con reordenamientos en todos los loci del gen TCR, reordenamientos clonales con TCR no funcionales, reordenamientos de los genes TCRα, β, γ, δ o ausentes(3). No se sabe si estas características genotípicas surgen debido a la represión epigenética de los genes blanco de las proteínas NOTCH1 o como consecuencia de alteraciones genéticas (deleciones del gen BCL11B o del gen supresor de tumor SETD2)(3). El estrés genotóxico promueve que los LIE aberrantes adquieran y acumulen otras mutaciones genéticas(2) como en TNIP3 y TNFAIP3, reguladores negativos de la vía de señalización NF-kB, los cuales no ocupan un rol importante en la linfomagénesis del EATL, pero pueden crear sinergias con otras mutaciones, como las implicadas en la activación de la vía de señalización JAK1/STAT3. El hecho de que las células linfoides aberrantes expresen el marcador enterocítico NKp46 en presencia de IL-15, le confiere una citotoxicidad de tipo NK contra las células epiteliales, que puede resultar en lesiones mucosas únicas, múltiples o masas tumorales que terminan en la destrucción de los enterocitos, llevando a necrosis extensa, perforación intestinal y/o peritonitis(2). Además, la IL-15 se ve implicada en la regulación positiva de la proteína antiapoptótica Bcl-xl al activar la vía de señalización JAK3/STAT5, facilitando la supervivencia de los LIE aberrantes. Otras mutaciones menos frecuentes implicadas incluyen SOCS1, mutaciones de la vía MAPK y en genes de reparación del ADN como TP53. Los LIE aberrantes van adquiriendo nuevas mutaciones lo que les permite expandirse a expensas de los LIE policlonales normales(2). Así mismo, entre algunas alteraciones cromosómicas se destacan ganancias en cromosomas 1q, 5q35, 9q31 y pérdidas en 8p, 13q22, 18q22, entre otras, aunque ninguna parece ser específica para esta enfermedad(3). Se evidenció, además, el papel de los microARN como posibles genes supresores de tumores, implicados en el proceso de diferenciación, muerte celular programada y crecimiento celular de los LIE(2). Estos microARN se ven involucrados en vías de señalización como JAK/STAT. En los casos de EATL, muchos de estos microARN se pierden dentro de regiones con alteraciones cromosómicas, lo que se observa mediante la sobreexpresión de c-MYC(2).
En cuanto al tratamiento, no existen protocolos validados y estandarizados para EATL(7). Se combinan regímenes de quimioterapia y cirugía con resección de masas tumorales con alto riesgo de obstrucción y perforación debido al daño causado por la infiltración linfomatosa multifocal y a la desnutrición de los pacientes. La mayoría de datos se basan en estudios retrospectivos que comparan regímenes de quimioterapia basados en antraciclinas (CHOP), combinados o no con tratamiento quirúrgico. En un estudio multicéntrico tipo cohorte, realizado por P. Nijeboer et al(7), se comparó la respuesta al tratamiento y la sobrevida de un total de 61 pacientes con una media de edad al diagnóstico de 63 años. Estos pacientes fueron seleccionados de 20 hospitales en Países Bajos. En 31 pacientes (51%) se diagnosticó EATL sin antecedente de EC, en los 30 restantes EATL secundaria, de los cuales 19 (63%) fueron diagnosticados con ECR-II. Diferentes regímenes quimioterápicos fueron comparados durante 15 años (1999-2013), así como esquemas de monoterapia con quimioterapia o cirugía de resección y terapia combinada con ambos regímenes. El estudio evaluó características clínicas, de tratamiento, respuesta y sobrevida. Los regímenes terapéuticos incluyeron: resección quirúrgica sola, quimioterapia basada en antraciclinas en combinación con resección quirúrgica, quimioterapia basada en antraciclinas sola, resección con/sin quimioterapia seguida de trasplante de células progenitoras hematopoyéticas y tratamiento de soporte/paliativo solo. El tratamiento fue elegido para cada paciente de acuerdo a la edad y a su estado funcional. En cuanto a los regímenes de quimioterapia utilizados estos fueron: CHOP, CHOP + alemtuzumab, CHOEP, CHOP + bleomicina y vincristina, CHOP+MTX. La respuesta al tratamiento se evaluó como remisión completa (RC), enfermedad estable o enfermedad progresiva, según la revisión de criterios de respuesta para el linfoma. Los resultados fueron evaluados a los 3 meses de la finalización de la terapia elegida. En este estudio se puso en evidencia que el grupo de EATL secundaria tuvo peor pronóstico, hecho probablemente asociado con un estado de desnutrición previo. Los pacientes con un IPI bajo al diagnóstico mostraron un resultado más favorable. En este estudio la mediana de supervivencia general no fue significativamente mayor en el régimen combinado de cirugía/quimioterapia. Sin embargo, fue superior en comparación con la monoterapia. Los mejores resultados se obtuvieron en pacientes que recibieron resección quirúrgica seguida de quimioterapia sistémica, de modo que fue planteado como el régimen estándar de tratamiento.
Estos linfomas suelen expresar CD30(17,18), lo que los hace susceptibles al uso de brentuximab vedotin(17,18). Es por esto que el ensayo EATL-001(19) evaluó el uso de brentuximab combinado con CHP (ciclofosfamida, doxorrubicina y prednisona) en un total de 14 pacientes con una edad media de 54 años, incluidos entre 2018 y 2021. Los resultados obtenidos mostraron una respuesta general después de la inducción del 79% (11 de 14 pacientes), de los cuales 2 fallecieron por complicaciones asociadas al auto trasplante. Con una mediana de seguimiento de 2.1 años, no hubo recaída y la SLP y la SG a 2 años fueron del 63 y 68% respectivamente, concluyendo que el esquema BV-CHP fue bien tolerado e indujo tasas altas de respuesta, lo que permitió que los pacientes fueran trasplantados.
A la fecha, se han realizado diversos estudios enfocados en buscar tratamientos más efectivos. Entre 1994 y 1998, el Grupo de Linfoma de Escocia y Newcastle (SNLG) llevó a cabo un estudio sobre el linfoma de células T asociado a enteropatía (EATL), abarcando a una población de 7.6 millones de personas en Escocia y el norte de Inglaterra(20). El propósito de la investigación fue examinar las características clínicas y los resultados terapéuticos de esta enfermedad poco frecuente y de mal pronóstico. Se analizaron 54 casos de EATL, y a partir de 1998 se implementó un nuevo protocolo de quimioterapia intensiva (IVE/MTX) combinado con trasplante autólogo de células madre (ASCT) en 26 pacientes. Los hallazgos indicaron que este enfoque logró una SLP y una SG a cinco años del 52% y 60%, respectivamente, lo que representó una mejora notable en comparación con el tratamiento convencional basado en antraciclinas, cuya SLP y SG fueron de 3.4 y 7.1 meses. En conclusión, el régimen IVE/MTX-ASCT se considera una alternativa eficaz con mejores resultados y una toxicidad manejable, sugiriendo la necesidad de validarlo en estudios más amplios y multicéntricos.
En cuanto al auto trasplante en EATL, se considera actualmente una estrategia viable y prometedora. Un estudio retrospectivo realizado por el Grupo de Trabajo sobre Linfoma (Lymphoma Working Party) del Grupo Europeo de Trasplante de Sangre y Médula Ósea tuvo como objetivo principal estudiar el resultado del trasplante autólogo de médula ósea como estrategia de consolidación o rescate para EATL(21). Se eligieron pacientes mayores de 18 años que habían recibido auto trasplante entre 2000 y 2010 para EATL, con un total de 44 pacientes en el análisis final. BEAM (carmustina, etopósido, citarabina y melfalán)(21) se utilizó como régimen de acondicionamiento en 36 pacientes. Veinticuatro de éstos se encontraban en primera RC o RP al momento del trasplante. Se realizó un seguimiento medio de 46 meses. Tres de los pacientes incluidos en el estudio murieron prematuramente por razones relacionadas al trasplante. La SLP y la SG fueron del 54% y del 59% a los cuatro años, respectivamente, con mejor SG en los pacientes trasplantados en primera RC o RP en comparación con un estado de la enfermedad más avanzado. Además, los pacientes con antecedentes de enfermedad celíaca tuvieron una SLP y SG superior (70% vs. 35% y 70% vs. 45%). Como conclusión, este estudio rescató que el trasplante autólogo de células madre es factible en pacientes seleccionados con EATL y puede producir un control duradero de la enfermedad y debe considerarse en pacientes con EATL que responden a la terapia inicial(20).
En general, el pronóstico para estos pacientes sigue siendo pobre a pesar del tratamiento intensivo, al ser un linfoma de comportamiento agresivo, de baja incidencia y de diagnóstico complejo. El hecho de que la mayoría de estos pacientes presenten una edad avanzada al diagnóstico, con altas tasas de malnutrición debido a un estado comórbido previo como la EC, no ha permitido el desarrollo de nuevos estudios prospectivos y controlados que demuestren resultados favorables con los regímenes de tratamiento. El caso de este paciente en particular, tuvo un diagnóstico de EC tardío, por lo que es probable que esta condición haya aumentado el riesgo para el desarrollo de la complicación maligna.
Principales diferencias entre EATL y ECR
|
|
Histopatología |
Inmunohistoquímica |
|
Enfermedad celíaca |
Aumento de LIE (fenotipo normal), hiperplasia de criptas, atrofia vellositaria |
sCD3+, CD8+, reordenamiento policlonal del TCR |
|
Enfermedad celíaca refractaria tipo I |
Atrofia de vellosidades moderada/grave <50% |
sCD3+, CD8+, TCR αβ+/γδ+, reordenamiento policlonal del TCR |
|
Enfermedad celíaca refractaria tipo II |
Gran atrofia de vellosidades moderada/grave >50%, infiltrado intraepitelial de linfocitos atípicos |
cCD3+, sCD3-, CD30-, CD8-, TCR αβ+/γδ+, reordenamiento oligo/monoclonal del TCR |
|
Linfoma asociado a enteropatía |
Células medianas, núcleo prominente |
CD3+, CD7+, CD30+, CD8-, CD56- |
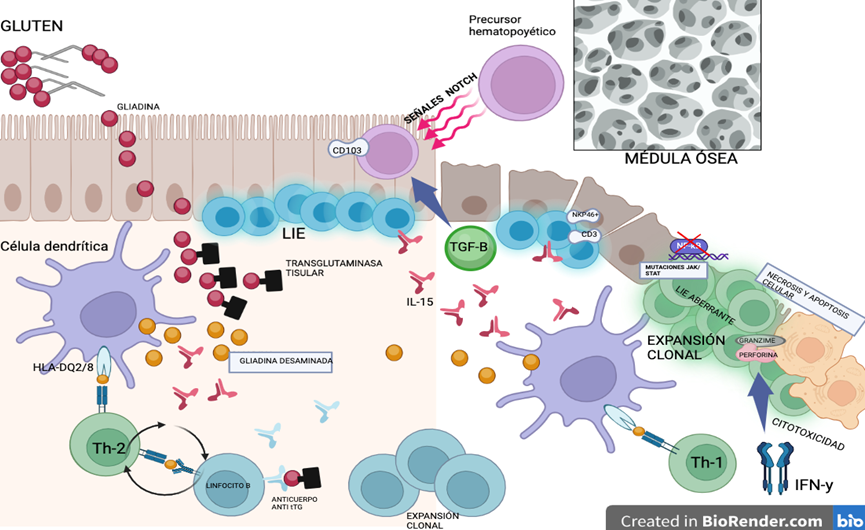
Fisiopatología de ECR-2 – EATL
En individuos sanos, la célula progenitora hematopoyética precursora de los linfocitos intestinales intraepiteliales, migra desde la médula ósea hasta el epitelio intestinal, donde se diferencia a través de señales NOTCH1 y expresan CD103, NK (CD94/NKGA) mediado por la regulación ejercida por la vía de señalización TGF-b. La exposición crónica e inadvertida al gluten es la principal causa relacionada a la enfermedad celíaca refractaria (ECR), considerándose a la ECR-II como un estado prelinfomatoso/linfoma silente. La gliadina, principal compuesto del gluten asociado al desarrollo de la EC, se une a la enzima transglutaminasa tisular, y ésta la desamina hasta péptidos, los cuales son reconocidos por las células dendríticas de la lámina propia del epitelio intestinal. Este reconocimiento antigénico estimularía la producción de IL-15 por las células epiteliales y dendríticas. Éstas últimas presentan los péptidos de gliadina desaminada a las células T, por medio de HLA-D2/DQ8. Los linfocitos T CD4+ activados producen citoquinas proinflamatorias como IFN-γ, las cuales, a su vez, activan la respuesta humoral por parte de los linfocitos B, estimulando la expansión clonal de éstos y activando la producción de autoanticuerpos específicos de tTG y antigliadina, lo que genera un círculo de amplificación y aumenta la activación de más células T. La IL-15 tiene un rol importante en la fisiopatología del EATL, ya que inactiva la diferenciación de los LIE e induce la expresión de NKp46+ (marcador NK). Estos LIE, con expresión de células T (cCD3+) y NK, empiezan una expansión clonal y pierden su capacidad apoptótica al adquirir mutaciones somáticas en vía JAK/STAT y en las vías de señalización NF-Kb.
Conclusiones
El linfoma T asociado a enteropatía es un linfoma agresivo y de mal pronóstico. Los pacientes que desarrollan la EC habitualmente son portadores de antígenos leucocitarios HLA DQ2/DQ8 y, en casos más raros, DQ7.5. Se tiene conocimiento de que un gran porcentaje de pacientes celíacos presentan un diagnóstico tardío, lo que contribuye a una exposición prolongada e inadvertida al gluten. Esto conllevaría a un estado de refractariedad (ECR) que, según la presencia o ausencia de características aberrantes en la célula de origen (linfocito intestinal intraepitelial), puede dividirse en ECR tipo I o II, respectivamente. Este último es considerado como un linfoma silente, y la progresión a EATL es muy frecuente. Se han estudiado diferentes mecanismos implicados en la fisiopatología de esta complicación maligna, y actualmente se postula que los linfocitos intraepiteliales aberrantes y la IL-15 constituirían los actores principales de la linfomagénesis.
Casi la totalidad de los pacientes que desarrollan este linfoma de comportamiento agresivo son, en su mayoría, pacientes de edad avanzada y tienen un estado de desnutrición previo asociado a la EC, lo que no ha permitido desarrollar nuevos esquemas de tratamiento, y los reportes en la literatura hasta el momento se centran en regímenes combinados que implican resección quirúrgica más quimioterapia sistémica. Lamentablemente, la mayoría de los pacientes no logran la remisión completa y fallecen durante el tratamiento por complicaciones relacionadas con la enfermedad.
Bibliografía
1. Di Sabatino A, Biagi F, Gobbi P et al, How I treat enteropathy-associated T-cell lymphoma. Blood. 2012;119: 2458-68. https://doi.org/10.1182/blood-2011-10-385559.
2. Azzam S, Goa P, Vandenberghe E et al. Update on the Pathogenesis of Enteropathy-Associated T-Cell Lymphoma. Diagnostics. 2023; 13: 2629. https://doi.org/10.3390/diagnostics13162629.
3. Chander U, Leeman-Neil R, Bhagat G. Pathogenesis of Enteropathy-Associated T Cell Lymphoma. Current Hematologic Malignancy Reports. 2018; 13: 308-317. https://doi.org/10.1007/s11899-018-0459-5.
4. De Leval L, Bisig B. What is new in the classification of peripheral T cell lymphomas? Pathologie. 2023; 44: 128-135. https://doi.org/10.1007/s00292-023-01260-y.
5. Busto V, Crespo L, Rodríguez-Gandía M et al. Linfoma T asociado a enteropatía: un reto diagnóstico. Gastroenterol Hepatol. 2011; 34: 686-689. https://doi:10.1016/j.gastrohep-2011.08.004.
6. Al Somali Z, Hamadani M, Kharfan-Dabaja M et al. Enteropathpy-Associated T cell Lymphoma. Curr Hematol Malig Rep. 2021; 16:140-147. https://doi.org/10.1007/s11899-021-00634-4.
7. Nijeboer P, R. de Baaij L, Visser O et al. Treatment response in enteropathy associated T-cell lymphoma; survival in a large multicenter cohort. Am J Hematol. 2015; 90: 493-8. https://doi.org/10.1002/ajh.23992.
8. Meresse B, Ripoche J, Heyman M et al. Celiac disease: from oral tolerance to intestinal inflammation, autoimmunity and lymphomagenesis. Mucosal Immunol. 2009; 2:8-23. https://doi: 10.1038/mi.2008.75.
9. Ma H, Qiu Y, Yang H. Intestinal intraepithelial lymphocytes: Maintainers of intestinal immune tolerance and regulators of intestinal immunity. J Leukoc Biol. 2021; 109: 339-347. https:// doi: 10.1002/JLB.3RU0220-111.
10. McDonald B, Jabri B, Bendelac A. Diverse developmental pathways of intestinal intraepithelial lymphocytes. Nat Rev Immunol. 2018; 18:514-525. https://doi.org/10.1038/s41577-018-0013-7.
11. Zhang J, Wang Y, Wang X et al. Type I enteropathy-associated T-cell lymphoma in the colon of a 29-year-old patient and a brief literature review. Onco Targets Ther. 2016; 22:863-868. https://doi: 10.2147/OTT.S96745.
12. Delabie J, Holte H, Vose J et al. Enteropathy-associated T-cell lymphoma: clinical and histological findings from the International Peripheral T-Cell Lymphoma Project. Blood. 2011; 118:148–155. https://doi.org/10.1182/blood-2011-02-335216.
13. Scarmozzino F, Pizzi M, Pelizzaro F et al. Refractory celiac disease and its mimickers: a review on pathogenesis, clinical-pathological features and therapeutic challenges. Front Oncol. 2023; 13:1273305. https://doi.org/10.3389/fonc.2023.1273305.
14. Vaquero L, Alvarado M, Arias L et al, Linfoma intestinal de células T asociado a enteropatía y sin relación con enfermedad celíaca. Gastroenterol Hepatol. 2012; 35:17-21. https://doi.org/10.1016/j.gastrohep.2011.11.003.
15. Moscoso F, Quera R. Update on celiac disease. Rev. Méd. Chile. 2016; 144:2, https://doi.org/10.4067/S0034-98872016000200010.
16. Freedman A, Aster J. (2022). Clinical manifestations. Pathologic features, and diagnosis of enteropathy-associated T cell lymphoma. Lister A, Rosmarin A (Ed.), UpToDate.
17. Nijeboer P, Malamut G, Mulder C et al. Enteropathy-Associated T-Cell Lymphoma: Improving Treatment Strategies. Digestive Diseases. 2015; 33:231-235. https://doi.org/10.1159/000369542.
18. Khalaf W, Caldwell M, Reddy N. Brentuximab in the Treatment of CD30-Positive Enteropathy-Associated T-Cell Lymphoma. Journal of the National Comprehensive Cancer Network. 2013; 11:137-140.
19. Sibon D, Khater S, Bruneau J et al. The Eatl-001 Trial: Results of a Phase 2 Study of Brentuximab Vedotin and CHP Followed By Consolidation with High-Dose Therapy - Autologous Stem-Cell Transplantation (HDT-ASCT) in the Frontline Treatment of Patients with Enteropathy-Associated T-Cell Lymphoma. Blood. 2021; 138:136. https://doi.org/10.1182/blood-2021-153709.
20. Sieniawski M, Angamuthu N, Boyd K et al. Evaluation of enteropathy-associated T-cell lymphoma comparing standard therapies with a novel regimen including autologous stem cell transplantation. Blood. 2010;115(18):3664-3670. https://doi.org/10.1182/blood-2009-07-231324.
21. Jantunen E, Boumendil A, Finel H et al. Autologous Stem Cell Transplantation (ASCT) for Enteropathy-Associated T-Cell Lymphoma (EATL): Final Analysis of a Retrospective Study On the Behalf of Lymphoma Working Party (LWP) of the European Group for Blood and Marrow Transplantation (EBMT). Blood. 2012; 120:3105. https://doi.org/10.1182/blood.V120.21.3105.3105.