Linfoma de Burkitt con infiltración del sistema nervioso central asociado al VIH. Un caso de respuesta al tratamiento.
Burkitt lymphoma with central nervous system infiltration associated with HIV. A case of treatment response.
Rodríguez V1*; Lozano C2; Rodríguez J3,4; Correa A5
1Servicio de Hematología, Hospital Teodoro Maldonado Carbo, Guayaquil, Ecuador.
2Servicio de Oncología, Hospital Teodoro Maldonado Carbo, Guayaquil, Ecuador.
3Servicio de Neurocirugía, Hospital de Especialidades Guayaquil. Guayaquil, Ecuador.
4 Facultad de Ciencias Médicas.
5 Hospital Teodoro Maldonado Carbo. Internado de Medicina.
Venus Rodríguez 0000-0002-8069-0501
Carlos Lozano 0000-0001-7537-4339
José Rodriguez 0000-0002-0148-6773
Amanda Correa 0009-0007-4307-0729
Palabras claves: linfoma de Burkitt,
VIH,
sistema nervioso central,
quimioterapia,
citometría de flujo.
Keywords: Burkitt lymphoma,
HIV,
central nervous system,
chemotherapy,
flow cytometry.
Resumen
El linfoma de Burkitt (LB) es una forma muy agresiva de neoplasia de células B que representa alrededor del 1-5% de todos los linfomas no Hodgkin. La Organización Mundial de la Salud clasifica el LB en tres grupos clínicos: endémico, esporádico y relacionado con inmunodeficiencias. Los regímenes de quimioterapia de alta intensidad han mejorado la supervivencia global de los pacientes con LB y, por ello, las recomendaciones terapéuticas actuales ofrecidas por la National Comprehensive Cancer Network incluyen regímenes multifarmacológicos con profilaxis del SNC. Se recomiendan pruebas inmunohistoquímicas y estudios citogenéticos que desempeñan un papel importante en el diagnóstico y el tratamiento del LB. El caso presentado pretende describir el manejo de un paciente diagnosticado de LB asociado a VIH con afectación del sistema nervioso. Como pruebas diagnósticas se realizaron biopsias tisulares de las masas mesentéricas y de la región maxilar derecha, pruebas de laboratorio, TC, aspiración y biopsia de médula ósea y análisis de líquido cefalorraquídeo. Se utilizaron 6 ciclos del régimen de quimioterapia R-hiper-CVAD, junto con terapia antirretroviral de alta actividad y quimioterapia intratecal, alcanzando la remisión completa.
Summary
Burkitt lymphoma (BL) is a very aggressive form of B-cells neoplasm that accounts for about 1%-5% of all non-Hodgkin lymphomas. The World Health Organization classifies BL into three clinical groups: endemic, sporadic and immunodeficiency related. High-intensity chemotherapy regimens have improved the overall survival of BL patients, and thus, current therapeutic recommendations offered by the National Comprehensive Cancer Network include multi-drug regimens with CNS prophylaxis. Immunohistochemistry tests and cytogenetic studies that play an important role in the diagnosis and treatment of BL are recommended. The presented case aims to describe the management of a patient diagnosed with HIV-associated BL with nervous system involvement. Tissue biopsies of the mesenteric and right maxillary region masses, laboratory tests, CT scans, bone marrow aspiration and biopsy, and cerebrospinal fluid analysis were performed as diagnostic tools. 6 cycles of R-hyper-CVAD chemotherapy regimen were used, along with high-activity antiretroviral therapy and intrathecal chemotherapy, reaching complete remission.
Introducción
El linfoma de Burkitt (LB) es una forma muy agresiva de neoplasia de células B no Hodgkin, identificada y descrita en el siglo pasado por Denis Burkitt en África. Desde entonces, también se ha reconocido fuera de las zonas endémicas de malaria. El LB afecta con frecuencia a niños africanos, así como a pacientes con inmunodeficiencia subyacente(1,2). El LB representa aproximadamente entre el 1% y 5% de todos los linfomas no Hodgkin en adultos. El LB representa el 40% de los linfomas asociados a HIV(3,6,11).
La Organización Mundial de la Salud (WHO por sus siglas en inglés) clasifica el LB en tres grupos clínicos: endémico, esporádico y relacionado con la inmunodeficiencia. La forma endémica está relacionada con la malaria y el virus de Epstein-Barr (EBV). La enfermedad suele estar asociada al virus de la inmunodeficiencia humana (VIH) y, a nivel molecular, se relaciona con translocaciones cromosómicas que provocan la sobreexpresión del oncogén c-MYC. En la quinta edición WHO, se postula que es mejor definirlos por sus características moleculares que por las geográficas o epidemiológicas. Se propone la distinción en dos subtipos: EBV positivos y EBV negativos para reflejar diferentes mecanismos de patogénesis (accionados por el virus o por mutaciones)(1-3,11).
El LB se caracteriza por la presencia de la translocación t(8;14) que acaba sobreexpresando el c-MYC, favoreciendo la proliferación celular descontrolada y el rápido crecimiento tumoral. En los últimos años se han identificado mutaciones adicionales, como las del gen supresor tumoral ID3 y el factor de transcripción TCF3(4,5).
El diagnóstico se realiza mediante la confirmación patológica del tejido de un nódulo o masa sospechosa. La biopsia por aspiración con aguja fina no proporciona una muestra de tejido suficiente para el diagnóstico; por lo tanto, se prefiere la biopsia por escisión. Además, debe realizarse una aspiración y biopsia de médula ósea, así como un estudio del líquido cefalorraquídeo (LCR) para valorar su posible afectación. Inicialmente, se realizan pruebas de laboratorio que incluyen hemograma completo, velocidad de eritrosedimentación (VSG), panel metabólico completo, tiempo de protrombina (TP), tiempo parcial de trombina (TPT), lactato deshidrogenasa sérica, ácido úrico, serología de la hepatitis B, prueba de embarazo en el caso de las mujeres y estado serológico del VIH. Posteriormente, deben realizarse estudios de imagen como escáneres corporales completos. También se sugiere la realización de PET/TC, pero no debe retrasar el tratamiento(3).
La inmunohistoquímica y la citogenética desempeñan un papel importante en el diagnóstico y el tratamiento del linfoma de Burkitt. Las células B malignas expresan IgM de superficie y marcadores característicos de células B, como CD19, CD20, CD79a y PAX5. También son positivos para los marcadores del centro germinal, CD10 y BCL-6, pero negativos para BCL-2. Las células neoplásicas no expresan marcadores de células T y no expresan marcadores inmaduros TdT o CD34. Por otra parte, el rápido recambio celular reflejado por la elevada positividad de Ki-67 es característico y útil para el diagnóstico. El grupo ICC (International Consensus Classification of Mature Lymphoid Neoplasms) separa del grupo Burkitt el linfoma de células precursoras TDT + con R MYC, y lo coloca dentro de las neoplasias de células precursoras: linfoma/leucemia de células B precursoras con R-MYC. En la cuarta edición WHO figuraba como entidad provisional el “linfoma símil-Burkitt con aberración del 11q”, llamado así por su semejanza clínica, morfológica e inmunofenotípica con el LB. Posteriormente ha sido demostrado que estos linfomas tienen mutaciones asociadas a los LDCGB sin las típicas mutaciones del linfoma Burkitt. Debido a estos estudios moleculares, ha sido separada del LB, siendo reconocida para el grupo ICC como entidad provisional bajo el nombre de “linfoma de células grandes B con aberración del 11q” y en la quinta edición WHO como “linfoma de células B de alto grado con aberración del 11q”(2,3,11).
Se están utilizando regímenes estándar e intensivos con resultados alentadores en pacientes con linfoma difuso de células B grandes, linfoma de Burkitt, linfoma de Hodgkin y linfoma primario del sistema nervioso central(2,3,9). Los regímenes de quimioterapia de alta intensidad han mejorado significativamente la supervivencia global de los pacientes con linfoma de Burkitt y, por ello, las recomendaciones terapéuticas actuales ofrecidas por la National Comprehensive Cancer Network incluyen regímenes multi farmacológicos con profilaxis del SNC: R-hyper-CVAD, CODOX-M/IVAC con o sin rituximab, y EPOCH ajustado a la dosis con rituximab. En los países desarrollados, la tasa global de curación del LB esporádico es cercana al 90% en la población pediátrica y de adultos jóvenes(3,7,8,10,11).
Desde la llegada de la terapia antirretroviral combinada, los resultados del tratamiento de los pacientes con linfoma relacionado con el VIH han mejorado, siendo como los del LB esporádico.
Caso clínico
Paciente masculino de 27 años, con antecedentes de infección por VIH diagnosticado en 2016, sin tratamiento hasta el ingreso, presentaba carga viral >240000 copias y CD4 >600. Refería cuadro clínico de 4 meses de evolución caracterizado por masa maxilar derecha en crecimiento, junto con pérdida de peso y sudores nocturnos (Figuras 1-3).
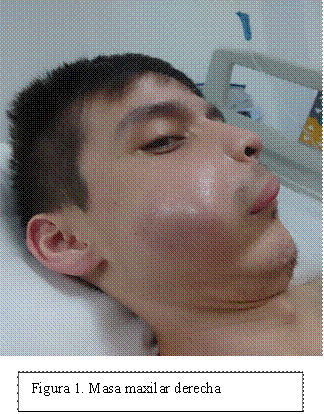
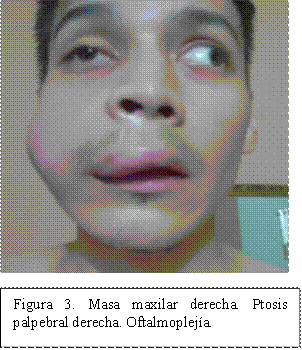

Al examen físico presentaba una masa de consistencia dura y fija en la región maxilar derecha que se extendía a la región malar, ptosis palpebral ipsilateral, compromiso de la cavidad oral con deformación de la mucosa del maxilar superior derecho, y a nivel abdominal presentaba dolor generalizado tipo cólico de intensidad moderada, que fue progresando y se localizó en fosa ilíaca derecha.
Se realizó TAC de área maxilofacial, observando en la hemicara derecha una masa de densidad de partes blandas en la región nasolabial, labio superior y que se extendía hacia la cavidad oral, de aproximadamente 9 x 6 x 5 cm, con afectación del reborde alveolar superior, paladar óseo, suelo del seno maxilar y pterigoideo ipsilateral. Hipertrofia de cornetes nasales inferiores.
En la RMN de senos paranasales la topografía del hemimaxilar superior derecho mostraba una lesión tumoral expansiva de baja señal en T1 a señal intermedia en T2-Flair que se desprendía de la región gingival vestibular y palatina de las encías 14 a 11 con dimensiones aproximadas de 4 cm de largo a 3.8 cm transversales, con cambios en las trabéculas alveolares y aumento del espacio del ligamento periodontal con extensión hacia la base del seno maxilar ipsilateral con infiltración y erosión (Figura 4-6).
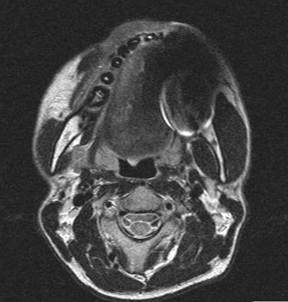
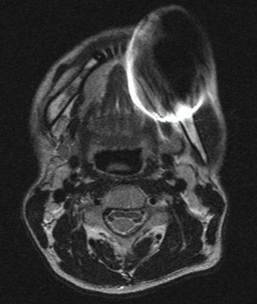
 |
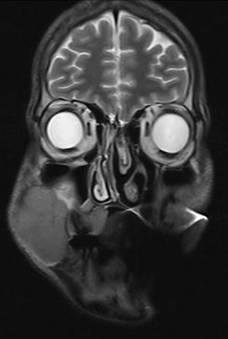
RMN cerebro y estructuras vasculares intracraneales y de cuello sin alteraciones.
TAC pelvis y abdomen, hígado de tamaño aumentado, bordes regulares, densidad homogénea. Asas intestinales distendidas de paredes gruesa con líquido en su interior.
TAC tórax, sin adenopatías.
Examen de laboratorio: hematocrito 34,3%, hemoglobina 11,1 g/dL, volumen corpuscular medio 76,4 fL, leucocitos 4,39 K/µL, neutrófilos 2,26 K/µL, plaquetas 529000 /µl, tiempo de protrombina 12,1 seg., INR: 1,01, fibrinógeno 387,83 mg/dl, TTP 26,4 seg., glucosa 79,90 mg/dl, cloro 103 mmol/L, urea 8,20 mg/dl, creatinina 0,52 mg/dl. Carga viral del VIH 2.760 copias.
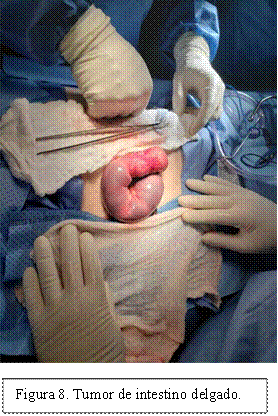
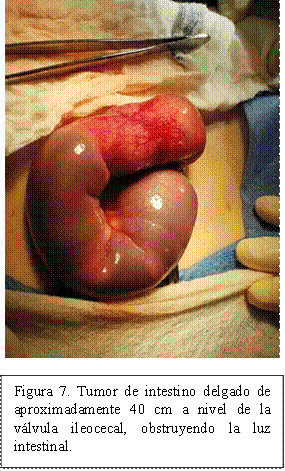
Se tomó biopsia de lesión maxilar y medula ósea para arribar al diagnóstico. Durante la evolución el paciente presentó dolor abdominal progresivo, por lo que tuvo que ser intervenido quirúrgicamente de urgencia, realizándose una apendicectomía con biopsia de ganglio linfático mesentérico, encontrando como hallazgos quirúrgicos la presencia de abundantes ganglios linfáticos mesentéricos, colónicos e intestinales, y una masa de 40 cm a nivel de la válvula ileocecal obstruyendo la luz intestinal (Figuras 7, 8).
 |
 |
Biopsia de médula ósea, libre de infiltración neoplásica.
Biopsia de masa de la región maxilar derecha informa de linfoma no Hodgkin de células grandes de tipo Burkitt. CD5 y ciclina D1 negativos; CD10, BCL-2, BCL-6, CD20 y Ki-67 positivos.
Biopsia de ganglio linfático mesentérico, diagnóstico: hallazgos histológicos compatibles con linfoma no Hodgkin difuso, inmunofenotipo B de alto grado: CD79a, CD19 positivo. Estudios inmunohistoquímicos: 1) CD19: positivo focal 5%. 2) CD79a: positivo 100%. 3) BCL-2: positivo focal 2%. 4) BCL-6: negativo. 5) Ciclina D1: negativa. 6) CD3: positivo 90%. 7) CD5: positivo 5%. 8) CD10: positivo 90%. 9) Ki-67: 100% (alto).
Citometría de flujo de líquido cefalorraquídeo (LCR). Se estudiaron los siguientes marcadores lambda, CD8, kappa, CD56, CD4, CD19, CD3, CD14, CD38, CD45. En la adquisición de 40.225 eventos totales, se detectaron células B neoplásicas, correspondientes al 11,91% del total de células viables evaluadas. Los parámetros de dispersión de luz (FSC/SSC) muestran células de gran tamaño y complejidad interna intermedia. Expresa CD45+, CD19+, CD20 débil, kappa+ débil; y negativo a CD3, CD14, lambda. Conclusiones: infiltración meningoencefálica del LCR por 11,91% de células B maduras con fenotipo patológico.
Por lo tanto, se realizó diagnóstico de linfoma de Burkitt, estadío EIVB, se inició rápidamente tratamiento con el esquema R-hyper-CVAD y quimioterapia intratecal, asociado a terapia antirretroviral. El paciente recibió un total de seis ciclos de junio de 2020 a marzo de 2021 con buena tolerancia, logrando remisión metabólica completa, desaparición de la masa maxilar, de la ptosis palpebral y región abdominal con estudio de líquido cefalorraquídeo de control sin evidencia de infiltración meningoencefálica por células B patológicas y carga viral de VIH < 40 copias (Figura 9 y 10).
 |
Discusión
El linfoma de Burkitt es poco frecuente y representa aproximadamente el 1-5%. La infrecuencia de estos casos es el motivo de la presentación de este trabajo, debido a la importancia del diagnóstico y tratamiento oportunos por el pequeño número de casos(10,11).
En cuanto a las manifestaciones clínicas del LB relacionado con inmunodeficiencias, la mandíbula, el mediastino, los testículos, la piel, la glándula tiroides y la mama no se ven afectados con frecuencia. Por otro lado, el LB endémico se presenta característicamente con una gran lesión de la mandíbula, hinchazón periorbitaria o afectación genitourinaria; en estos casos, la afectación de la mandíbula se observa predominantemente en niños. En los pacientes infectados por el VIH, el 80% de los casos de LNH presentan una enfermedad sistémica avanzada, correlacionada con niveles elevados de lactato deshidrogenasa. Existe una tendencia a la afectación extraganglionar del linfoma, como ocurre con otros linfomas relacionados con la inmunosupresión, debido a que se trata de un linfoma periférico de células B con una tasa de proliferación extremadamente alta. Los sitios frecuentes de afectación incluyen el SNC, el tracto gastrointestinal, el hígado y la médula ósea(3,10-14).
En nuestro caso, el paciente presentaba una masa en la región maxilar superior derecha, adenopatía mesentérica, una masa en el duodeno e infiltración del sistema nervioso central.
El tratamiento se estratifica en función de la edad y el estadío clínico del paciente y consiste en una quimioterapia combinada intensa, junto con profilaxis del SNC, que debe iniciarse lo antes posible tras el diagnóstico. Los regímenes de quimioterapia estándar, con ciclofosfamida, doxorrubicina, vincristina y prednisona (CHOP) son inadecuados para tratar el linfoma de Burkitt en adultos. Las recomendaciones actuales incluyen regímenes multifarmacológicos con profilaxis del SNC, como R-hyper-CVAD, R-CODOX-M / IVAC, R-DA-EPOCH. El metotrexato intratecal está indicado cuando hay evidencia de afectación cerebral y de la médula espinal(3,4,6,8,10,15). En un estudio multicéntrico de terapia adaptada al riesgo con R-DA-EPOCH en adultos con linfoma de Burkitt no tratado, los pacientes con afectación del LCR tuvieron mayor riesgo de fracaso del tratamiento. En pacientes con características de alto riesgo, como afectación del LCR, se debería estudiar la adición de agentes dirigidos con penetración en el SNC(16). En nuestro caso, elegimos el régimen de quimioterapia R-hyper-CVAD, ya que la combinación de rituximab con terapia antirretroviral diaria en linfomas agresivos asociados al VIH aumenta la supervivencia libre de eventos a largo plazo(6,8,15).
Se están investigando nuevos anticuerpos monoclonales: ofatumumab y obinutuzumab (anti-CD20), blinatumomab (anti-CD19) e inotuzumab (anti-CD22), así como fármacos experimentales, como inhibidores de la histona acetilasa (rapamicina, ácido valproico, tubacina), inhibidores de mTOR (temsirolimus), agentes anti-PD-1 y terapias que inhiben el oncogén MYC(3).
Conclusiones
En nuestro caso se evidenció una respuesta favorable al tratamiento oportuno realizado, con mejoría de su cuadro clínico, mejorando su calidad de vida.
****El paciente fue informado y dio su consentimiento para la divulgación clínica de su caso, así como para el uso de las fotos asociadas al mismo, arriba descritas.
Bibliografía
1. Fang H, Wang W, Medeiros LJ. Burkitt lymphoma. Hum Pathol. 2024 Dec 9:105703. doi: 10.1016/j.humpath.2024.105703.
2. Casulo C, Friedberg JW. Linfoma de Burkitt: un linfoma raro pero difícil. Best Pract Res Clin Haematol. 2018;31(3):279-84.
3. Graham BS, Lynch DT. Linfoma de Burkitt. StatPearls. Treasure Island (FL)2021.
4. Cabrera M. Protocolo clínico Linfoma de Burkitt. 2019:30.
5. Dunleavy K, Little RF, Wilson WH. Actualización sobre el linfoma de Burkitt. Hematol Oncol Clin North Am. 2016;30(6):1333-43.
6. Kalisz K, Alessandrino F, Beck R, Smith D, Kikano E, Ramaiya NH et al. An update on Burkitt lymphoma: a review of pathogenesis and multimodality imaging assessment of disease presentation, treatment response, and recurrence Insights Imaging. 2019;10(1):56.
7. Atallah-Yunes SA, Murphy DJ, Noy A. HIV-associated Burkitt lymphoma. Lancet Haematol. 2020;7(8):e594-e600.
8. Gopal S, Gross TG. How I treat Burkitt lymphoma in children, adolescents, and young adults in sub-Saharan Africa. Blood. 2018 Jul 19;132(3):254-263. doi: 10.1182/blood-2018-04-844472.
9. Hunter NB, Vogt S, Ambinder RF. Tratamiento de los linfomas asociados al VIH: The Latest Approaches for Optimizing Outcomes. Oncología (Williston Park). 2017;31(12):872-7, 84.
10. Sapkota S, Shaikh H. Non-Hodgkin Lymphoma. 2023 Feb 24. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; 2024 Jan–. PMID: 32644754.
11. Sociedad Argentina de Hematología. Guías de diagnóstico y tratamiento: edición 2023/compilación de Juan Dupont. -1a ed revisada. -Ciudad Autónoma de Buenos Aires: SAH, 2023.
12. Grogg KL, Miller RF, Dogan A. HIV infection and lymphoma. J Clin Pathol. 2007;60(12):1365-72.
13. Kuo YS, Wu YH, Sun A, Chiang CP. Burkitt's lymphoma of the mandible. J Dent Sci. 2017 Dec;12(4):421-423. doi: 10.1016/j.jds.2017.09.001.
14. Matsueda K, Fujita I, Horii J, Toyokawa T. Burkitt Lymphoma of the Duodenum. Intern Med. 2018 May 15;57(10):1493-1494. doi: 10.2169/internalmedicine.9896-17.
15. Saleh K, Michot JM, Camara-Clayette V, Vassetsky Y, Ribrag V. Burkitt and Burkitt-Like Lymphomas: a Systematic Review. Curr Oncol Rep. 2020;22(4):33
16. Roschewski M, Dunleavy K, Abramson JS, Powell BL, Link BK, Patel P, et al. Multicenter Study of Risk-Adapted Therapy With Dose-Adjusted EPOCH-R in Adults With Untreated Burkitt Lymphoma. J Clin Oncol. 2020;38: 2519–2529.