Disponibilidad y distribución de los recursos de hemostasia y trombosis en Argentina en el año 2022
Availability and distribution of hemostasis and thrombosis resources in Argentina in 2022
Chuliber F1,2, Gutiérrez A1,3, Kordys E1,4, Rossi E1,5, Romañano V1,6, Lobo E1,7, Horrach B1,6, Castoldi V1,8, Martí A1,6.
1 Grupo Promoción del Acceso a los Recursos en Hemostasia y Trombosis - Grupo CAHT.
2 Hospital Italiano de Buenos Aires. CABA, Argentina.
3 Hospital San Martín, La Plata. Buenos Aires, Argentina.
4 Hospital El Carmen. Mendoza, Argentina.
5 Laboratorio de Salud Pública. Tucumán, Argentina.
6 Hospital El Cruce Néstor Kirchner. Buenos Aires, Argentina.
7 Hospital San Bernardo. Salta, Argentina.
8 Hospital San Martín de Paraná. Entre Ríos, Argentina.
Chuliber https://orcid.org/0000-0001-8625-8624
Gutiérrez https://orcid.org/0009-0001-0220-2592
Kordys https://orcid.org/0009-0000-8689-3329
Rossi https://orcid.org/0009-0006-2916-3884
Romañano https://orcid.org/0009-0008-8134-6455
Lobo https://orcid.org/0009-0009-0940-6377
Horrach https://orcid.org/0009-0007-9398-5046
Castoldi https://orcid.org/0009-0000-4103-044X
Martí https://orcid.org/0009-0004-1438-062x
grupoaccesocaht@gmail.com; fernando.chuliber@hospitalitaliano.org.ar
Palabras clave: hemostasia,
trombosis,
recursos de salud.
Keywords: hemostasis,
thrombosis,
health resources.
Resumen
Introducción
En Argentina la información sobre la disponibilidad de los recursos en hemostasia y trombosis es muy escasa. El grupo Promoción del Acceso a los Recursos del grupo CAHT (Cooperativo Argentino de Hemostasia y Trombosis) desarrolló un amplio relevamiento de los recursos en Argentina para conocer el estado de situación de la especialidad.
Objetivos. Describir la disponibilidad de los recursos humanos y físicos (diagnósticos y terapéuticos) en hemostasia y trombosis en los centros asistenciales de Argentina en 2022 e identificar diferencias regionales y/o entre los sectores privado y público.
Materiales y métodos. Estudio de cohorte transversal. Se incluyeron centros asistenciales de la República Argentina: instituciones con internación, centros ambulatorios y laboratorios. Se obtuvieron datos respecto a la disponibilidad de recursos humanos, diagnósticos, y terapéuticos en hemostasia y trombosis, en algún momento del año 2022, mediante una encuesta a profesionales de la salud. En los recursos analíticos se definió disponibilidad cuando la prueba se realizaba en la institución o se derivaba la muestra/paciente.
Resultados. En el estudio se incluyeron 215 centros de 77 ciudades argentinas. El 85,5% de los centros contaban con internación.
La mediana de especialistas en hematología por institución fue de 3 (RIC 1-5). Se encontraron diferencias entre las medianas de las regiones: CABA-Ciudad Autónoma de Buenos Aires-(5), Centro/Cuyo (3,5) GBA/LP-Gran Buenos Aires/La Plata-(2), NOA-Noroeste Argentino-(2), NEA-Nordeste Argentino-(1) y SUR (1). El 27% de los centros contaban con 1 (“trabajo solitario”) o ningún especialista en hematología. El 59% de los centros reportaron que contaban con bioquímicos especialistas en hemostasia/hematología. La región con menor porcentaje de centros con especialistas fue GBA/LP (37%).
Se observó una alta disponibilidad de pruebas básicas de la coagulación. Por el contrario, en las estudios de mayor complejidad la disponibilidad fue subóptima y se detectaron marcadas asimetrías regionales (GBA/LP, NOA y NEA presentaron la menor proporción de centros con los recursos). Algunas pruebas, como la agregación plaquetaria o el anti-factor plaquetario 4 / heparina (anti-PF4/hep), no estuvieron disponibles en amplias áreas del país.
En la mayoría de los recursos terapéuticos se detectó una mayor disponibilidad en el sector privado.
Conclusiones. Detectamos una disponibilidad sub-óptima de los recursos físicos de alta complejidad y disparidades público-privada y regionales. Consideramos que el establecimiento de redes integradas es una estrategia que permitirá reducir las inequidades de acceso. Desde su lugar, las sociedades científicas podrían realizar valiosos aportes para obtener esa meta.
Abstract
Introduction. In Argentina, information regarding the availability of resources in hemostasis and thrombosis is very scarce. The “Grupo Promoción del Acceso” del grupo CAHT (Cooperativo Argentino de Hemostasia y trombosis) conducted an extensive survey of resources in Argentina to understand the current state of the specialty.
Objectives. To describe the availability of human and physical resources (diagnostic and therapeutic) in hemostasis and thrombosis in healthcare centers across Argentina in 2022 and to identify regional differences or disparities between the private and public sectors.
Materials and methods. Cross-sectional cohort study. Healthcare centers from the Argentine Republic were included: institutions with inpatient services, outpatient centers, and laboratories. Data regarding the availability of human, diagnostic, and therapeutic resources in hemostasis and thrombosis were obtained at some point during the year 2022 through surveys conducted among healthcare professionals. Availability in analytical resources was defined when the test was performed within the institution or when the sample/patient was referred elsewhere for testing.
Results. The study included 215 centers from 77 cities across Argentina. 85.5% of the centers had inpatient services.
The median number of hematologists per institution was 3 (IQR 1-5). Differences were found among the median numbers across regions: CABA-Ciudad Autónoma de Buenos Aires-(5), Centro/Cuyo (3.5), GBA/LP-Gran Buenos Aires/La Plata-(2), NOA-Noroeste Argentino-(2), NEA-Nordeste Argentino-(1), and SUR (1). 27% of the centers had 1 or no hematologist. 59% of the centers reported employing specialized biochemists in hemostasis/hematology. The region with the lowest percentage of centers with specialists was GBA/LP (37%).
There was a high availability of basic coagulation tests observed. Conversely, for more complex tests, availability was suboptimal and marked regional asymmetries were detected (GBA/LP, NOA, and NEA presented the lowest proportion of centers with resources). Some tests, such as platelet aggregation or anti-platelet factor 4/heparin, were not available in wide areas of the country.
In most therapeutic resources, greater availability was detected in the private sector.
Conclusions. We identified suboptimal availability of high-complexity physical resources and public-private and regional disparities. We believe that the establishment of integrated networks is a strategy that will help reduce access inequities. Scientific societies, from their position, can make valuable contributions to achieve this goal.
Introducción
En los últimos años, el acceso a los recursos de salud ha adquirido mayor relevancia, constituyendo un tema central de debate en los sistemas de salud en distintas partes del mundo(1,2). En Argentina, cuyo sistema de salud tiene altos niveles de fragmentación y segmentación, existen indicios respecto a la presencia de inequidades en el acceso a los recursos de salud. En el ejercicio asistencial cotidiano se observan las múltiples barreras de acceso y el desarrollo de disparidades. Además, ya existen publicaciones nacionales en este sentido(3). Sin embargo, en hematología la información publicada es muy escasa.
Acceso es un concepto complejo y multidimensional, y de difícil evaluación en estudios de investigación(4,5). Uno de sus aspectos es la disponibilidad, es decir, su oferta a la población, la presencia de los recursos para que puedan ser utilizados. Sin embargo, la mera disponibilidad no garantiza el acceso, ya que pueden interponerse múltiples barreras (geográficas, económicas, religiosas, culturales, entre otras). La presencia de barreras es otra de las dimensiones del acceso.
En marzo de 2022 se constituyó el grupo Promoción del Acceso a los Recursos en Hemostasia y Trombosis, integrado por socios y socias del grupo CAHT (Cooperativo Argentino de Hemostasia y Trombosis), de distintos lugares del país, especialistas en hematología y bioquímica con experiencia en hemostasia y trombosis. El proyecto surgió por la fuerte convicción del grupo CAHT respecto al lugar central que deben tener las problemáticas de acceso en las actividades de las sociedades científicas.
El primer paso del grupo fue el desarrollo de un relevamiento nacional de los recursos disponibles en hemostasia y trombosis que presentaremos a continuación. Los objetivos del estudio fueron:
- Describir la disponibilidad de los recursos humanos y físicos (diagnósticos y terapéuticos) en hemostasia y trombosis en los centros asistenciales de Argentina en 2022
- Identificar diferencias regionales y/o entre los sectores privado y público en la disponibilidad de los recursos mencionados
Materiales y métodos
Estudio de cohorte transversal. Se incluyeron centros asistenciales de la República Argentina. Se obtuvieron datos respecto a la disponibilidad de recursos humanos, diagnósticos, y terapéuticos durante el año 2022. Para ello se envió una encuesta en formulario de Google mediante las vías oficiales de comunicación del Grupo CAHT. Además, la misma fue distribuida en el XV Congreso Argentino del grupo CAHT 2022 y por envíos informales a profesionales de nuestro país. No fueron incluidos los centros que aportaron un porcentaje menor del 70% de los datos solicitados.
Las unidades de análisis fueron los centros asistenciales. Los mismos se clasificaron en instituciones con internación, centros de atención ambulatoria y laboratorios. Los centros con internación fueron clasificados en complejidad según las categorías del registro REFES (Registro Federal de Establecimientos de Salud)(6). El registro caracteriza a los centros con Unidad de Terapia Intensiva (UTI) especializada a aquéllos en los que se atienden pacientes de muy alta complejidad, como post operatorios de cirugías cardíacas o trasplantes. Además, las instituciones fueron agrupadas según el tipo de gestión en públicos y privados. También se registró el tipo de población asistida por el centro: adulta, pediátrica, mixto (pediátrico y adultos).
Los centros asistenciales fueron agrupados en seis regiones:
- CABA
- Gran Buenos Aires y La Plata (GBA/LP)
- Centro y Cuyo: resto de la provincia de Buenos Aires, Córdoba, Santa Fe, La Pampa, Mendoza, San Luis y San Juan
- NOA (Noroeste): Tucumán, Salta, Jujuy, La Rioja, Catamarca, Santiago del Estero
- NEA (Nordeste): Entre Ríos, Corrientes, Formosa, Chaco, Misiones
- Sur: Río Negro, Neuquén, Chubut, Santa Cruz, Tierra del Fuego
Se colectaron datos sobre la disponibilidad de recursos humanos en los centros asistenciales, diagnósticos y terapéuticos. Se relevó información sobre los recursos diagnósticos y terapéuticos de las enfermedades de mayor prevalencia y/o morbi-mortalidad del área.
A continuación se detallan los recursos relevados:
- Variables de recursos humanos: modo de organización de la atención hematológica (servicio, especialista sin conformar un servicio, ausencia de especialistas), número de especialistas en hematología por institución, presencia de sistema de formación en hematología, bioquímicos especialistas en hemostasia/hematología;
- Variables de recursos diagnósticos: TP/APTT/RIN, corrección de TP y APTT con plasma normal, recuento de plaquetas por contador automatizado, fibrinógeno por Clauss, fibrinógeno derivado del TP, tiempo de trombina (TT), tiempo de reptilasa, dímero D (DD)/p roductos de degradación de la fibrina (PDF), heparinemia por Anti Xa, medición de algún anticoagulante oral directo (DOAC), determinación de los factores de la coagulación, pruebas de 1er nivel para enfermedad de von Willebrand -EvW- (FVIII:C, VWF:Ag, VWF:RCo -o actividad de VWF-), pruebas de 2º nivel para EvW (prueba de agregación plaquetaria inducida por ristocetina-RIPA- a bajas dosis , análisis de multímeros del VWF, ensayo de unión del VWF al FVIII (VWF: FVIIIB), ensayo de unión de VWF al colágeno (VWF:CB), cuantificación de VWFpp -propéptidos-), prueba de desmopresina, prueba de agregación plaquetaria, evaluación de adhesividad plaquetaria, estudios genéticos de mutación factor V Leiden y protrombina 20210, determinación de antitrombina, proteína C y S, estudios de síndrome antifosfolípido (inhibidor lúpico, anticardiolipinas, anti-beta 2 glicoproteínas), inhibidor de FVIII, ADAMTS 13 (antígeno, actividad, inhibidor), pruebas viscoelásticas, anti-factor plaquetario 4 / heparina (anti-PF4/hep), ecodoppler venoso, angiotomografía de pulmón.
- Variables de recursos terapéuticos: enoxaparina o heparina no fraccionada para tromboprofilaxis, disponibilidad de DOACs o enoxaparina para el tratamiento de trombosis asociada a cáncer, disponibilidad de enoxaparina para profilaxis o tratamiento en embarazadas, terapias endovasculares en enfermedad trombo-embólica, inserción de filtro de vena cava inferior (FVCI), transfusión de plaquetas, transfusión de plasma, administración de concentrados protrombínicos, administración de concentrado de fibrinógeno o transfusión de crioprecipitados, utilización de desmopresina previo a procedimientos, plasmaféresis terapéutica, inmunoglobulina G endovenosa (IGEV) para el tratamiento de urgencia en trombocitopenia inmune (TI), y terapias de 2ª línea en TI.
En los recursos analíticos se evaluó si la determinación se realizaba en la institución o se derivaba la muestra de sangre o al paciente para la medición en otro centro. Se definió disponibilidad del recurso ante la existencia de alguna de las dos situaciones previas (realización en centro o derivación de muestra/paciente). Además, en el caso de la derivación, se definió un tiempo máximo de obtención del resultado según el estudio y la lógica en la necesidad del resultado para la decisión terapéutica.
En cuatro recursos terapéuticos (anticoagulación en trombosis asociada a cáncer, indicación de enoxaparina en embarazadas y las 2 variables de terapias en TI) se utilizó un amplio abanico de opciones de respuesta contemplando los distintos escenarios de disponibilidad del recurso. Para el análisis comparativo se consideró disponibilidad en estos dos escenarios: “Disponible en todos los pacientes” y “Dependiente de la cobertura, lo obtengo en la mayoría de los pacientes”.
Se realizó un análisis descriptivo. Las variables categóricas fueron presentadas como valores absolutos y relativos, y las numéricas con media y desvío estándar o mediana y rango intercuartil (RIC 25-75) según su distribución. Además, se realizaron comparaciones entre los centros de gestión pública versus privada, y entre distintas regiones, utilizando Chi cuadrado.
Resultados
Datos generales
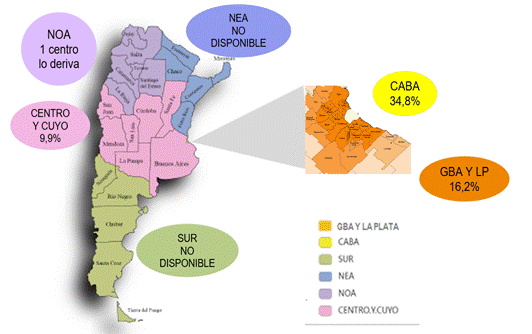
En el estudio se incluyeron 215 centros de 77 ciudades argentinas. Se obtuvieron datos de instituciones de todas las provincias. En la figura 1 y en la tabla 1 se muestra la distribución de los centros por regiones. La mayoría de los encuestados fueron especialistas en hematología. El 85,5% de los centros analizados contaban con internación. Como se observa en la tabla 2, predominaron las instituciones con UTI.
Ciento seis instituciones (46%) atendían a adultos y 15 (7%) brindaban atención exclusiva a pacientes pediátricos. El resto atendía a ambos tipos de pacientes. La distribución según el tipo de gestión (pública o privada) fue equivalente (Tabla 2).
Recursos humanos
En los centros con atención a pacientes (n=204, se excluyeron los laboratorios) se analizó cómo se organizaba la prestación de servicios hematológicos. En 107 (52%) de las instituciones existía servicio de hematología, en 88 (44%) centros había especialistas en hematología sin conformar un servicio, y el resto de las instituciones no contaban con especialistas. En el total de la cohorte, la mediana de especialistas en hematología por institución fue de 3 (RIC 1-5). Se encontraron diferencias marcadas entre las medianas de las regiones: CABA (5), Centro/Cuyo (3,5) GBA/LP (2), NOA (2), NEA (1) y SUR (1). Considerando los centros con internación (n=184), el 27% contaba con 1 o ningún especialista en hematología. En la figura 2 se pueden observar las disparidades entre las regiones en el porcentaje de centros con 1 o ningún especialista.
En el estudio se relevó el porcentaje de centros con internación (n=184) que poseían sistemas de formación en hematología. En 116 (63%) la respuesta fue negativa, 49 (27%) contaban con residencias, 10 tenían sistemas de concurrencia (5%) y 9 formación mediante becas (5%). En este aspecto se encontraron diferencias entre las regiones. Destacamos que el 54% de los centros de CABA poseía algún sistema de formación, en cambio el porcentaje se reducía marcadamente en GBA/LP (30%), NEA (23%) y NOA (26%). Un solo centro del SUR reportó que brindaba formación en hematología.
En la figura 3 se muestra el porcentaje de centros con bioquímicos especialistas en hemostasia/hematología. El 59% de los centros del país reportaron que trabajaban especialistas. El porcentaje fue similar en los centros con UTI y superior (71%) en los efectores con UTI especializadas.
En un mayor porcentaje de centros públicos se desempeñaban bioquímicos especialistas (70% vs 53%, p=NS), aunque la diferencia no fue estadísticamente significativa. La región con menor porcentaje de centros con especialistas fue GBA/LP (37%)
Recursos diagnósticos
Pruebas básicas de la coagulación
Se detectó una amplia disponibilidad de las pruebas básicas de la hemostasia: TP-APTT-RIN (96,5%), recuento de plaquetas por contador automatizado (96%) y corrección de APTT con plasma normal (88,5%). Un alto porcentaje de centros realizaban la determinación de fibrinógeno por Clauss (80%) o derivaban la muestra con resultado en menos de 48 horas (9%). Respecto al tiempo de trombina (TT), el 72% de los centros reportaron que lo realizaban, el 14% derivaba la muestra (con resultado antes de las 48 horas) y el 14% no disponía de la prueba.
Monitoreo especializado de la coagulación
Del total de los centros relevados, el 47% (n=101) realizaban heparinemia por anti Xa, 21,5% (n=47) derivaban la muestra a otra institución con resultado en 48 horas y el 31,5% (n=68) no lo tenía disponible. En la figura 4 se muestra la disponibilidad de heparinemia por anti Xa en las distintas regiones. La disponibilidad (por realización en centro o derivación) fue del 70% en las instituciones con UTI (n=91) y del 85% en las instituciones con UTI especializadas (n=55). Una mayor proporción de centros privados tenían disponible la prueba (por realización o derivación) comparado con los centros públicos (88% vs 59%, p<0,0001).
La amplia mayoría de los centros del país 73% (n=158) no contaban con pruebas para medición de algún DOAC. El 13% (n=27) derivaba la muestra con obtención del resultado en 48 horas, y sólo el 9% (n=19) realizaba la determinación en la institución (5% de los encuestados no reportaron información). La mayoría de los centros que contaban con la prueba eran de CABA (n=7) o Centro/Cuyo (n=7). En el 2022, ningún centro del NOA informó que contaba con la prueba (3 derivaban muestras a otras regiones), y sólo uno del SUR la poseía. La disponibilidad en GBA/LP fue muy baja: 5% (n=2) de los centros contaban con la prueba y 8% (n=3) derivaban la muestra. Sólo 6 instituciones públicas disponían de la prueba en el centro o por derivación.
Factores de la coagulación
En la tabla 3 se muestra la proporción de centros con disponibilidad de los distintos factores de la coagulación. El 52% de los centros del país relevados no tenían disponible para sus pacientes la determinación de factor XIII (por realización en el centro o derivación). El 9% de los centros reportaron que realizaban la medición de todos los factores, y el porcentaje ascendía a 39% cuando también se contemplaba la derivación.
Patologías hemorrágicas: enfermedad de von Willebrand, trombocitopatías y hemofilia adquirida
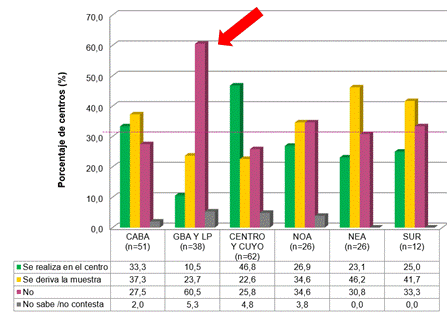
En la EvW, el 36% (n=77) de las instituciones reportaron que realizaban las pruebas de primer nivel, 32% (n=69) derivaba la muestra a otro centro con resultado en menos de 72 horas y un porcentaje similar no tenía disponibilidad de las pruebas. Se detectaron disparidades regionales (Figura 5) y entre los sectores público y privado (Figura 6). La disponibilidad de las pruebas de diagnóstico de 2° nivel de EvW fue muy baja: el 12% contaba con alguna prueba y el 26% tenían capacidad para derivar al paciente.
Se evaluó la disponibilidad de la prueba de la desmopresina en los centros con atención de pacientes (n=204, se excluyeron los laboratorios). El 22% reportaron que realizaban la prueba en su centro, en 27,5% que derivaban el paciente a otra institución, mientras que un 47% no tenía capacidad de ofrecer el estudio a sus pacientes (un 3,5% de los encuestados no reportaron información). Un alto porcentaje de los centros (42%) que realizaban estudios de 1er nivel de EvW no efectuaban pruebas de la desmopresina (Figura 7).
La mayoría de los centros del país (50,5%) reportaron que no podían brindar a sus pacientes pruebas de agregación plaquetaria. Por otro lado, el 13,5% informaron que realizaban la prueba y un 32% tenían capacidad de derivar al paciente (el 4% de los encuestados no reportaron respuesta). En la figura 8 se puede observar la proporción de centros por regiones que contaban con agregación plaquetaria o que tenían capacidad para derivar al paciente. Se observaron disparidades, y GBA/LP era la región con menor porcentaje de disponibilidad de la prueba. En los siguientes distritos se detectaron instituciones con agregómetros: CABA, GBA/LP, Santa Cruz, Corrientes, Misiones, Santa Fe, Tucumán, Córdoba y Neuquén, aunque en estas últimas dos provincias sólo en centros privados. Una mayor proporción de centros privados tenían disponibilidad de la prueba (por realización o derivación del paciente) comparado con los públicos (55% vs 37%, p=0,008). La disparidad fue más notoria en el AMBA-Área Metropolitana de Buenos Aires- (56% vs 28,5%, p=0,01).
La disponibilidad de la determinación de inhibidor de factor VIII se puede describir en tercios: 31% realizaban la prueba en el centro, 32% derivaban la muestra y 34% no contaban con el recurso (3% no reportaron información). En la figura 9 se muestran las disparidades regionales. También se detectaron diferencias según el tipo de gestión de los centros, ya que se observó una mayor proporción de centros privados con disponibilidad (realizada en centro o por derivación) de la prueba (72,9% vs 51,9%, p=0,001).
Estudios de trombofilias
En la figura 10 se describe la disponibilidad de los estudios de trombofilia. Se detectaron marcadas disparidades entre las regiones en la proporción de instituciones que realizaban la determinación de inhibidor lúpico: CABA (63%), GBA/LP (39,5%), Centro/Cuyo (61%), NOA (19%), NEA (23%), SUR (42%). Se evaluó la relación entre la realización de inhibidor lúpico en los centros y la presencia de bioquímico especialista en hemostasia/hematología (figura 11). Una mayor proporción de centros en los que se realizaba inhibidor lúpico presentaba bioquímico especialista en hemostasia/hematología (80, 2% vs 40,4%, p<0,0001).
Diagnóstico de trombocitopenia inducida por heparina (HIT)
Se detectó una muy baja disponibilidad de las pruebas de anticuerpos anti-PF4/hep. Teniendo en cuenta los centros con internación (n=184), el 79% (n=146) respondieron que no disponían del estudio, 11,5% (n=21) derivaba la muestra con resultado en menos de 48 horas y sólo el 4% (n=8) realizaba la determinación (5% no reportaron información). Centros de 3 regiones reportaron que realizaban la prueba: CABA (n=5, 11%), GBA/LP (n=2; 5,5%) y Centro/Cuyo (n=1; 2,2%). El NEA y el SUR no tenían disponibilidad de la prueba diagnóstica (Figura 12). En la figura 13 se muestra la diferencia en la disponibilidad entre los sectores privado y público (26,5% vs 5,9%, p<0,0001). Una minoría de centros públicos realizaba la prueba o derivaba la muestra.
Otras pruebas analíticas
Se registró una alta disponibilidad de dímero D (DD) cuantitativo y de PDF: 72% por realización en la institución y 15% por derivación con resultado en las primeras 48 horas.
Como contrapartida, la disponibilidad de ADAMTS 13 (antígeno, actividad, anticuerpos) fue baja: 3% (n=7) se realizaba en el centro, 35,5% (n=76) se derivaba la muestra, y el 57,5% (124) no contaba con disponibilidad del estudio (4% no informado).
Diferencias público-privado de pruebas analíticas en AMBA
En la región del AMBA, detectamos asimetrías muy marcadas entre los sectores público y privado en la disponibilidad de la mayoría de las pruebas de laboratorio (Tabla 4).
Pruebas viscoelásticas
Se evaluó la disponibilidad de tromboelastograma/ROTEM en los centros con UTI especializada (n=55). En la mayoría de ellos el recurso no estaba disponible (Figura 14).
Estudios por imágenes
En la tabla 5 se describe la disponibilidad de la ecografía doppler y de angiotomografía para el diagnóstico de tromboembolismo de pulmón. Respecto a este último estudio, se detectó que una mayor proporción de centros privados contaban con el recurso (76% vs 56%, p=0,003). No se observaron diferencias regionales notorias. Las áreas con menor proporción de centros con el recurso fueron GBA/LP (58%) y el NOA (54%).
Recursos terapéuticos
Terapias anticoagulantes
En los centros con internación (n=184), se observó una amplia disponibilidad de heparina no fraccionada (91%), enoxaparina (91%), ambas para profilaxis, y enoxaparina para el inicio de tratamiento de enfermedad tromboembólica venosa (92%).
En la tabla 6 se describe la disponibilidad de enoxaparina para la profilaxis/tratamiento de las embarazadas y, además, la disponibilidad de enoxaparina o DOACs para el tratamiento de la trombosis asociada a cáncer. Respecto a este último recurso se observaron diferencias entre los sectores privado y público (privado 77% vs público 42%, p=0,0001).
Terapias endovasculares
En los centros con internación (n=184) se evaluó la posibilidad de inserción de filtro de vena cava inferior (FVCI). Se obtuvieron las siguientes respuestas: disponible en 50,5% (n=93), no disponible 32,5% (n=60), y no se obtuvieron datos en 17% (n=31). La disponibilidad en los centros privados duplicó a la de los públicos (70% vs 35%, p=0,0001). El GBA/LP fue el área con menor proporción de centros con internación relevados con posibilidad de inserción de FVCI: 48,5%. La disponibilidad en el resto de las regiones fue: CABA (59%), Centro/Cuyo (61%), NOA (58%), NEA (64%), SUR (78%).
Respecto a las terapias endovasculares para ETV, se detectó una disponibilidad del 48% en los centros con internación encuestados. Al igual que con FVCI, un porcentaje marcadamente mayor de los centros privados contaban con el recurso (69% vs 31%, p=0,0001).
Terapias con hemocomponentes y hemoderivados
Se observó una alta disponibilidad para transfusión de plaquetas y plasma en los centros con internación (Figura 15).
En la tabla 7 se describe la disponibilidad, en los centros con internación, para la infusión de concentrado protrombínicos y para la administración de fibrinógeno/crioprecipitados. Como se puede observar, el porcentaje de centros con este último recurso fue más elevado respecto a la disponibilidad de concentrados protrombínicos. Una proporción más alta de centros privados contaban con concentrado protrombínico (70% vs 47,5%, p=0,002). Como contrapartida, no se observaron diferencias estadísticamente significativas en fibrinógeno/crioprecipitados entre los sectores público y privado, ni tampoco entre las regiones (rango de disponibilidad entre 72% y 82% en las regiones); aunque sí las hubo en la disponibilidad de concentrado protrombínico. El NEA (50%) y NOA (36%) fueron las regiones con un porcentaje menor de centros relevados con acceso a la terapia.
Indicación de desmopresina previo a procedimientos
El 49% de los centros con internación (n=184) reportaron que habitualmente tenían a disposición desmopresina para los procedimientos y un 20% tenían acceso con una disponibilidad irregular. No se observaron diferencias significativas entre las regiones. El NOA mostró el porcentaje menor de centros con disponibilidad (32%). No se observaron diferencias estadísticamente significativas entre los centros privados y públicos (57% vs 43%, p=0,058).
Terapia de recambio plasmático
En la figura 16 se detalla la proporción de centros con internación con terapia de recambio plasmático en cada región. En este recurso también se observaron diferencias entre los sectores privado y público (72% vs 48%, p=0,003).
Tratamiento para trombocitopenia inmune (PTI)
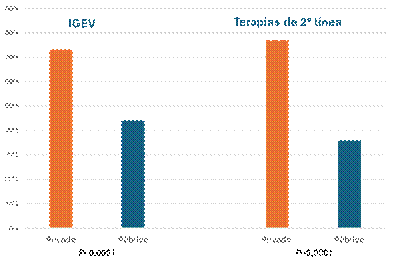
En el estudio se relevó la disponibilidad de algunas terapias para la TI. Se evaluaron el acceso a la inmunoglobulina G EV (IGEV) con hemorragia severa en las primeras 12 horas desde su indicación y a esquemas de 2ª línea (agonistas del receptor de la trombopoyetina o rituximab) en los primeros 7 días desde la prescripción médica. En la tabla 7 se resume la información obtenida. En ambos recursos se detectaron diferencias significativas en la disponibilidad (Respuestas a “todos los pacientes” o “a la mayoría de los pacientes”), con una mayor proporción para las instituciones privadas (Figura 17). Además, en ambas terapias se observó que las regiones del GBA/LP y NOA presentaban la menor proporción de centros con disponibilidad: en IGEV NOA 42% y GBA/LP 41%, y en terapias de 2ª línea, NOA 42% y GBA/LP 43%.
Discusión
Presentamos un amplio relevamiento de los recursos de hemostasia y trombosis disponibles en Argentina en el año 2022. En el relevamiento se logró obtener información de instituciones de todas las provincias argentinas y 77 ciudades estuvieron representadas. Consideramos que es un aporte valioso para la gestión de los recursos del área. Hasta el momento existía muy escasa información al respecto, con datos fragmentados según algunas patologías específicas.
En el relevamiento observamos una baja disponibilidad en general de los recursos de mayor complejidad. Además, se detectaron notorias disparidades regionales, principalmente en los recursos diagnósticos, con una tendencia a una distribución centralista. También los datos mostraron diferencias profundas entre los sectores públicos y privados, fundamentalmente en los recursos terapéuticos.
Los recursos humanos fueron evaluados desde la perspectiva de las instituciones, debido a que fueron las unidades de análisis. Por las características del estudio no se pudo determinar la cantidad y distribución de los especialistas en hematología o bioquímica en el país. Respecto a los especialistas en hematología, observamos un alto porcentaje de “trabajo solitario”, es decir, instituciones con sólo un especialista. Esta condición suele generar problemas en el desempeño asistencial, principalmente por sobrecarga de trabajo o imposibilidad de discusión de casos complejos, barreras para el desarrollo académico, entre otros. La proporción de centros con trabajo solitario fue particularmente alta en el NOA, NEA y SUR. En las dos últimas regiones mencionadas superó el 50%. CABA fue la región con menor proporción, un dato esperable considerando la mayor densidad de profesionales médicos.
Aproximadamente el 60% de las instituciones reportaron que contaban con bioquímicos especialistas en hemostasia/hematología. Resulta sumamente complejo estimar si ese porcentaje es el adecuado para nuestro sistema de salud, teniendo en cuenta la escasa información publicada y algunas características de nuestro sistema, como su alta fragmentación. Sin embargo, pudimos observar que en alrededor de un 30% de los centros con UTI especializadas no trabajaban bioquímicos expertos en hemostasia/hematología. Consideramos que las instituciones que asisten a pacientes de una complejidad tan alta necesitan contar con este tipo de especialistas para brindar atención de calidad. Por otro lado, detectamos diferencias regionales marcadas en el porcentaje de centros con bioquímicos especializados. Resulta llamativamente bajo el porcentaje en GBA/LP (37%), la mitad que en otras regiones como CABA y Centro/Cuyo.
De manera interesante, la presencia de bioquímico especialista fue un factor que influyó en la disponibilidad de pruebas de mayor complejidad, como por ejemplo el inhibidor lúpico, que requiere un alto nivel de entrenamiento en el área.
En los recursos analíticos se consideró disponibilidad ante la presencia de la prueba en el centro o la derivación de la muestra/paciente. Se definió que el recurso estaba disponible para los pacientes atendidos en el centro relevado cuando podía ser ofrecido por realización en la institución o derivación. En ningún sistema del mundo todos los efectores de salud cuentan con la totalidad de las pruebas. Sin embargo, para evitar inequidades en el acceso es imprescindible que el sistema se organice según niveles de complejidad para que el recurso esté disponible cuando sea necesario. Para cumplir con ese objetivo es esencial desarrollar redes integradas de servicios de salud (RISS). Los modelos sanitarios con perspectiva de RISS tienen ventajas en la gestión y asignación de los recursos(7,8). Cuando las instituciones se organizan en red es más probable que se obtenga el objetivo de brindar asistencia de forma equitativa e integrada. Las RISS mejoran la accesibilidad del sistema, reducen la fragmentación. El desarrollo de las RISS debe estar orientado a las necesidades de la población que asiste. Por ese motivo, requiere ajustes continuos.
Existe un amplio desarrollo teórico respecto a las clasificaciones de las RISS. Una de las más útiles es la que se refiere a redes geográficas, que asisten a una población de una región determinada, o redes de aseguramiento, población definida según tipo de cobertura(9). Las redes geográficas integradas verticalmente según niveles de complejidad con mecanismos aceitados de referencia y contra-referencia pueden ser un camino para optimizar el acceso a la salud.
Observamos una alta disponibilidad de las pruebas básicas de la coagulación. Sin embargo, la situación no fue similar en los estudios de mayor complejidad. La disponibilidad del dosaje de DOACs fue muy baja en el país (menor al 25%), y una minoría de centros de las regiones distintas a CABA y Centro/Cuyo podían ofrecer el estudio a sus pacientes. La disponibilidad de la prueba de heparinemia por anti Xa fue mayor, posiblemente debido a su mejor estandarización y uso expandido. Sin embargo, un porcentaje alto de centros de alta complejidad no tenían la prueba (30% centros con UTI y 15% con UTI especializada).
Detectamos dificultades significativas en el diagnóstico de los desórdenes hemorrágicos. Aproximadamente un tercio de los centros no tenían posibilidad de ofrecer a sus pacientes los estudios de 1er nivel de EvW. Además, se observaron notorias disparidades regionales y entre los sectores público y privado, a favor de este último. Un hallazgo relevante fue el alto porcentaje de centros que con capacidad de realizar estudios de 1er nivel de EvW que no realizaban la prueba de desmopresina. En el grupo hipotetizamos que razones logísticas (requerimiento de hospital de día, disponibilidad de recurso humano, acceso a la droga) y dificultad en el recupero de costos, podrían ser explicaciones de esta brecha. Además, hallamos barreras en el diagnóstico de hemofilia adquirida, ya que alrededor de un tercio de los centros no tenían capacidad de ofrecer a sus pacientes la detección de inhibidor de FVIII.
En este relevamiento detectamos una notoria limitación en el estudio de las disfunciones plaquetarias. Alrededor de la mitad de los centros reportados no podían ofrecer a sus pacientes la prueba de agregación plaquetaria). En el 2022, la mayoría de las provincias no tenían instituciones equipadas con agregómetros. Si tenemos en cuenta la imposibilidad técnica de derivar la muestra para obtener un resultado confiable, se plantea, como una posible solución, expandir la disponibilidad del equipamiento para incrementar el acceso al diagnóstico de las disfunciones plaquetarias.
La disponibilidad de la detección de anti-PF4/hep fue muy baja en el país en 2022. En amplias regiones, como el SUR y NEA, ninguna institución tenía capacidad para realizar diagnóstico de HIT por realización de la prueba o derivación. Los centros públicos excepcionalmente pudieron ofrecer la prueba a sus pacientes. En un estudio reciente conducido por nuestro grupo (en proceso de publicación) detectamos que una de las principales causas de la falta de disponibilidad era la baja sospecha clínica con la consecuente subestimación de la solicitud del estudio. El fortalecimiento de la formación en esta patología es una herramienta valiosa para optimizar el diagnóstico.
El análisis de los recursos terapéuticos mostró una asimetría muy notoria entre los sectores público y privado. En varias de las terapias de mayor complejidad, la proporción de instituciones privadas con el recurso disponible duplicaba a las públicas. Del análisis de estos resultados se afirma el grado de segmentación según tipo de cobertura del sistema de salud argentino.
El relevamiento cuenta con debilidades que es necesario poner en relieve para una mejor interpretación de los datos. Tal vez la de mayor peso es el marcado predominio en el relevamiento de instituciones de complejidad alta y muy alta. Por ello, es muy probable que la disponibilidad en la realidad sea inferior. Además, no se pudo determinar el impacto asistencial de las instituciones incluidas, es decir, el tamaño poblacional que cada centro atiende, permitiendo una determinación más precisa de la disponibilidad de cada recurso. Por otro lado, debido a que las unidades de análisis fueron los centros asistenciales, no se pudo estimar adecuadamente la fuerza de trabajo en el área en cuanto a cantidad de profesionales y su distribución.
En el grupo consideramos que las sociedades científicas están en condiciones de realizar aportes valiosos para ampliar el acceso a los recursos y reducir disparidades. Aunque la tarea no es sencilla, si tenemos en cuenta la complejidad del problema y las limitaciones de acción e incumbencia. Como se demostró en este proyecto, cuando conducen un relevamiento de los recursos disponibles, se puede alcanzar una amplia representación debido a las fuertes redes de profesionales establecidas en este tipo de organizaciones. Además, la formación de profesionales y la asesoría de los gestores de salud son acciones muy relevantes para disminuir las inequidades de acceso.
Conclusiones
En este amplio relevamiento detectamos una disponibilidad sub-óptima de los recursos físicos de alta complejidad y un alto porcentaje de “trabajo solitario”. Además, pudimos mensurar las disparidades público-privada y regionales en la disponibilidad en los recursos del área. Consideramos que el establecimiento y expansión de redes integradas es una estrategia que permitirá reducir las inequidades de acceso. Sin lugar a dudas, son necesarias políticas sanitarias activas para afrontar las notorias brechas de acceso a los servicios. Desde su lugar, las sociedades científicas pueden realizar valiosos aportes para obtener esa meta.
Bibliografía
- Zelmer J. Measuring Progress in Access to Health Services. Health Policy. 2018;14:6-9. doi: 10.12927/hcpol.2018.25554.
- Almeida APSC, Nunes BP, Duro SMS, Facchini LA. Socioeconomic determinants of access to health services among older adults: a systematic review. Rev Saude Publica. 2017;51:50. doi: 10.1590/S1518-8787.2017051006661.
- Navarro Pérez P, Jesús Contreras Sánchez A, Junco Gómez MC, Sánchez Villegas P, Sánchez-Cantalejo Garrido C, Luque Martin N. ANÁLISIS DE LA DISTRIBUCIÓN GEOGRÁFICA DE MÉDICOS ESPECIALISTAS EN LA REPÚBLICA ARGENTINA. Informe del Ministerio de Salud Argentino, 2015.
- Gulliford M, Figueroa-Munoz J, Morgan M, y col. What does 'access to health care' mean? J Health Serv Res Policy. 2002;7:186-8. doi: 10.1258/135581902760082517.
- Garcia MM, Barbosa MM, Silva RM, Reis EA, Alvares J, Assis Acurcio F, Godman B, Guerra Junior AA. Indicator of access to medicines in relation to the multiple dimensions of access. J Comp Eff Res. 2019 Sep;8(12):1027-1041. doi: 10.2217/cer-2019-0031.
- https://sisa.msal.gov.ar/sisadoc/docs/050101/refes_home.jsp
- Barrios O, Méndez C, Holder Morrison R, Suárez Jiménez J. Redes integradas de servicios e salud: el desafío de los hospitales. Presentación OMS/OPS Chile. Número 1, 2011.
- Booth M, Hill G, Moore MJ, Dalla D, Moore MG, Messenger A. The new Australian Primary Health Networks: how will they integrate public health and primary care? Public Health Res Pract. 2016; 26:e2611603. doi: 10.17061/phrp2611603.
- Vásquez Navarrete M, Vargas Lorenzo I. Redes integradas de servicios de salud: ¿solución o problema? Revista de Ciencias de la Salud. 2006; 4:5-9.
Agradecimientos: "A los profesionales que participaron con el envío de datos para el relevamiento, a Roberto Pozner y a la CD del CAHT 2021-2023, a Luis Bastos y a la CD del CAHT 2023-2024, a Miguel Castro Ríos".
Contribución de autores: Todas las personas autoras han efectuado una contribución sustancial a la concepción o el diseño del estudio o a la recolección, análisis o interpretación de los datos; han participado en la redacción del artículo o en la revisión crítica de su contenido intelectual; han aprobado la versión final del manuscrito; y son capaces de responder respecto de todos los aspectos del manuscrito de cara a asegurar que las cuestiones relacionadas con la veracidad o integridad de todos sus contenidos han sido adecuadamente investigadas y resueltas
Figura 1. Distribución por regiones de los centros incluidos
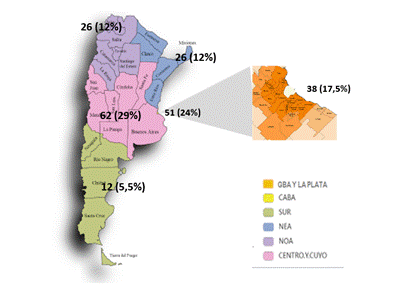
CABA: Ciudad autónoma de Buenos Aires; GBA/LP: Gran Buenos Aires y La Plata; NOA: Noroeste Argentino; NEA: Noreste Argentino
Tabla 1. Distribución y caracterización de los centros incluidos
|
Regiones |
Cantidad de centros N (%) |
Cobertura (%) |
Centros con internación (%) |
||
|
Público |
Privado |
||||
|
CABA |
51 (24) |
35% |
65% |
90% |
|
|
Gran Buenos Aires y La Plata |
38 (17,5) |
63% |
37% |
97% |
|
|
Centro y Cuyo |
62 (29) |
48,5% |
51,5% |
100% |
|
|
NOA |
26 (12) |
65,5% |
34,5% |
73% |
|
|
NEA |
26 (12) |
61,5% |
38,5% |
84,5% |
|
|
SUR |
12 (5,5) |
25% |
75% |
75% |
|
Centros por provincias
Centro y Cuyo: Resto de la provincia de Buenos Aires (15), Córdoba (18), Santa Fe (16), La Pampa (2), San Luis (4), Mendoza (5), San juan (2)
NOA: Tucumán (7), Salta (10), Jujuy (1), Santiago del Estero (4), La Rioja (1), Catamarca (3)
NEA: Entre Ríos (10), Corrientes (5), Chaco (3), Misiones (7), Formosa (1)
SUR: Neuquén (5) Río Negro (2), Chubut (2), Santa Cruz (2), Tierra del Fuego (1)
Tabla 2. Datos generales
|
Instituciones incluidas, n |
215 |
|
Centros con internación, n (%) |
184 (85,5) |
|
Internación con UTI, n |
91 |
|
Internación con UTI especializada, n |
55 |
|
Internación de complejidad baja o mediana, n |
38 |
|
Centros sin internación, n (%) |
20 (9,5) |
|
Laboratorios, n (%) |
11 (5) |
|
Especialidad del encuestado, n (%) |
|
|
Hematólogo |
116 (54) |
|
Bioquímico |
62 (29) |
|
Hematólogo y bioquímico* |
27 (12) |
|
Internista |
5 (2,5) |
|
Otro |
5 (2,5) |
|
Años de trabajo en la institución del encuestado, mediana (RIC) |
12 (5-22) |
|
Población de pacientes de la institución, n (%) |
|
|
Adultos |
106 (49) |
|
Pediátricos |
15 (7) |
|
Ambos |
94 (44) |
|
Tipo de gestión, n (%) |
|
|
Pública |
108 (50) |
|
Privada |
107 (50) |
*La encuesta fue respondida por un médico hematólogo y por un bioquímico
UTI: Unidad de terapia intensiva; RIC: Rango inter-cuartil
Figura 2. Porcentaje de centros por región con 1 o ningún especialista médico en hematología
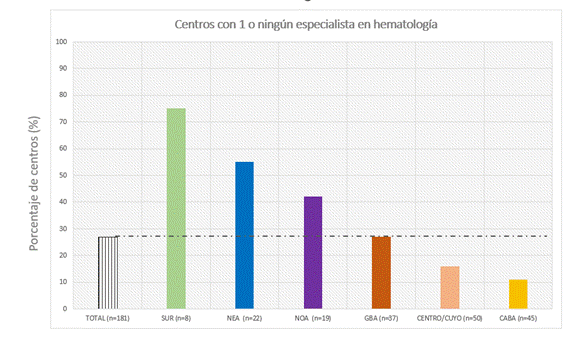
Figura 3. Porcentaje de centros con bioquímico especialista en hemostasia/hematología
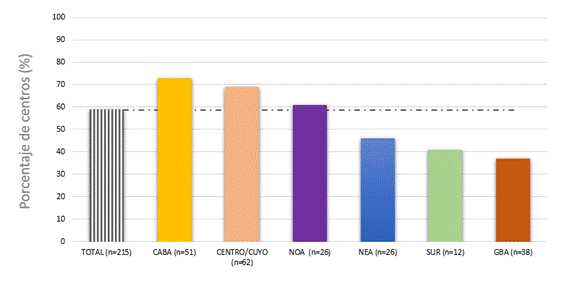
Figura 4. Disponibilidad en las regiones de heparinemia por Anti Xa (n=215)
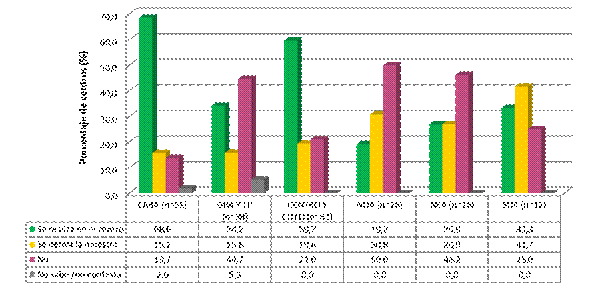
Tabla 3. Disponibilidad de factores de la coagulación por regiones.
|
Factores II,V, VII, VIII, IX, X (Todos ellos), % |
Total |
CABA |
GBA/ LP |
Centro/ Cuyo |
NOA |
NEA |
SUR |
|
Se realiza en el centro |
52,5 |
74,5 |
34 |
61,5 |
46 |
34,5 |
25 |
|
Se deriva la muestra* |
17 |
15,5 |
26,5 |
24 |
38,5 |
46 |
58 |
|
No está disponible |
29 |
10 |
34 |
14,5 |
15 |
15,5 |
17 |
|
No sabe/ no contesta |
1,5 |
0 |
5,5 |
0 |
1,5 |
0 |
0 |
|
Factor XI y XII, % |
|||||||
|
Se realiza en el centro |
34 |
59 |
21 |
39 |
19 |
19 |
0 |
|
Se deriva la muestra* |
26 |
11,5 |
21 |
21 |
38,5 |
46 |
58 |
|
No está disponible |
36 |
23,5 |
52,5 |
37 |
35 |
35 |
42 |
|
No sabe/ no contesta |
4 |
6 |
5,5 |
3 |
7,5 |
0 |
0 |
|
Factor XIII, % |
|||||||
|
Se realiza en el centro |
16 |
27,5 |
10,5 |
19 |
4 |
4 |
16 |
|
Se deriva la muestra* |
26 |
19,5 |
18,5 |
21 |
38,5 |
42 |
26 |
|
No está disponible |
52 |
39 |
66 |
55 |
50 |
54 |
51,5 |
|
No sabe/ no contesta |
6 |
13 |
5 |
5 |
7,5 |
0 |
6,5 |
*Se deriva la muestra y se obtiene el resultado en menos de 48 horas
Figura 5. Disponibilidad por regiones de las pruebas diagnósticas de 1° nivel en enfermedad de von Willebrand
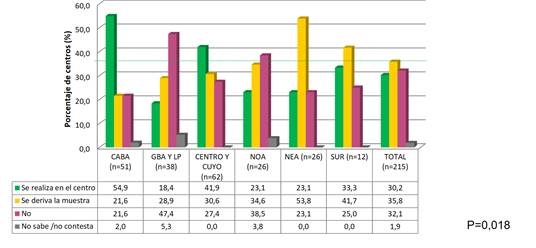
Figura 6. Comparación entre los sectores en la disponibilidad de pruebas de 1er nivel en enfermedad de von Willebrand
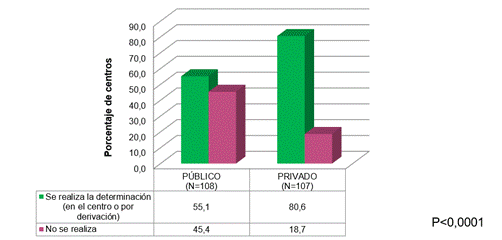
Figura 7. Relación entre las pruebas diagnósticas en enfermedad de von Willebrand y prueba de la desmopresina
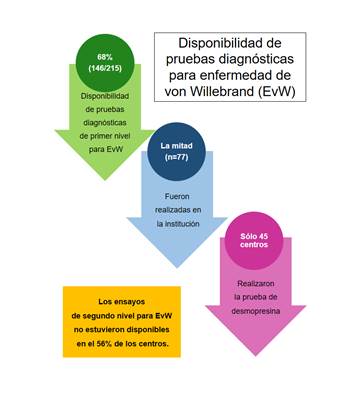
Figura 8. Disponibilidad de agregación plaquetaria por regiones
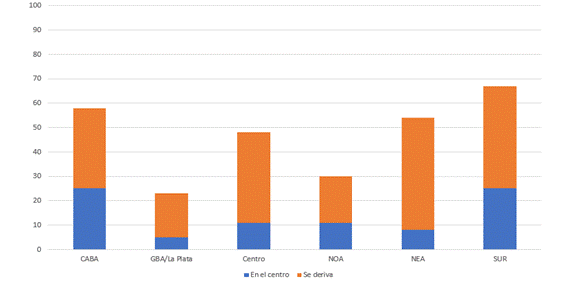
Figura 9. Disponibilidad de inhibidor de FVIII por regiones
La región de GBA/LP fue la que presentó el mayor porcentaje de centros sin disponibilidad de inhibidor de FVIII. La diferencia con las otras regiones fue marcada.
Figura 10. Análisis de disponibilidad de estudios de trombofilias
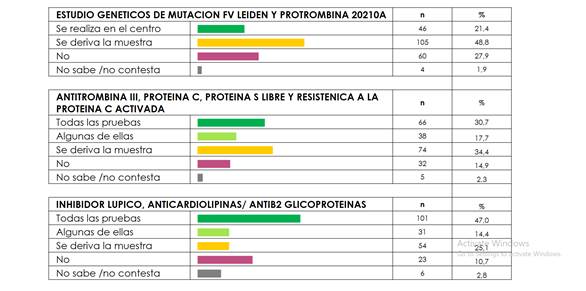
Figura 11. Proporción de bioquímicos especialistas en hemostasia según la realización de inhibidor lúpico en el centro
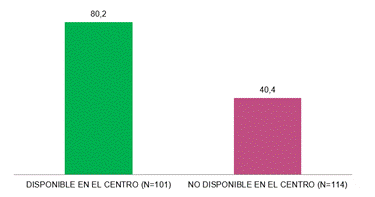
Figura 12. Disponibilidad de anti-PF4/hep en centros con internación (n=184) en las regiones argentinas
Anti-PF4/hep: Anticuerpos anti complejo heparina/factor plaquetario 4
Figura 13. Comparación entre los sectores privado y público
en la disponibilidad de anti-PF4/hep 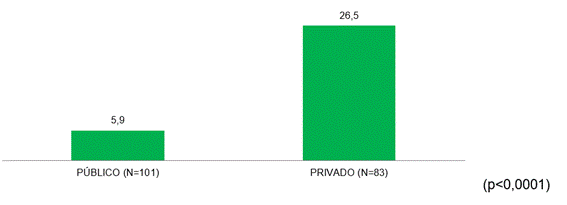
Figura 14 Disponibilidad de pruebas viscoelásticas en centros con UTI especializada
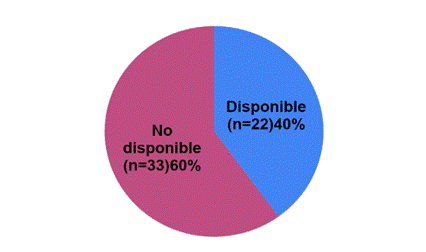
Tabla 4. Comparación de las pruebas de laboratorio entre los sectores público y privado en la región del AMBA
|
Público N=42 n (%) |
Privado N=41 n (%) |
p |
|
|
Anti Xa |
25 (59,5) |
33 (80,5) |
0,037 |
|
DOACs |
4 (9,5) |
14 (34) |
0,007 |
|
FXIII |
13 (31) |
19 (46) |
0,150 |
|
EvW 1° nivel |
19 (45) |
34 (83) |
0,0001 |
|
Agregación plaquetaria |
12 (28,5) |
23 (56) |
0,011 |
|
Inhibidor de VIII |
13 (31) |
32 (78) |
0,0001 |
|
Anti-H/PF4 |
3 (7) |
19 (46) |
0,0001 |
Anti Xa: heparinemia por anti Xa; DOACs: anticoagulantes orales directos; EvW: enfermedad de von Willebrand; Anti-H/PF4: Anti complejo heparina/factor plaquetario 4
Tabla 5. Disponibilidad de pruebas para diagnóstico de enfermedad tromboembólica venosa
|
Ecodoppler n (%) |
Angiotomografía n (%) |
||
|
Se realiza en el centro |
157 (77) |
134 (66) |
|
|
No disponible |
35 (17) |
53 (26) |
|
|
No sabe /no contesta |
12(6) |
17 (8) |
|
Tabla 6. Disponibilidad de enoxaparina para el manejo de pacientes embarazadas
|
Enoxaparina para profilaxis/tratamiento de embarazadas n (%) |
Enoxaparina o DOACS para el tratamiento de ETV asociado a cáncer n (%) |
|
|
Sí, en todos los pacientes |
107 (53) |
73 (36) |
|
Depende de la cobertura, lo obtengo en la mayoría |
31 (15) |
47 (23) |
|
Depende de la cobertura, lo obtengo en la minoría |
8 (4) |
16 (8) |
|
No, en ocasiones se obtiene por otros medios (donaciones, préstamos) |
11 (5) |
11 (5) |
|
Sí, pero la disponibilidad es muy irregular |
0 |
14 (7) |
|
No |
2 (1) |
20 (10) |
|
No sabe/ no contesta |
45 (22) |
23 (11) |
Figura 15
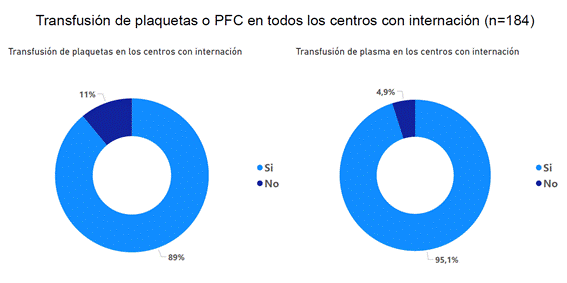
Tabla 7. Disponibilidad de concentrados protrombínicos y concentrado de fibrinógeno/transfusión de crioprecipitados
|
|
Infusión de concentrados protrombínicos n (%) |
Concentrado de fibrinógeno o transfusión de crioprecipitados n (%) |
|
Se realiza en el centro |
106 (57) |
142 (77) |
|
La disponibilidad es muy irregular |
26 (14) |
15 (8) |
|
No |
35 (19) |
16 (9) |
|
No sabe/ no contesta |
17 (9) |
11 (6) |
Figura 16 Disponibilidad en las regiones de la terapia de
recambio plasmático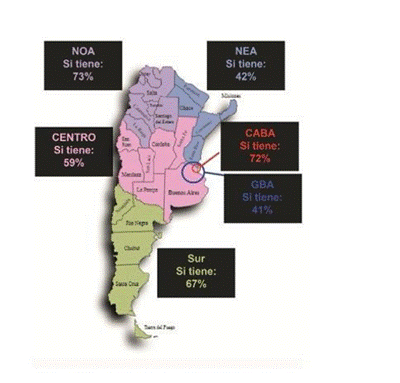
Tabla 8 Disponibilidad de IGEV y terapias de 2ª línea en TI
|
IGEV para TI con sangrado severo n (%) |
Terapias de segunda línea en PTI n (%) |
|
|
Sí, en todos los pacientes |
68 (37) |
43 (21) |
|
Depende de la cobertura, lo obtengo en la mayoría |
37 (20) |
71 (35) |
|
Depende de la cobertura, lo obtengo en la minoría |
8 (4) |
12 (6) |
|
No, en ocasiones se obtiene por otros medios (donaciones, préstamos) |
7 (4) |
14 (7) |
|
La disponibilidad es muy irregular |
28 (15) |
16 (8) |
|
No |
15 (8) |
25 (12) |
|
No sabe/ no contesta |
21 (11) |
23 (11) |
Figura 17. Comparación entre los sectores público y privado en la disponibilidad de IGEV y en las terapias de 2ª línea en TI