Células precursoras hematopoyéticas en sangre periférica
Hematopoietic precursor cells in peripheral blood
Sánchez N1, Minissale C1, Martínez E1, Malusardi C2, Sciaccaluga D3, Auat M2, Altube A2.
1 Cuerpo médico. División Hematología. Hospital de Clínicas “José de San Martín”, Universidad de Buenos Aires.
2 Laboratorio de Citometría de Flujo. División Hematología. Hospital de Clínicas “José de San Martín”, Universidad de Buenos Aires.
3 Departamento de Patología. Hospital de Clínicas “José de San Martín”, Universidad de Buenos Aires.
Sanchez: https://orcid.org/0009-0002-0366-8527
Minissale: https://orcid.org/0009-0006-9988-656X
Martinez: https://orcid.org/0009-0001-7704-3362
Malusardi: https://orcid.org/0000-0002-7287-8539
Sciaccaluga: https://orcid.org/0009-0008-5031-2383
Auat: https://orcid.org/0000-0001-9312-9249
Altube: https://orcid.org/0000-0003-4380-6779
altubea@hospitaldeclinicas.uba.ar
Palabras claves: células madre,
precursores hematopoyéticos,
hematopoyesis extramedular,
CD34,
mielofibrosis.
Keywords: stem cells,
hematopoietic precursor cells,
CD34,
extramedullary hematopoiesis,
myelofibrosis.
Introducción
En una medula ósea (MO) normal se detectan dos compartimentos de células que expresan CD34: una población principal que corresponde a las células precursoras hematopoyéticas (CPH) y una población minoritaria que corresponde a células endoteliales (células del estroma medular). Las CPH son una población celular heterogénea que incluye precursores CD34+ pluripotentes no comprometidos hacia ninguna línea celular y precursores CD34+ ya comprometidos. Dentro de esta última población, se observa compromiso a linaje linfoide B y hacia las diferentes líneas mieloides, es decir, compromiso a línea eritroide, megacariocítica, monocítica, mieloide granular neutrófila, a eosinófilos, y también a líneas mieloides minoritarias como basófilos, mastocitos y células dendríticas. En condiciones normales, un pequeño porcentaje de CPH (menor a 0,10%) se encuentran circulando en sangre periférica (SP), desde aquí migran a nichos medulares distantes con el objetivo de mantener niveles adecuados y constantes de hematopoyesis. Estas CPH circulantes, en su mayoría son CD34+ no comprometidas a ninguna línea celular(1).
Bajo ciertas condiciones de estrés, como infecciones, tumores sólidos, ciertas neoplasias hematológicas, anemia, estrés metabólico o cambios en el microambiente hematopoyético, una gran cantidad de CPH son liberadas desde MO a SP, proceso conocido como “movilización”. Estas CPH movilizadas son la base para inducir hematopoyesis extramedular (HEM), mecanismo compensatorio para la hematopoyesis ineficaz de la MO(2). Los sitios más comunes para la HEM incluyen bazo e hígado, aunque también ha sido descripta en muchos otros tejidos, incluida la piel(3).
El inmunofenotipo de las CPH no comprometidas muestra CD34intenso CD38débil HLADR+ CD117+ CD33+ CD13+, en ausencia de otros marcadores asociados a línea linfoide y mieloide(1), y morfológicamente tienen un aspecto inmaduro linfoblastoide.
Caso clínico
Paciente con diagnóstico de mielofibrosis primaria (MFP). En la figura 1 se muestra el frotis de sangre periférica (FSP) en el que se observan células de aspecto inmaduro. Una de las características de la MFP es la HEM, por lo que los recuentos de CD34+ en SP se encuentran habitualmente elevados. Otro de los rasgos característicos es la anisopoiquilocitosis, los hematíes en lágrima o dacriocitos y la reacción leucoeritroblástica en SP (Figura 2).
En la figura 3 se muestran los dot plots obtenidos por citometría de flujo multiparamétrica (CFM) de SP. El inmunofenotipo evidenció que las células de la figura 1 correspondían a la fracción no comprometida de las células madre hematopoyéticas. El valor hallado de CD34+ por CFM fue 1,00% (valor de referencia: menor a 0,10%).
En la biopsia de MO con CD34 se evidenció un 1% de elementos mononucleares. Con la técnica de Gomori se observó un incremento de la trama reticular con entrecruzamiento de fibras gruesas, constituyendo signos de mielofibrosis grado 2 (MF2) (Figura 4).
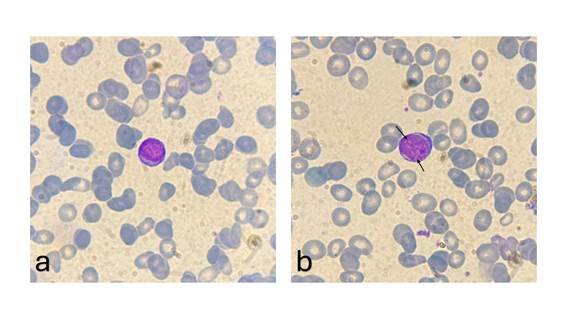
Figura 1. Morfológicamente se observan células con alta relación
núcleo/citoplasma, con cromatina laxa, nucleolo inconspicuo (a) versus
nucleolos evidentes (b: flechas), refuerzo basófilo de la membrana
citoplasmática, y ausencia de gránulos. May-Grünwald Giemsa x100.
Figura 2. Extendido de sangre periférica donde se observa anisopoiquilocitosis, dacriocitos (flechas negras) y eritroblasto circulante (flecha azul). May-Grünwald Giemsa x100.
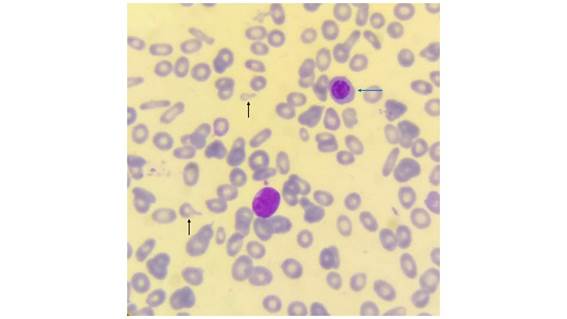
Figura 3. Los gráficos de puntos muestran células madre CD34+ (puntos rojos) con fenotipo de célula precursora hematopoyética no comprometida: CD34+, CD117+, HLA-DR+, CD38(negativo a positivo débil), CD33+débil, CD13+débil. También se muestran neutrófilos (puntos grises), monocitos (puntos amarillos) y linfocitos (puntos verdes).
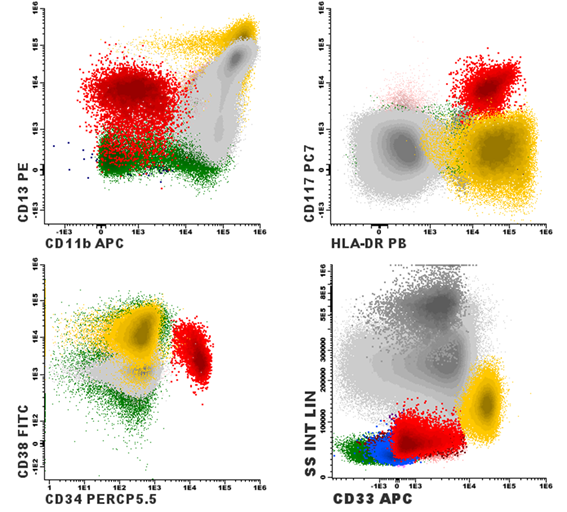
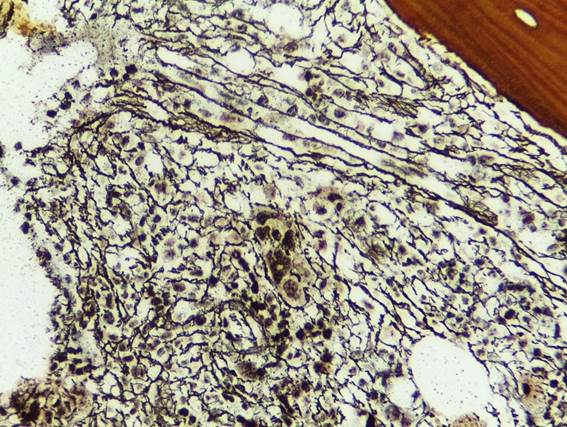
Figura 4. Fibrosis reticulínica con entrecruzamiento de fibras gruesas y finas a nivel intersticial (MF-2: mielofibrosis grado 2) (Técnica de Gomori x400).
Conclusión
Las CPH de SP pueden encontrarse aumentadas bajo ciertas condiciones, como ocurre en la MFP. Estas CPH movilizadas, en su mayoría no comprometidas a ninguna línea celular, son la base para inducir hematopoyesis extramedular.
Bibliografía
1. Orfao A, Matarraz S, Pérez-Andrés M et al. Immunophenotypic dissection of normal hematopoiesis. J Immunol Methods. 2019;475:112684. doi:10.1016/j.jim.2019.112684
2. Yang X, Chen D, Long H, Zhu B. The mechanisms of pathological extramedullary hematopoiesis in diseases. Cell Mol Life Sci. 2020;77(14):2723-2738. doi:10.1007/s00018-020-03450-w
3. Khalil S, Ariel Gru A, Saavedra AP. Cutaneous extramedullary haematopoiesis: Implications in human disease and treatment. Exp Dermatol. 2019;28(11):1201-1209. doi:10.1111/exd.14013