Linfoma B difuso de células grandes asociado a KSHV/HHV8 con áreas focales de enfermedad de Castleman multicéntrico: reporte de un caso inusual y revisión de la literatura
Difuse large B-cell lymphoma associated with KSHV/HHV8 with focal areas of multicentric Castleman disease: report of an unusual case and literature review
Mario Alberto Caviedes Cleves1, Dilia Rosa Díaz2, Vanessa Santiago Pacheco3.
1. Residente de Patología, Universidad de Antioquia, Medellín.
ORCID: https://orcid.org/0000-0002-4783-2774
2. Docente de Patología, Universidad de Antioquia Medellín.
ORCID: https://orcid.org/0000-0003-3913-1983
3. Docente de Hematopatología, Universidad de Antioquia Medellín.
ORCID: https://orcid.org/0000-0002-2912-1688
Mail de contacto: mcaviedes115@gmail.com
Palabras clave: Herpesvirus Humano 8,
VIH,
trastornos linfoproliferativos,
linfoma plasmablástico,
enfermedad de Castleman.
Keywords: Herpesvirus 8, Human,
HIV,
lymphoproliferative disorders,
plasmablastic lymphoma,
Castleman disease.
Resumen
Las lesiones linfoproliferativas de aspecto plasmablástico/plasmocitoide asociadas a KSHV/HHV8 en pacientes con infección por virus de la inmunodeficiencia humana (VIH) más frecuentemente encontradas incluyen la enfermedad de Castleman multicéntrica (ECM), el linfoma B difuso de células grandes asociado a KSHV/HHV8 (LBDCG KSHV/HHV8+), el linfoma primario de cavidades, el linfoma primario de cavidades extracavitario y el más recientemente descrito síndrome inflamatorio de citoquinas asociado al KSHV/HHV8 (KICS). Más que entidades separadas, se las considera un espectro de manifestaciones clínicas asociadas a la infección por KSHV/HHV8. Los pacientes con sarcoma de Kaposi tienen mayor riesgo de desarrollar ECM, y a su vez éstos, cuando se acompañan de agregados plasmablásticos, tienen mayor probabilidad de progresar a linfoma franco asociado a KSHV/HHV8. Se presenta el caso de un paciente masculino de 42 años, con VIH/SIDA y sarcoma de Kaposi en quien posteriormente se evidenció histopatológicamente áreas de ECM con LBDCG KSHV/HHV8+. Adicionalmente, se hace una revisión de la literatura del diagnóstico diferencial de este espectro de entidades.
Abstract
Lymphoproliferative lesions with plasmablastic/plasmacytoid appearance associated with KSHV/HHV8 in HIV patients most frequently found include multicentric Castleman disease (MCD), KSHV/HHV8-associated diffuse large B-cell lymphoma (KSHV/HHV8+ DLBCL), primary effusion lymphoma, extracavitary primary effusion lymphoma, and more recently described, the KSHV inflammatory cytokine syndrome (KICS). These, more than separate entities, are considered a spectrum of clinical manifestations associated with KSHV/HHV8 infection. Patients with Kaposi's sarcoma are at higher risk of developing MCD and, in turn, those with plasmablastic aggregates are more likely to progress to frank lymphoma associated with KSHV/HHV8. We present the clinical case of a 42-year-old male patient with HIV/AIDS and Kaposi's sarcoma who was later found to have histopathologically proven areas of MCD with KSHV/HHV8+ DLBCL. Additionally, a literature review of the differential diagnosis of this spectrum of entities is provided.
Introducción
Las lesiones linfoproliferativas de aspecto plasmablástico/plasmocitoide asociadas a KSHV/HHV8 en el contexto de pacientes con VIH, requieren una investigación exhaustiva que incluya la historia clínica, estudios de laboratorio y el control virológico, además de estudios morfológicos, inmunofenotípicos y, en algunos casos, genéticos como parte de su evaluación(1,2). Las entidades más frecuentemente asociadas incluyen ECM, LBDCG KSHV/HHV8+, el linfoma primario de cavidades, el linfoma primario de cavidades extracavitario(3,4), y más recientemente descrito, el KICS(5,6).
La enfermedad de Castleman multicéntrica asociada a KSHV/HHV8 es un trastorno linfoproliferativo observado con frecuencia en pacientes infectados por VIH (89%)(7) y se caracteriza por la presencia de centros germinales en regresión, con proliferación de linfocitos y células plasmáticas paracorticales e interfoliculares politípicas(1), con presencia de plasmablastos en zonas inter y perifoliculares infectados por KSHV/HHV8(8), con expresión de IgM lambda citoplasmática monotípica por inmunohistoquímica, pero sin evidencia de monoclonalidad en estudios moleculares. El LBDCG KSHV/HHV8+ es una entidad muy rara y agresiva que surge generalmente en un contexto de ECM KSHV/HHV8+(9), generalmente en pacientes VIH positivos con inmunosupresión profunda(7), que histopatológicamente se caracteriza por láminas y grupos confluentes de plasmablastos, con borramiento de la arquitectura del ganglio linfático, y que generalmente son monotípicos con restricción de cadenas lambda(8), con positividad variable para antígenos de células B, y negatividad para marcadores de células plasmáticas y para VEB(1). El linfoma primario de cavidades extracavitario es una entidad observada preferentemente en personas con VIH+/SIDA(10), por definición es positiva para KSHV/HHV8 y en el 75% de los casos también son positivas para VEB por EBER(11). Histopatológicamente las células neoplásicas son de aspecto plasmablástico, inmunoblástico o anaplásico(12), con marcación variable para antígenos de células B, positividad para marcadores de diferenciación de células B terminales, y a diferencia del LBDCG KSHV/HHV8+, son positivos para CD138 y CD38(7).
Presentamos el caso clínico de un paciente de la quinta década de la vida con VIH/SIDA y sarcoma de Kaposi, quien consultó por linfadenopatías generalizadas y síntomas B, cuyo diagnóstico histopatológico fue un LBDCG KSHV/HHV8+, con evidencia en áreas focales de enfermedad de Castleman multicéntrica, lo cual representa el espectro morfológico e inmunofenotípico de las entidades asociadas a la infección por el KSHV/HHV8. Aportamos a la literatura mundial con este caso representativo del diagnóstico diferencial de dichas entidades.
Caso clínico
Paciente masculino de 42 años de edad, con diagnósticos desde 3 años antes del ingreso de infección VIH y síndrome de la inmunodeficiencia adquirida (SIDA) por sarcoma de Kaposi e infección por virus del papiloma anal con lesión intraepitelial escamosa de alto grado, que se encontraba en manejo con terapia antirretroviral de alta eficacia (HAART) con tenofovir disoproxil fumarato (TDF), emtricitabina (FTC) y efavirenz (EFV) logrando recuento de linfocitos T CD4+ de 395 células /mm3, y carga viral indetectable. Ingresó por cuadro clínico de 3 meses de evolución consistente en poliserositis, adenopatías generalizadas, pérdida involuntaria de 5 kilogramos de peso y diaforesis nocturna.
En los exámenes de laboratorio, hemograma con anemia leve, LDH elevada, electrolitos normales y tiempos de coagulación normales. Ante la sospecha de tuberculosis diseminada versus trastorno linfoproliferativo, se realizó resección de ganglio axilar derecho, obteniendo un nódulo de 3x2x1 cm, con superficie rugosa color café y parénquima homogéneo de aspecto violáceo. El examen histopatológico evidenció folículos linfoides pequeños con centros germinales residuales, con expansión de la paracorteza dada la proliferación de células de tamaño grande, pleomórficas e hipercromáticas y de vasos sanguíneos con células endoteliales de morfología atípica. Se realizaron marcadores de inmunohistoquímica que reportó células atípicas positivas para HHV8/LANA1, CD31, con Ki67 del 90%, y negativas para los marcadores CD20, CD3, CD30, citoqueratina, proteína S-100 y CD38. Las tinciones especiales para Ziehl Neelsen, Ziehl Neelsen modificado, plata metenamina y mucicarmín fueron negativos para microorganismos. Se concluyó que los hallazgos eran consistentes con sarcoma de Kaposi (Figura 1).
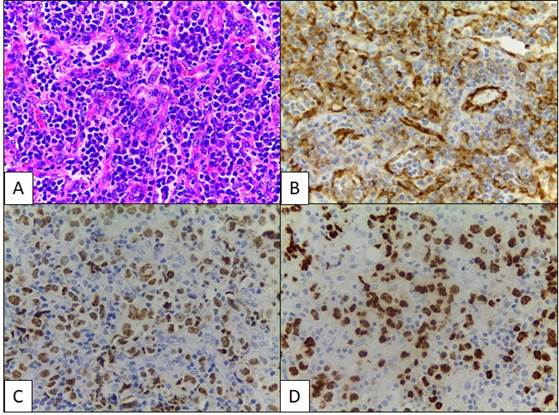
Figura 1. Sarcoma de Kaposi: A) paracorteza con proliferación de células de tamaño grande y pleomórficas, y células endoteliales morfología atípica (H&E, aumento 40X). Las células atípicas fueron positivas para CD31 (B), HHV8/LANA1 (C), KI67 (D). Cortesía: Departamento de Patología de la Universidad de Antioquia.
Sin embargo, ante los síntomas clínicos, y la alta sospecha de enfermedad linfoproliferativa, se decidió realizar resección de nuevo ganglio linfático cervical derecho. En el Servicio de Patología se recibieron 2 ganglios linfáticos, el mayor de 1.3 x 0.8 cm, color crema. Al examen histopatológico, se observó distorsión de la arquitectura ganglionar con algunos folículos linfoides con centro germinal redondo agotado e hiperplasia concéntrica de la zona del manto, con áreas de la paracorteza expandidas por la presencia de abundantes células plasmáticas, además de proliferación vascular prominente. Dichos hallazgos correspondían a enfermedad de Castleman variante plasmacelular (Figura 2). En otras áreas, se identificaron agregados confluentes y láminas de células atípicas de gran tamaño, pleomórficas, binucleadas y multinucleadas con nucléolo prominente, de aspecto plasmablástico con alta actividad mitótica, las cuáles infiltraban algunos folículos linfoides, con borramiento de la arquitectura nodal, y con extensión a la cápsula ganglionar y al tejido blando perinodal. Se realizaron tinciones especiales con Ziehl Neelsen y plata metenamina que fueron negativas para microorganismos. Las células atípicas fueron fuertemente positivas para los marcadores de inmunohistoquímica MUM-1, C-MYC y HHV8/LANA1; débilmente positivas para CD20 y CD38, y negativas para CD3, CD30, CD138, LMP-1, CD31, CD34, CD79a, PAX-5, CD23, CD10, BCL2 y BCL6. El índice de proliferación medido por Ki67 fue del 90%, y presentaban restricción de cadenas lambda (Figura 3). No se realizó hibridación in-situ para el virus de Epstein-Barr (EBER-CISH) por no disponibilidad del recurso. Los hallazgos favorecían el diagnóstico de LBDCG KSHV/HHV8+. El paciente presentó deterioro progresivo de su patrón respiratorio, con inestabilidad hemodinámica y finalmente falleció.
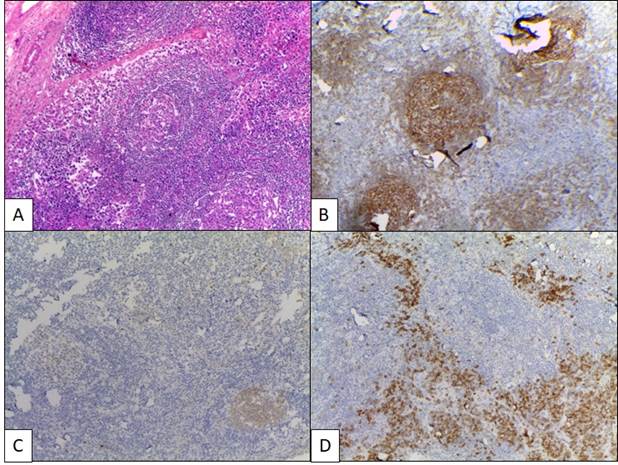
Figura 2. Enfermedad de Castleman multicéntrica. A) Áreas focales con folículos linfoides con centro germinal redondo agotado, con hiperplasia concéntrica de la zona del manto en aspecto de piel de cebolla; hay agregados plasmablásticos en zona interfolicular (H&E, aumento 10x). B) CD23 positivo en la malla de células dendríticas foliculares. C) CD10 débilmente positivo en centros germinales residuales agotados. D) CD138 positivo en células plasmáticas interfoliculares. Cortesía: Departamento de Patología de la Universidad de Antioquia.
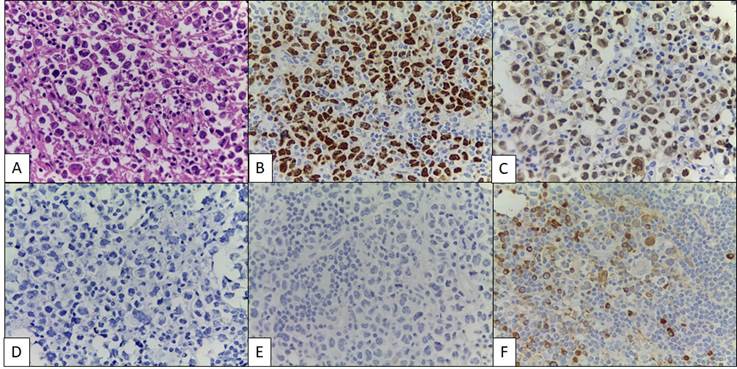
Figura 3. Linfoma B difuso de célula grade asociado a KSHV/HHV8. A) Agregados y láminas de células atípicas de gran tamaño, pleomórficas, binucleadas y multinucleadas con nucléolo prominente, de aspecto plasmablástico, con borramiento de la arquitectura nodal (H&E, aumento 40x). Las células neoplásicas fueron positivas por inmunohistoquímica para HHV8/LANA1 (A), MUM-1 (B), y negativas para CD138 (D), con restricción de cadenas ligeras IgM/lambda (F), negativas para IgM/Kappa (E). Cortesía: Departamento de Patología de la Universidad de Antioquia.
Discusión
Las lesiones linfoproliferativas de aspecto plasmablástico/plasmocitoide son difíciles de separar basándose únicamente en la morfología, lo cual resalta la necesidad de realizar una investigación exhaustiva de estos pacientes que incluya la historia clínica, estudios de laboratorio y estado viral, además de estudios morfológicos, inmunofenotípicos y en algunos casos genéticos como parte de su evaluación. Dichas lesiones en el contexto de pacientes inmunodeficientes incluyen el linfoma plasmablástico, plasmocitoma, mieloma múltiple, leucemia de células plasmáticas, proliferaciones linfoides positivas para KSHV/HHV8, entre otras(1,2).
Los trastornos linfoproliferativos relacionados con KSHV/HHV8 en pacientes con VIH incluyen ECM, LBDCG KSHV/HHV8+, el linfoma primario de cavidades, el linfoma primario de cavidades extracavitario(3,4) y más recientemente se describió el KICS(5,6) (Tabla 1). El trastorno linfoproliferativo germinotrópico ocurre preferentemente en pacientes inmunocompetentes(9). Algunas de estas lesiones, además de estar asociadas al HHV8, también son positivas para el virus de Epstein-Barr (VEB). El virus KSHV/HHV8 puede infectar células B vírgenes (CD19+, CD20+, IgM+, IgD+, CD27-) o células B de memoria IgM (CD19+, CD20+, IgM+, IgD +/-, CD27+). Las células con infección latente bajo la influencia de la IL-6 y otros factores virales tienen la capacidad de transformarse en células B con una apariencia plasmablástica con expresión de inmunoglobulina intracelular y de superficie(1).
Tabla 1. Trastornos linfoproliferativos relacionados con KSHV/HHV8 en pacientes con infección por VIH.
|
Características clínico-patológicas |
Enfermedad |
|||
|
Enfermedad de Castleman multicéntrica |
Linfoma B difuso de células grandes asociado a KSHV/HHV8 |
Linfoma primario de cavidades/extracavitario |
Síndrome inflamatorio de citoquinas asociado al KSHV/HHV8 |
|
|
Manifestaciones clínicas |
Síntomas constitucionales con linfadenopatías generalizadas en más de 2 estaciones ganglionares. |
Enfermedad extremadamente agresiva con mal pronóstico con compromiso ganglionar y extraganglionar. Generalmente surge en el contexto de una ECM KSHV/HHV8 +. |
Enfermedad grave con muy mal pronóstico. Compromiso primario de cavidades con formación de derrames, o como masa sólida extracavitaria. El 50% pueden estar asociados a sarcoma de Kaposi o ECM. |
Enfermedad sistémica clínicamente grave en personas con VIH con otras enfermedades relacionadas con KSHV/HHV8 diferentes ECM. |
|
Histopatología |
Centros germinales en regresión con proliferación de células plasmáticas paracorticales e interfoliculares. Hialinización y/o proliferación vascular prominente. |
Borramiento de arquitectura ganglionar por proliferación difusa de plasmablastos. Es frecuente encontrar áreas de ECM. |
Proliferación difusa de células de aspecto plasmablástico, inmunoblástico o anaplásico. |
Sin características histopatológicas específicas. |
|
Inmuno-histoquímica |
Células plasmáticas CD138 positivas sin restricción de cadenas ligeras de Ig. Plasmablastos dispersos en zona interfolicular positivos para MUM-1 y HHV8/LANA1; con positividad variable para antígenos de células B y negativos para CD138. |
Células neoplásicas con positividad para MUM-1, positividad variable para antígenos de células B, negativos para CD30, CD38 y CD138, con restricción de cadenas ligeras lambda. |
Células neoplásicas positivas para MUM-1, CD30, EMA, CD38 y CD138; y con positividad variable para antígenos de células B. |
No aplica. |
|
Coinfección con virus del Epstein Bar. |
No. |
No. |
EBER positivo en el 75%. |
No. |
|
Estudios moleculares de clonalidad |
Policlonal. |
Monoclonal. |
Monoclonal |
No aplica. |
La enfermedad de Castleman es un síndrome clinicopatológico, con diferentes variantes morfológicas (hialina vascular, de células plasmáticas/plasmablásticas y mixtas o transicionales), y clínicas (unicéntrica y multicéntrica). ECM se asocia con síntomas constitucionales y linfadenopatías generalizadas, y usualmente exhibe las características morfológicas de la variante de células plasmáticas(1). Su clasificación de acuerdo con el estado KSHV/HHV8+ es clínicamente más relevante. ECM KSHV/HHV8 negativa (idiopática) puede tener gran variedad de etiologías. La ECM asociada al KSHV/HHV8 es actualmente considerada por la Organización Mundial de la Salud como un trastorno linfoproliferativo que se observa comúnmente en pacientes infectados por VIH (89% de los casos), y afecta con mayor frecuencia a los ganglios linfáticos axilares, abdominales, pélvicos, mediastínicos y cervicales, y al bazo (7). Macroscópicamente, por definición los ganglios linfáticos deben tener > 10 mm de diámetro con > 2 estaciones afectadas (13). Histopatológicamente se caracteriza por proliferación de linfocitos, células plasmáticas y vasos sanguíneos, exhibiendo folículos linfoides en regresión, con diferentes grados de hialinización, proliferación vascular prominente, proliferación difusa de células plasmáticas paracorticales e interfoliculares, positivas para CD138 y sin restricción de cadenas Kappa/lambda (1). Hay presencia de plasmablastos en zonas inter y perifoliculares, los cuales están infectados por el HHV8 (8). El análisis inmunofenotípico de esta entidad mostrará que los plasmablastos son positivos para HHV8/LANA1, MUM-1, PAX-5, el 33-50% positivos para CD20 y/o CD79a, y negativas para CD138, CD10 y BCL6; y con expresión IgM lambda citoplasmática monotípica por inmunohistoquímica, pero sin evidencia de monoclonalidad en estudios moleculares(7). El CD21 y CD23 resaltan la malla de células dendríticas foliculares. Es frecuente encontrar focos de sarcoma de Kaposi en la misma muestra(7). Característica que estaba presente en nuestro paciente.
La ECM con agregados plasmablásticos, se refiere a un estado más avanzado de la enfermedad, donde los plasmablastos aumentan en número y confluyen formando agregados de tamaño variable por dentro y por fuera de los centros germinales, los cuales son positivos para HHV8, y por inmunohistoquímica presentan restricción de cadenas lambda. Sin embargo, por PCR son células policlonales u oligoclonales con genes de inmunoglobulina no mutados. A diferencia del LCBD HHV8+, no hay formación de láminas de estas células atípicas, y hay mínimo borramiento de la arquitectura del ganglio linfático. La positividad para C-MYC indica clonalidad y podría presagiar una progresión a linfoma franco(1).
El LBDCG KSHV/HHV8+, es una entidad muy rara extremadamente agresiva con una supervivencia de pocos meses(14), que surge generalmente en un contexto de ECM KSHV/HHV8+(9), generalmente en pacientes VIH positivos con inmunosupresión profunda(7). Puede comprometer ganglios linfáticos, bazo e incluso diseminarse a sitios extraganglionares con compromiso de sangre periférica. Histopatológicamente se caracteriza por láminas y grupos confluentes de plasmablastos con borramiento de la arquitectura del ganglio linfático, los cuales son monoclonales con restricción de cadenas ligeras, generalmente lambda(8). Tienen positividad variable para marcadores B como CD20 y CD79a, expresan marcadores de diferenciación de células B terminales como MUM-1, pero carecen de marcadores de activación como CD30(7), y a menudo son negativas para marcadores de células plasmáticas como CD138 y CD38(10). Son negativas para VEB(1). La positividad es variable para marcadores como CD45 y CD20. Suele ser negativo para EBER, pero se han reportado casos con doble positividad para HHV8 y VEB(15). Los hallazgos descritos son concordantes con los encontrados en nuestro caso.
El linfoma primario de cavidades extracavitario es una entidad observada preferentemente en personas con VIH+/SIDA(16), y por definición son positivas para KSVH/HHV8, y en el 75% de los casos que están asociados a VIH también son positivas para VEB(11). Ocurre principalmente en forma de masa sólida sin formación de derrames(17), involucrando ganglios linfáticos o sitios extraganglionares como tracto gastrointestinal, pulmones, piel, sistema nervioso central de localización intravascular(18). Histopatológicamente, las células neoplásicas son de aspecto plasmablástico, inmunoblástico o anaplásico, pueden tener una apariencia similar a las células tipo Hodgkin o Reed-Sternberg(12). En el linfoma primario de cavidades, las células neoplásicas por inmunohistoquímica carecen de marcadores B (CD19, CD20, PAX-5, OCT2, BOB.1, CD79a)(19) y de marcadores de centro germinal (CD10, BCL6). Pueden incluso carecer de CD45, pudiéndose diagnosticar erróneamente como otros tumores(17). Sin embargo, se componen de células B clonales basadas en el análisis de ADN(20). En la forma extracavitaria expresan con mayor frecuencia antígenos asociados a células B(17). Expresan marcadores de diferenciación de células B terminales como MUM-1, Blimp1 (como ECM), CD138 y CD38 (en contraste con los plasmablastos de la ECM)(7). Generalmente son positivos para EMA y CD30. Se ha reportado casos con marcación aberrante para antígenos de células T en el 30% de los casos(21). Se ha descrito que otras entidades asociadas a HHV8 como sarcoma de Kaposi y ECM pueden estar presentes en el 50% de los casos al momento de su presentación. El VEB se demuestra por EBER, pero no por inmunohistoquímica para LPM-1(7).
KICS es un trastorno grave y poco común, asociado a infección por KSHV/HHV8, que se presenta principalmente en personas infectadas por VIH, caracterizado por síntomas sistémicos como fiebre, trastornos gastrointestinales, edema, síntomas respiratorios, derrames, anemia, hipoalbuminemia y trombocitopenia entre otros, y que se asocia con otras enfermedades subyacentes relacionadas con KSHV/HHV8 diferentes de ECM, como sarcoma de Kaposi y linfoma de efusión primaria. El mecanismo fisiopatológico, aunque no está claro, se cree que ocurre por una sobreproducción de IL-6 e IL-10, similar a lo que ocurren en ECM. El diagnóstico se basa netamente en criterios clínicos, ya que, a diferencia de otras neoplasias malignas relacionadas con KSHV/HHV8, aún no se han descrito las características histopatológicas específicas. Clínicamente puede superponerse con ECM o shock séptico, por lo cual se deben descartar estas dos últimas entidades antes de hacer un diagnóstico de KICS(5,6). En nuestro paciente había evidencia de ECM, por lo cual se descartó este síndrome.
En conclusión, nuestro caso representa el espectro morfológico de las entidades clínicas asociadas a la infección por HHV8 desde el sarcoma de Kaposi hasta el linfoma B difuso de células grandes asociado a HVSK/HHV8, dejando en claro que el diagnóstico no es fácil dado el solapamiento clínico, morfológico, inmunofenotípico, viral y molecular entre estas patologías. En nuestro caso, la evidencia de sarcoma de Kaposi y enfermedad de Castleman multicéntrica, junto con la restricción monotípica IgM/lambda en las células neoplásicas favorece el diagnóstico de LBDCG HVSK/HHV8. Se debe tener en cuenta que la distinción con el linfoma primario de cavidades extracavitario es un gran desafío y es muy útil la realización de EBER-CISH, sin embargo, el acceso a dicha prueba diagnóstico en nuestro medio es difícil. Consideramos este caso académicamente muy representativo del diagnóstico diferencial de dichas entidades.
Bibliografía
1. Chadburn A, Said J, Gratzinger D, Chan JKC, de Jong D, Jaffe ES et al. HHV8/KSHV-Positive Lymphoproliferative Disorders and the Spectrum of Plasmablastic and Plasma Cell Neoplasms: 2015 SH/EAHP Workshop Report—Part 3. Am J Clin Pathol. 2017;147(2):171-87.
2. Ramla S, Guy J. An unusual posttransplant EBV-associated lymphoproliferative disorder exhibiting plasmacytic features in leukemic phase. Blood. 2015;125(10):1672.
3. Carbone A, Cesarman E, Spina M, Gloghini A, Schulz TF. HIV-associated lymphomas and gamma-herpesviruses. Blood. 2009;113(6):1213-24.
4. Natkunam Y, Gratzinger D, Chadburn A, Goodlad JR, Chan JKC, Said J et al. Immunodeficiency-associated lymphoproliferative disorders: time for reappraisal? Blood. 2018;132(18):1871-8.
5. Polizzotto MN, Uldrick TS, Wyvill KM, Aleman K, Marshall V, Wang V et al. Clinical Features and Outcomes of Patients With Symptomatic Kaposi Sarcoma Herpesvirus (KSHV)-associated Inflammation: Prospective Characterization of KSHV Inflammatory Cytokine Syndrome (KICS). Clin Infect Dis Off Publ Infect Dis Soc Am. 2016;62(6):730-8.
6. Piñeiro F, Climent F, Imaz A, Gudiol C, Niubó J, Palomar-Muñoz A et al. Clinical and pathological features of Kaposi sarcoma herpesvirus-associated inflammatory cytokine syndrome. AIDS Lond Engl. 2020;34(14):2097-101.
7. Alaggio R, Amador C, Anagnostopoulos I, Attygalle AD, Araujo IB de O, Berti E et al. The 5th edition of the World Health Organization Classification of Haematolymphoid Tumours: Lymphoid Neoplasms. Leukemia. 2022;36(7):1720-48.
8. Dupin N, Diss TL, Kellam P, Tulliez M, Du MQ, Sicard D et al. HHV-8 is associated with a plasmablastic variant of Castleman disease that is linked to HHV-8-positive plasmablastic lymphoma. Blood. 2000;95(4):1406-12.
9. Du MQ, Diss TC, Liu H, Ye H, Hamoudi RA, Cabeçadas J et al. KSHV- and EBV-associated germinotropic lymphoproliferative disorder. Blood. 2002;100(9):3415-8.
10. Oksenhendler E, Boulanger E, Galicier L, Du MQ, Dupin N, Diss TC et al. High incidence of Kaposi sarcoma-associated herpesvirus-related non-Hodgkin lymphoma in patients with HIV infection and multicentric Castleman disease. Blood. 2002;99(7):2331-6.
11. Pan ZG, Zhang QY, Lu ZB (Jim), Quinto T, Rozenvald IB, Liu LT et al. Extracavitary KSHV-associated Large B-Cell Lymphoma: A Distinct Entity or a Subtype of Primary Effusion Lymphoma? Study of 9 Cases and Review of an Additional 43 Cases. Am J Surg Pathol. 2012;36(8):1129.
12. Brimo F, Michel RP, Khetani K, Auger M. Primary effusion lymphoma. Cancer Cytopathol. 2007;111(4):224-33.
13. Fajgenbaum DC, Uldrick TS, Bagg A, Frank D, Wu D, Srkalovic G et al. International, evidence-based consensus diagnostic criteria for HHV-8-negative/idiopathic multicentric Castleman disease. Blood. 2017;129(12):1646-57.
14. Ramaswami R, Lurain K, Polizzotto MN, Ekwede I, Waldon K, Steinberg SM et al. Characteristics and outcomes of KSHV-associated multicentric Castleman disease with or without other KSHV diseases. Blood Adv. 2021;5(6):1660-70
15. Gonzalez-Farre B, Martinez D, Lopez-Guerra M, Xipell M, Monclus E, Rovira J et al. HHV8-related lymphoid proliferations: a broad spectrum of lesions from reactive lymphoid hyperplasia to overt lymphoma. Mod Pathol. 2017;30(5):745-60.
16. Nador R, Cesarman E, Chadburn A, Dawson D, Ansari M, Sald J et al. Primary effusion lymphoma: a distinct clinicopathologic entity associated with the Kaposi’s sarcoma-associated herpes virus. Blood. 1996;88(2):645-56
17. Chadburn A, Hyjek E, Mathew S, Cesarman E, Said J, Knowles DM. KSHV-Positive Solid Lymphomas Represent an Extra-Cavitary Variant of Primary Effusion Lymphoma. Am J Surg Pathol. 2004;28(11):1401.
18. Bruce-Brand C, Rigby J. Kaposi sarcoma with intravascular primary effusion lymphoma in the skin: A potential pitfall in HHV8 immunohistochemistry interpretation. Int J Surg Pathol [Internet]. 2020;28(8):868-71.
19. Knowles D, Inghirami G, Ubriaco A, Dalla-Favera R. Molecular genetic analysis of three AIDS-associated neoplasms of uncertain lineage demonstrates their B-cell derivation and the possible pathogenetic role of the Epstein-Barr virus. Blood. 1989;73(3):792-9
20. Walts AE, Shintaku P, Said JW. Diagnosis of Malignant Lymphoma in Effusions from Patients with AIDS by Gene Rearrangement. Am J Clin Pathol. 1990;94(2):170-5.
21. Said JW, Shintaku IP, Asou H, deVos S, Baker J, Hanson G et al. Herpesvirus 8 Inclusions in Primary Effusion Lymphoma: Report of a Unique Case With T-Cell Phenotype. Arch Pathol Lab Med. 1999;123(3):257-60.