Presentación Atípica de Leucemia Linfoblastica Aguda de tipo B en Adulto Joven sin expresión en sangre periférica
Atypical Presentation of Acute Lymphoblastic Leukemia type B in a Young Adult without expression in peripheral blood
Fabra Martinez M., Patiño R., Enciso C., Rivas N.
Servicio de Hematología, Hospital HIGA L.C de Gandulfo, Lomas de Zamora, Bs.As., Argentina.
Palabras Claves: leucemia linfoblástica aguda, adultos jóvenes, presentación atípica de leucemia linfoblástica aguda, lesiones osteolíticas.
Key words: acute lymphoblastic leukemia, Young adults, atypical acute lymphoblastic leukemia, osteolytic lesions.
Resumen
La leucemia linfoblástica aguda B (LLA B) es una patología con distribución bimodal con un primer pico en pacientes menores de 20 años y el segundo a partir de los 45 años de edad (1). Representa el 75-80% de las leucemias agudas en pediatría, principalmente con afectación medular aunque puede presentar compromiso extramedular.
La presentación de LLA B sin presencia de blastos en sangre periférica tiene una incidencia de 15% en adolescentes y adultos jóvenes (AYA) (2), y la afectación extramedular al diagnóstico con lesiones óseas osteolíticas e hipercalcemia es infrecuente, por lo que puede retrasar su diagnóstico.
Se presenta el caso de un paciente de 38 años quien presentó como única manifestación de LLA B al diagnóstico, lesiones osteolíticas con compromiso de calota, esqueleto axial y ambas caderas asociado a hipercalcemia e insuficiencia renal aguda en ausencia de blastos linfoides B en sangre periférica.
Abstract
B acute lymphoblastic leukemia (B-ALL) is a pathology with bimodal distribution with a first peak in patients under 20 years of age and the second after 45 years of age (1). It represents 75-80% of acute leukemias in pediatrics, mainly with spinal cord involvement, although it may present extramedullary involvement.
The presentation of ALL B without the presence of blasts in peripheral blood has an incidence of 15% in adolescents and young adult (AYA) (2), and extramedullary involvement at diagnosis with osteolytic bone lesions and hypercalcemia is rare, so it can delay your diagnosis.
The case of a 38-year-old patient who presented as the only manifestation of ALL B at first, osteolytic lesions with compromise of the skull, axial skeleton and both hips is presented associated with hypercalcemia and acute renal failure in the absence of B lymphoid blasts in peripheral blood.
Introducción
La leucemia linfoblástica aguda (LLA) es la leucemia más frecuente en la infancia, constituyendo el 75-80% de todas las leucemias agudas de la edad pediátrica, el 19% de todos los tumores en adolescentes de entre 15 y 19 años, y representa el 15% de las leucemias en adultos (2).
Se caracteriza por una alta tasa de proliferación de precursores linfoides atípicos con alteraciones citogenéticas y moleculares con gran implicancia en el pronóstico y evolución de la enfermedad.
Su expresión clínica es variable, pudiendo manifestarse con astenia, disnea y pérdida de peso, sangrados, fiebre o infecciones recurrentes y síntomas secundarios a la infiltración de órganos por células neoplásicas como anemia, trombocitopenia, leucopenia, organomegalia e infrecuentemente dolor óseo.
El compromiso óseo está descripto en el 23% de los niños y en menos del 4% de los adultos, siendo las lesiones óseas en algunos casos la única manifestación de la enfermedad (3).
Se presenta el caso de un adulto joven con diagnóstico de LLA-B que debuta con dolores óseos, lesiones osteolíticas, hipercalcemia y falla renal aguda, sin presencia de blastos en sangre periférica.
Caso
Paciente de sexo masculino de 38 años de edad, sin antecedentes patológicos relevantes, oriundo de la Provincia de Buenos Aires; ingresa a nuestro centro refiriendo dolores óseos generalizados a predominio de región lumbosacra con limitación para deambular. Al examen físico se detecta esplenomegalia de 150 mm por ecografía.
Laboratorio al ingreso: GB: 37.33 K/uL: neutrófilos 63%, eosinófilos 1.3%, basófilos 0.5%, linfocitos 16.2%, monocitos 4.9%, Plaquetas: 87.000/uL, Calcio sérico: 14.4 mg/dL, Creatinina: 5.4 mg/dL.
Se realizó frotis de sangre periférica observándose leucocitosis con neutrofilia, sin presencia de formas inmaduras ni blastos, y plaquetopenia moderada.
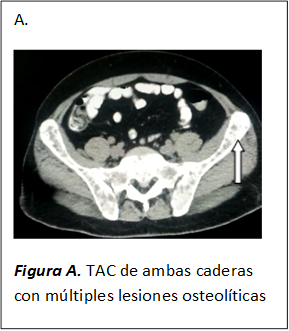
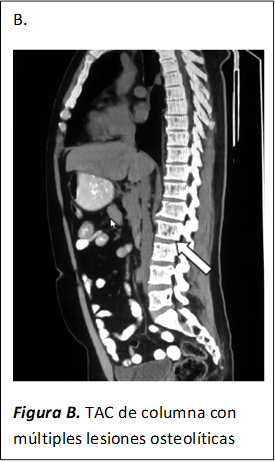
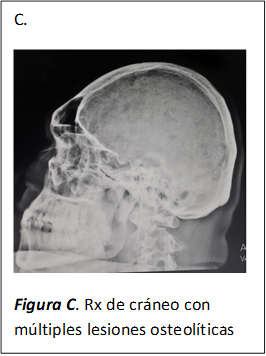
En la Tomografía computada se observaron múltiples imágenes osteolíticas a nivel de calota, esqueleto axial, sacro, cresta ilíacas sin evidencia de masas tumorales. (Figuras A, B, C)
Otros estudios realizados: colagenograma normal, PTH elevada (375 pg/ml), serologías virales negativas (CMV, VEB, HIV, VDRL, VHB, VHC), proteinograma electroforético normal, hormona paratiroidea normal, marcadores tumorales normales (Ca 19-9, CEA, betahCG), ecografía tiroidea y testicular sin particularidades.
Se plantearon como diagnósticos diferenciales: neoplasia de células plasmáticas, metástasis óseas de tumor oculto, hiperparatiroidismo y síndrome paraneoplásico.
Inició tratamiento médico de urgencia con ácido zoledrónico 4 mg y corticoides 1 mg/kg con franca mejoría de la hipercalcemia y función renal (Calcio sérico: 9.2 mg/dL, Creatinina: 0.96 mg/dL)
Se realizó punción biopsia de medula ósea con los siguientes resultados:
- Medulograma: Médula ósea normocelular para la edad, con presencia de 3 series hematopoyéticas, sin presencia de blástos ni incremento de células plasmáticas.
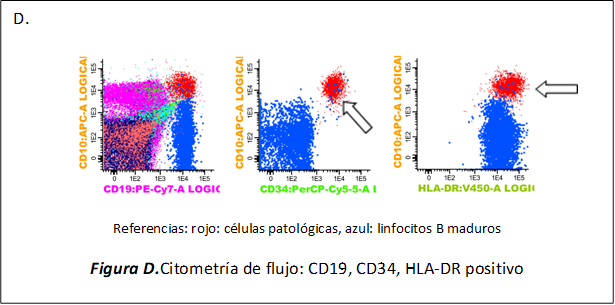
- Citometría de flujo: 1.4% de células de tamaño pequeño, CD45neg, CD34++, CD19++, CD20neg, CD10++, CD81+, HLA-DR+, CD66c+, CD15neg, CD38+débil, MPOneg, CD79a+, CD3neg, CD7neg compatibles con blastos linfoides B. (Figura D).
Se descartó contaminación de muestra con sangre periferia con toma de nueva muestra de médula ósea para evaluación por citometría de flujo que informó: 0.063% de células de tamaño pequeño, CD45neg, CD34++, CD19++, CD20neg, CD10++, CD81+, HLA-DR+, CD66c+, CD15neg, CD38+débil, MPOneg, CD79a+, CD3neg, CD7neg compatibles con blástos linfoides B.
- Anatomía patológica de medula ósea: celularidad hematopoyética 95% con 55% de células mononucleares CD34+, CD20-. Compatible con infiltración blástica.
Se solicitó PET-TC Corporal Total con FDG, el cual no llego a realizarse ya que el paciente fue derivado a un centro de mayor complejidad para inicio de tratamiento.
Conclusión
Las lesiones osteolíticas e hipercalcemia como única forma de presentación de la LLA B sin presencia de blastos en sangre periférica están descriptas en la bibliografía en aislados reportes de casos siendo más frecuentes en la población pediátrica (4).
Las lesiones óseas podrían estar subestimadas como forma de presentación inicial de la LLA B, ya que se suele hacer estudio de imágenes solo en pacientes que presentan síntomas (5).
Se han descripto dos mecanismos fisiopatológicos posibles relacionados a lesiones osteolíticas e hipercalcemia en este contexto: la interacción de las células tumorales con el microambiente medular provocaría la activación de osteoclastos; por un lado por activación directa de los osteoclastos los cuales secretan el péptido relacionado a la hormona paratiroidea (PTHrP) capaz de activar al ligando del receptor de activación del factor nuclear kappa (RANKL) y contribuiría a la hipercalcemia por unión al receptor del activador del factor nuclear kappa B (RANK) en la superficie de los precursores de los osteoclastos y por otro lado, citoquinas inflamatorias, tales como, IL-1, IL-6, TNFa podrían activar indirectamente a los osteoclastos generando un desbalance hacia la resorción con posterior hipercalcemia y fallo renal (5) (6) (7).
Debemos considerar a la LLA B dentro de los diagnósticos diferenciales ante un paciente con dolores óseos por lesiones osteolíticas, hipercalcemia e insuficiencia renal, aun en ausencia de alteraciones significativas del hemograma como citopenias o blastos en sangre periférica, a fin de llegar a un pronto diagnóstico en esta patología aguda e iniciar un adecuado tratamiento que será definitorio en la evolución de la enfermedad.
Reportamos este caso por la forma infrecuente de presentación de escasa bibliografía de una patología habitual en la práctica oncohematológica.
Dado que nuestro centro corresponde a un Hospital Público del Conurbano Bonaerense que carece de acceso a estudios de alta complejidad, hay exámenes complementarios que al momento del proceso diagnóstico no pudieron ser realizados.
Bibliografía:
1. Agriello E, Belli C, Carnelutto N y col. Leucemias Agudas, LeucemiaLinfoblastica Aguda, Guías de Diagnóstico y Tratamiento, Sociedad Argentina de Hematología, versión 2021. Pág. 383-401
2. Shaimaa EI-Ashwah, NohaEisa and col. Hypercalcemia With Disseminated Osteolytic Lesions: A Rare Presentation of Adulthood Acute Lymphoblastic Leukemia. J Hematol. 2018 Dec; 7(4): 154-157.
3. Kara M, Kelly MD. Acute Lymphoblastic Leukemia. En: Weiner MA, Cairo MS. Pediatric Hematology/Oncology Secrets. Philadelphia. Hanley and Belfus Inc. 2002; 109-14.
4. Anup Kumar Trikannad Ashwini Kumar, Sruthi Vellanki, Geetha Krishnamoorthy. Hypercalcemia As the Sole Initial Presentation of Precursor B-cell Acute Lymphoblastic Leukemia. Cereus. 2022 Feb; 14 (2): e22081.
5.Natthapon A, Attaya S. Acute lymphoblastic leukaemia with osteolytic bone lesions: diagnostic dilemma. BMJ Case Rep. 2018; 2018: bcr2018225008.
6. González S, Beccacece M, Sardu L, Avila L. Leucemia Linfoblastica Aguda: rara presentación con lesiones osteolíticas múltiples. Revista de Hematología, Sociedad Argentina de Hematología, Vol. 21 N°3: 310-316, 2017
7. Karima F, Fatima Zahra L, Illias T. Hypercalcémie maligne révélant une leucémie aiguë lymphoblastique: à propos d´un cas. Pan African Medical Journal. 2022;41 (257).