Inmunofijación: más allá de la tipificación de gammapatías monoclonales.
valor pronóstico, categorización de respuesta al tratamiento e importancia en la detección de interferencias por el uso de anticuerpos monoclonales terapéuticos y en pacientes con enfermedad Covid-19
Immunofixation: beyond the typification of monoclonal gammopathies.
Prognostic value, categorization of responses to treatments and importance in the detection of interferences by the use of therapeutic monoclonal antibodies and in patients with COVID-19 disease
Alejandre, M.E.
Laboratorio de Proteínas del Hospital de Clínicas José de San Martín. Departamento de Bioquímica Clínica, Facultad de Farmacia y Bioquímica de la Universidad de Buenos Aires. Laboratorio de Análisis Proteicos Especializados. Centro de Hematología Pavlovsky.
Palabras claves: inmunofijación,
gammapatías monoclonales,
bandas oligoclonales,
interferencias por daratumumab.
Keywords: immunofixation,
monoclonal gammopathies,
oligoclonal bands,
interference by daratumumab.
Resumen
La presencia en suero, o al menos en orina, de un componente monoclonal (CM) o sus subunidades, las cadenas livianas, como producto de la proliferación clonal de linfocitos B o células plasmáticas, caracteriza un amplio grupo de gammapatías monoclonales (GM). La principal aplicación de la inmunofijación (IFx) es la identificación inmunológica del CM en suero y orina para establecer el diagnóstico de las mismas. Además, dicho resultado tiene valor pronóstico para algunas de las GM. La IFx también permite establecer los diversos grados de respuesta al tratamiento alcanzado por los pacientes y determinar la reaparición del CM, marcando la recaída de la enfermedad.
La IFx consiste en precipitar la proteína de interés en el gel mediante la adición de antisuero monoespecífico, al finalizar el fraccionamiento electroforético de las muestras de suero u orina, sembradas en soporte de agarosa o acetato de celulosa gelatinizado. Los lavados posteriores deben ser exhaustivos para evitar visualizaciones inespecíficas. Finalmente se revela con azul brillante de Coomassie R 250 o tinción ultrasensible de plata u oro coloidal.
La aparición en suero de bandas oligoclonales durante el seguimiento de pacientes con mieloma múltiple (MM) post trasplante autólogo de células madres (TAMO) generó dificultad para evaluar el CM original. Su aparición, certificada por IFx se asoció con la ocurrencia de efectos adversos menos frecuentes a la terapia aplicada y mayores tiempos de sobrevida global y libre de enfermedad en los pacientes.
Más recientemente, los anticuerpos monoclonales terapéuticos para el tratamiento del MM también complican la evaluación de su CM. Aparecen en el proteinograma (PROT) a dosis terapéuticas y son de tipo IgG-kappa en la IFx. Dicha interferencia puede indicar falsamente un grado de respuesta deficiente a la terapia, sobre todo en aquellos casos en que el CM original es del mismo tipo inmunológico y tiene igual movilidad electroforética que el anticuerpo terapéutico.
En el seguimiento de pacientes con enfermedad COVID-19 pudo observarse la aparición de bandas homogéneas en el PROT, interfiriendo en la evaluación del CM para aquellos pacientes con diagnóstico previo de GM.
Por todo lo expuesto resulta aconsejable realizar el seguimiento de los pacientes en un mismo laboratorio de análisis clínicos, dada la necesidad de sumar al correcto procesamiento técnico de la IFx el conocimiento de los datos de la historia analítica y clínica. Esto favorece la adecuada interpretación y redacción del informe, a la vez que permite discernir en cuál de las diversas situaciones antes mencionadas se encuentran nuestros pacientes.
Abstract
The presence in serum or at least in urine of a monoclonal component (MC) or its light chain subunits, as a product of clonal proliferation of B lymphocytes or plasma cells, characterizes a large group of monoclonal gammopathies (MG). The main application of immunofixation (IFx) is the immunological identification of MC in serum and urine to establish their diagnosis. In addition, this result has prognostic value for some of the MG. IFx also makes it possible to establish the various degrees of response to treatment achieved by patients, and to determine the reappearance of MC, marking the relapse of the disease.
IFx consists of precipitating the protein of interest in the gel by adding monospecific antiserum at the end of the electrophoretic fractionation of the serum or urine samples, seeded on agarose or gelatinized cellulose acetate support. Subsequent washes must be exhaustive to avoid nonspecific visualization. Finally, it is revealed with Coomassie Brilliant Blue R 250 or ultrasensitive colloidal silver or gold stain.
The appearance of oligoclonal bands in serum during the follow-up of patients with multiple myeloma (MM), after autologous stem cell transplantation (ASCT), generated difficulty in evaluating the original MC. Its appearance, certified by IFx, was associated with the occurrence of fewer adverse effects to the applied therapy, and longer overall disease-free survival in patients.
More recently, therapeutic monoclonal antibodies for the treatment of MM also complicate the evaluation of its MC. They appear in the proteinogram (PROT) at therapeutic doses and of type IgG-kappa by IFx.
Such interference may falsely indicate a poor response to therapy, especially in those cases where the original MC is of the same immunological type and has the same electrophoretic mobility as the therapeutic antibody.
In the follow-up of patients with COVID-19 disease, the appearance of homogeneous bands in the PROT could be observed, interfering in the evaluation of their MC for those patients with a previous diagnosis of MG.
For all the above, it is advisable to follow up patients in the same clinical analysis laboratory, given the need to add to the correct technical processing of the IFx, the knowledge of the analytical and clinical history data. This favors the proper interpretation and writing of the report, while it allows us to discern in which of the various situations mentioned above our patients are included.
Abreviaturas
BO: bandas oligoclonales
CF: citometría de flujo
CM: componente monoclonal
EM: espectrometría de masa
EMR: enfermedad mínima residual
GM: gammapatía monoclonal
GMSI: gammapatía monoclonal de significado incierto
IFx: inmunofijación
IMWG: Grupo Internacional de Estudio del Mieloma
MM: mieloma múltiple
PBJ: proteína de Bence Jones
PROT: proteinograma electroforético
RC: remisión completa
sFLC: cuantificación de cadenas livianas libres en suero
TAMO: trasplante autólogo de células madre
2ME: 2-mercaptoetanol
Introducción
La presencia en suero, o al menos en orina, de una inmunoglobulina monoclonal, llamada componente monoclonal (CM) o paraproteína, o de sus subunidades, las cadenas livianas, como producto de la proliferación clonal de linfocitos B o células plasmáticas caracteriza un amplio grupo de gammapatías monoclonales (GM) con impacto clínico muy heterogéneo. Las mismas comprenden desde las mencionadas gammapatías monoclonales de significado incierto (GMSI), completamente asintomáticas y que no requieren intervención hasta el mieloma múltiple (MM) agresivo con necesidad de tratamiento inmediato(1).
El CM se visualiza en el proteinograma electroforético (PROT) como la aparición de una banda homogénea que puede migrar desde la fracción de las a2-globulinas hasta el punto de siembra, originando un pico en la densitometría electroforética posible de cuantificar. Posteriormente, la identificación inmunológica de dicha paraproteína es efectuada por la técnica de inmunofijación (IFx).
En los primeros años del siglo XXI se sumó a estos análisis proteicos especializados el ensayo de cuantificación de las cadenas livianas libres en suero (sFLC)(2). La combinación de dicha técnica con el PROT y la IFx en suero y en orina aumenta la sensibilidad y constituye el panel de cribado para el diagnóstico de GM(3).
La detección, caracterización y medición de los CM ayuda en el diagnóstico inicial de estos desórdenes a la vez que permite realizar la estratificación del riesgo de progresión de pacientes con GMSI o MM indolente o asintomático a MM u otra GM maligna relacionada(4-6). Por ejemplo, el isotipo del CM caracterizado por IFx influye en el riesgo de progresión de una GMSI, ya que se observó que individuos con CM de tipo no IgG presentan una mayor probabilidad de progresión a MM que los del tipo IgG. A su vez, dicho panel de cribado permite detectar pacientes asintomáticos con alto riesgo de progresión, que podrían beneficiarse de recibir tratamientos tempranos(7).
Por lo tanto, la inspección visual rigurosa del PROT junto a la realización posterior de la IFx y el estudio proteico en orina, especialmente cuando persiste la sospecha clínica y no hay una clara visualización del CM en la corrida electroforética, resultan imprescindibles para su pesquisa(8).
Finalmente, disponer de la información del isotipo de la paraproteína por IFx y la posición en que migra dicho CM en el PROT, es necesario cuando se hace un seguimiento de los diversos grados respuesta al tratamiento alcanzados por los pacientes y para poder determinar si, de haber una recaída, ésta se produce con el mismo clon o una proteína monoclonal de isotipo diferente (factor de mal pronóstico)(9).
Ensayo de inmunofijación
Mientras que la electroforesis de proteínas puede detectar patrones de bandas que permiten sospechar una GM, para poder identificar que la aparición de dicha banda homogénea en el PROT sea un CM, es necesario combinar esta técnica electroforética con métodos inmunoquímicos(10).
La IFx es una técnica altamente aconsejable para identificar bandas mono y oligoclonales. La proteína de interés es precipitada en el soporte mediante su antisuero monoespecífico luego del fraccionamiento electroforético de la muestra. Existen diferentes maneras de dispensar el antisuero diluido. En los soportes de acetato de celulosa gelatinizado, mediante dispensadores especiales y en los geles de agarosa, aplicando sobre la superficie del gel una plantilla con espacios para el agregado de los antisueros sobre las proteínas fraccionadas. En ambos soportes es posible agregarlos también mediante una tira de papel de filtro o acetato de celulosa saturados con la dilución adecuada de antisuero(11).
La proteína monoclonal identificada en la IFx debe tener la misma movilidad electroforética que presenta en la electroforesis de proteínas (Figura 1). Cuando se detectan dos o más bandas pequeñas en una región, se asocia con un perfil oligoclonal característico de cuadros infecciosos, patologías autoinmunes o enfermedades linfoproliferativas(10).
Figura 1. Ejemplo de la visualización de la técnica de inmunofijación en gel de agarosa y equipo automatizado.
a) Inmunofijación de un paciente que presenta una banda homogénea en el proteinograma electroforético observado en la calle control (ELP), que resulta ser un componente monoclonal de tipo IgG-kappa por reaccionar frente a los antisuero anti cadenas pesadas g y anti cadenas livianas k de las inmunoglobulinas.

Si los antisueros utilizados no identifican una banda vista en la corrida electroforética de la muestra largada en paralelo, que se utiliza como control de comparación de bandas de corrida, se deben considerar pasos adicionales, como la dilución del antisuero (abordando la posibilidad de tener Ag en exceso) o el uso de antisueros contra otras proteínas(10). Otras veces se realiza el pre-tratamiento de la muestra con 2-mercaptoetanol (2ME) durante 30 minutos, para exponer epitopes antigénicos no detectados en el análisis de las moléculas en su estado conformacional nativo, lo que favorece la identificación de ciertos CM con epitopes ocultos(10,11).
Existen métodos automatizados aplicables a geles de agarosa que disminuyen los errores operativos. La reacción necesita entre 5 y 45 minutos para completarse. Posteriormente los soportes son lavados en buffer fosfato salino con pH entre 7 y 7,5 para eliminar toda la proteína no precipitada(11).
El antisuero se encuentra en contacto directo con las bandas de proteínas fraccionadas electroforéticamente, previniendo así la difusión de las mismas en el soporte. De este modo presenta como ventaja sobre la inmunoelectroforesis una mejor resolución de las bandas de interés y comparables fácilmente con el PROT de referencia. Esta característica la hace más sensible para detectar CM de pequeña concentración asociados a normo o hipergammaglobulinemia policlonal e inmunoglobulinas oligoclonales o biclonales de la misma clase, cercanas entre sí(11).
Sin embargo, la falta de difusión la hacen más susceptible que la inmunoelectroforesis a las condiciones de exceso de antígeno. Efectivamente, debe realizarse una dilución de la muestra, adecuada a la concentración de proteína a identificar, en función del título de antisuero utilizado. Una situación de exceso de antígeno produce la redisolución del inmunocomplejo, con el consecuente resultado falso negativo(11).
La redisolución de bandas monoclonales en la IFx por efecto de prozona ha sucedido, inclusive, respetando las diluciones de muestras recomendadas por el fabricante. El agregado de polietilenglicol al antisuero puede aumentar la sensibilidad del método. El tratamiento previo de la muestra con agentes reductores puede favorecer la detección de pequeños CM complejados con inmunoglobulinas autólogas, que pasan desapercibidos en el PROT y la inmunoelectroforesis(12).
Desde el punto de vista de las buenas prácticas debe tenerse en cuenta que, por tratarse de un fraccionamiento electroforético, se respetarán las mismas consideraciones que para el PROT en fase sólida. Por estar basado en el equilibrio entre antígeno y anticuerpo es sumamente importante verificar el título de los antisueros previamente a su incorporación en la rutina del laboratorio(11). Un título de antisuero inferior al declarado puede ocasionar una redisolución del analito en la IFx. No todos los fabricantes informan la fuente y característica del antígeno utilizado en la inoculación. En el caso de los antisueros utilizados en la IFx con anti-kappa y anti-lambda en orina, la diferencia de reactividad entre marcas comerciales hace necesario utilizar varias de ellas para identificar una PBJ. Más grave es la situación de los antisueros para detectar cadenas livianas libres(15).
Por la misma razón, esta técnica requiere estimar previamente la concentración de la proteína a identificar. En el caso de que sea extremadamente elevada, la muestra deberá́ diluirse.
En condiciones generales, la concentración de trabajo para identificar un CM debe oscilar entre 0.25 y 1 g/dL para obtener una precipitación adecuada con los antisueros comerciales más comúnmente utilizados. La concentración de trabajo óptima del antígeno depende del título de cada antisuero.
Cuando la IFx no se realiza mediante sumersión del soporte en el antisuero, debe asegurarse que se realice en una cámara húmeda para evitar que se sequen los geles. Los lavados posteriores a la fijación deben ser exhaustivos para evitar que la coloración inespecífica del soporte dificulte la visualización de las bandas(11).
Por último, se revela con azul brillante de Coomassie R 250 o por tinción con plata u oro coloidal. Los metales pesados incrementan la sensibilidad del método, haciéndola apropiada para su uso en orina y líquido cefalorraquídeo sin necesidad de concentración previa de las muestras(13). La IFx coloreada con plata u oro coloidal tiene un límite de detección estimada entre 0,6 y 1 mg/L para la proteína de Bence Jones (PBJ). Cinco a diez veces más sensible que el PROT con la misma tinción(14). En la IFx realizada en forma manual utilizando geles de acetato de celulosa deben observarse los resultados obtenidos, previamente al transparentado del gel.
Utilidad y alcance de los resultados
La principal aplicación de la IFx es la identificación de los CM en suero y orina. La monoclonalidad, vista como una banda homogénea en la IFx, es la característica de una GM.
La identificación correcta de la cadena liviana y pesada de un CM puede evitar errores de interpretación de un resultado. Pacientes con MM a cadenas livianas, llamado también MM micromolecular, sólo excretan PBJ en orina. Si la función renal está disminuida y la concentración del CM es elevada, puede ser vista también en suero, confundiéndose con una inmunoglobulina entera y conduciendo a conclusiones erróneas (Figura 2).
Figura 2:. Paciente con diagnóstico de MM a cadenas livianas de tipo lambda y 60% de infiltración de células plasmáticas en médula ósea.
a) Proteinograma sérico en gel de agarosa y equipo automatizado. El paciente presenta una banda homogénea en el proteinograma en la fracción de las betaglobulinas.

b) Proteinograma del suero del paciente en gel de agarosa y equipo automatizado, y de la orina de 24 horas de recolección sin concentración previa, en gel de acetato de celulosa manual y tinción ultrasensible de plata coloidal, largados en simultáneo. En el proteinograma de la orina se ve una banda homogénea, también en la fracción betaglobulinas, posible PBJ.
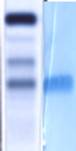
c) Inmunofijación del suero del paciente en gel de agarosa y equipo automatizado. Se ensayan los antisueros frente a las 5 clases de cadenas pesadas y los 2 tipos de cadenas livianas de las inmunoglobulinas, certificando que la banda del suero es el reflejo sérico de la PBJ.

De la misma manera, una inmunoglobulina monoclonal entera puede tener una concentración tan elevada que satura el glomérulo y el túbulo renal, excretándose por orina. Una mala interpretación de este cuadro puede llevar a concluir la presencia de una PBJ, cuando en realidad no lo es. Cabe mencionar que todo MM o GMSI tiene peor pronóstico si presenta PBJ(16).
Nuestro grupo de trabajo (en concordancia con otros autores) ha observado durante el seguimiento de pacientes con MM tratados con altas dosis de quimioterapia seguido de trasplante de autólogo de células madres (TAMO), la aparición en suero de bandas oligoclonales (BO) post-TAMO. El 16.4% (50/305) de los pacientes presentaron durante su seguimiento múltiples componentes homogéneos de baja concentración que, tipificados por IFx, podían diferir en el isotipo de la cadena pesada, en la cadena liviana y en la movilidad electroforética del CM original. Esto se visualizó en el PROT a los 6,6 meses post-TAMO en promedio (1-81 meses) y con una duración promedio de 9,8 meses (1-36). Se pudo observar que los 50 pacientes presentaron recuperación de las inmunoglobulinas policlonales, con cifras normales o incluso ligeramente aumentadas, coincidentemente con la aparición de dichas BO de baja concentración. Posteriormente, al desaparecer las mismas, se mantuvieron las inmunoglobulinas policlonales dentro del rango normal, en varios pacientes con ausencia del CM original confirmado por IFx y en otros con vestigios del mismo.
Aunque la aparición de BO en el suero de los pacientes generó una dificultad adicional a la hora de realizar la interpretación cuali/cuantitativa del CM original, su presencia se correlacionó con efectos adversos menos frecuetes de la terapia aplicada y mayores tiempos de sobrevida global y libre de enfermedad de los pacientes(17,18) (Figura 3).
Figura 3. Paciente con diagnóstico de MM, que recibe como tratamiento un TAMO.
a) Proteinograma del suero del paciente en gel de agarosa y equipo automatizado, y de la orina de 24 horas de recolección sin concentración previa, en gel de acetato de celulosa manual y tinción ultrasensible de plata coloidal. Proteinograma sérico donde se observa la presencia de un componente monoclonal en la zona rápida de las gammaglobulinas, que se caracterizó por inmunofijación como de tipo IgG-kappa. El proteinograma de orina muestra una proteinuria de tipo “mielomatosa” con compromiso glomerular de alta selectividad.
![]()

b) Proteinograma e inmunofijación realizadas en gel de agarosa y equipo automatizado. Proteinograma sérico del paciente a los 5 meses post-TAMO donde se observa la aparición de bandas oligoclonales, caracterizadas por inmunofijación como 2 IgG-K, 1 IgM-L y 1 IgG-L. Puede observarse que el paciente logra una muy buena remisión parcial al tratamiento, al visualizarse su componente “M” original sólo por inmunofijación, con aparente ausencia en el proteinograma sérico.

Debido a la importancia que tiene la variación de la concentración del CM en la evaluación de la respuesta terapéutica y por otra parte, la importancia de la detección de las BO dado su valor pronóstico favorable luego del trasplante, resulta imprescindible realizar IFx conjuntamente con el PROT en el seguimiento de dichos pacientes.
A su vez, se ha observado que aquellos pacientes con BO y zona gammaglobulina elevada en el PROT arrojan resultados de relación anormal de la sFLC, a favor de la cadena liviana libre kappa vs una relación normal, en los pacientes con valores de zona gammaglobulina normal, con diferencia estadísticamente significativa. En estos casos vuelve a considerarse fundamental la realización de la IFx para certificar la presencia de BO y la remisión completa (RC) (ausencia del CM por IFx) alcanzada o no, post-TAMO. A su vez, se demuestra una limitación en la prueba de sFLC en la evaluación de la RC estricta para estos pacientes con MM, TAMO y RC, si presentan BO en suero(18,19).
Más recientemente, con el advenimiento de los anticuerpos monoclonales terapéuticos para el tratamiento de pacientes con MM, es posible observar en el suero de los mismos una interferencia con las dosis habituales utilizadas, que resulta en la aparición de una proteína monoclonal visible y cuantificable en el PROT y una banda monoclonal de tipo IgG-kappa caracterizada por IFx (Figura 4).
Figura 4. Paciente con diagnóstico de MM de tipo IgA-kappa en recaída y rescate con daratumumab.
a) Proteinograma del suero del paciente en gel de agarosa y equipo automatizado, donde se observa la presencia del componente monoclonal en la fracción beta-2 globulinas, que se caracterizó por inmunofijación como de tipo IgA-kappa, mostrando la recaída del MM.

b) Proteinograma del suero del paciente en gel de agarosa y equipo automatizado. Fijación en acetato de celulosa gelatinizado manual cuando comienza tratamiento con daratumumab/dexametasona. Se observa en el proteinograma sérico una nueva banda homogénea en el sector lento de la zona de las gammaglobulinas. Al realizar la inmunofijación se identifica como de tipo IgG-kappa y ausencia del componente monoclonal original IgA-kappa en beta. El paciente alcanza la remisión completa de la enfermedad y se observa la interferencia del anticuerpo monoclonal terapéutico daratumumab, debido a la banda de precipitación de tipo monoclonal frente a anti IgG-kappa correspondiente.
 |
La relevancia de dicha interferencia es que tiene el potencial de indicar falsamente un grado de respuesta deficiente a la terapia, sobre todo en aquellos casos en que el CM original es del mismo tipo inmunológico (IgG-kappa) y tiene igual movilidad electroforética en el PROT que el anticuerpo terapéutico(20). La posibilidad de superponer, en PROT realizados por electroforesis capilar, los perfiles del paciente en ingresos anteriores a comenzar el tratamiento, sobre los nuevos controles, nos permiten comparar movilidades e identidades y descartar la interferencia.
Dado los criterios de grupo de trabajo internacional sobre el MM (IMWG) para evaluar la calidad de respuesta al tratamiento aplicado resulta fundamental que la banda monoclonal proporcionada por el anticuerpo terapéutico no se confunda con el CM original del paciente. Aunque la interferencia no se circunscribe exclusivamente al daratumumab (anticuerpo monoclonal anti-CD38 IgG1-κ), ya que también se observa en tratamientos con elotuzumab e isatuximab, se ha desarrollado un ensayo de IFx específico para anularla, llamado DIRA, pero el mismo no se encuentra disponible en nuestro país(21).
En nuestra experiencia llevamos realizado el seguimiento de 89 pacientes tratados con daratumumab, 3 con elotuzumab y 3 con isatuximab, de allí la importancia de que el bioquímico esté informado respecto del tratamiento que reciben sus pacientes y sea consciente de que la presencia de una nueva banda con movilidad de migración en la región de las gammaglobulinas, de 0,10 gr/dL de concentración aproximada en el PROT y tipificada como IgG-kappa por IFx puede derivar del tratamiento con anticuerpos terapéuticos y así expresarlo en los informes de laboratorio entregados.
Más recientemente se comenzó a estudiar el uso de la técnica de espectrometría de masa (EM) para la detección e identificación de las GM. Como cuestiones negativas para su accesibilidad en los laboratorios de análisis clínicos podríamos citar su alto costo, que viene dado por la necesidad de contar con el equipamiento necesario y realizar, previo al análisis, una purificación de las cadenas pesadas y livianas de las inmunoglobulinas en las muestras. La misma consiste en cinco incubaciones del suero del paciente con micropartículas magnéticas recubiertas de anticuerpos anti-IgG, anti-IgA, anti-IgM, anti-kappa y anti-lambda (a las que pueden adicionarse dos incubaciones más, con anti-kappa libre y anti-lambda libre, para obtener mayor sensibilidad), los posteriores lavados y la re-suspensión de los purificados.
Se suma como dificultad la necesidad de contar con el procesamiento de la muestra al momento del diagnóstico, para poder conocer el número de masa específico del CM del paciente y así poder evaluar en controles posteriores la presencia o no del mismo en el espectro y establecer la respuesta terapéutica alcanzada.
Por otro lado, cabe mencionar que la automatización de los procesos es total y la sofisticación del programa informático del equipo permite la interpretación objetiva de los resultados. En cuanto a su utilidad clínica, hay estudios que revelan que la posibilidad de detectar la glicosilación de las cadenas livianas del CM en pacientes con GMSI mediante EM, permite aportar un potente factor de riesgo de progresión a amiloidosis, MM u otra discrasia de células plasmáticas(22).
Está en estudio continuo la mayor sensibilidad de la EM y su posible aporte, en comparación con la IFx y la CF, para determinar la calidad de la respuesta al tratamiento alcanzada por los pacientes y, con ello, la posterior toma de decisión médica. En este sentido hay estudios que demuestran que el valor predictivo negativo de la EM respecto de la enfermedad mínima residual (EMR) por CF en pacientes con MM después del TAMO y al final de la consolidación se acerca al 90%, con una sensibilidad también del 90%. Esto significa que el 90% de los pacientes que eran negativos por EM también lo eran para EMR por CF. Pero, según los autores, el 10% de los pacientes que tenían un CM en la EM, con resultados de EMR negativa por CF, podrían ser o bien falsos negativos debido a la distribución parcheada del MM en médula ósea, o deberse a la presencia de enfermedad extramedular, que impide su identificación en médula(23).
Finalmente, el estudio de EM permite diferenciar la presencia de los anticuerpos monoclonales terapéuticos del CM original del paciente, ya que presentan un número de masa diferente y se ubican, por lo tanto, en otro lugar del espectro.
La pandemia de COVID-19 tampoco pasó desapercibida respecto de la aparición de interferencias de bandas homogéneas en el PROT, especialmente relevantes en pacientes con diagnóstico previo de GM. Así, es posible mencionar, como parte de nuestra experiencia, el ejemplo de un paciente de 57 años y diagnóstico de MM de tipo IgG-kappa. El mismo fue tratado con TAMO, logrando RC en abril de 2021. En su control de agosto del mismo año presentó una banda homogénea de 0,70 gr/dL en la zona gamma del PROT, en un lugar de movilidad diferente que su CM original. La misma fue caracterizada como de tipo IgG-lambda por IFx, permaneciendo el paciente en RC de su MM dada la ausencia de su CM IgG-kappa. Podemos inferir que este hallazgo se trató de una interferencia, por estar cursando la enfermedad COVID-19 de reciente diagnóstico, ya que en la actualidad se encuentra sin mayores complicaciones, sin la interferencia en el PROT y continúa en RC de su MM por IFx.
Reflexiones finales
A la luz de lo antes desarrollado, antes de informar los resultados de la IFx en los diversos líquidos biológicos de los pacientes estudiados, es indispensable evaluarlos clínica y metrológicamente para asegurar la coherencia con informes previos, el diagnóstico presuntivo y su historia clínica.
Una vez que se haya validado la serie analítica mediante los resultados del esquema de control interno y del informe de errores emitidos por el instrumental o reportado por el personal, se procede a la validación bioquímica y clínica. También es conveniente un seguimiento estadístico de la proporción de resultados anormales(11).
La validación bioquímica implica conocer el comportamiento de los analitos en forma individual y en conjunto con otros, asociados en un perfil de laboratorio, y así emitir un informe completo y complementario de todas las pruebas. Por ejemplo, el estudio de las GM implica un perfil que suele incluir el PROT, la cuantificación de inmunoglobulinas IgM, IgA e IgG, IFx, cuantificación de β2 microglobulina y sFLC en suero.
Finalmente, la validación clínica del resultado obtenido implica la coherencia de los mismos en función de la historia clínica. debiendo ser compatibles con el estado del paciente, su historia analítica previa y/o el tratamiento al que está siendo sometido. De ahí que es aconsejable realizar los seguimientos de los pacientes en un mismo laboratorio de análisis clínicos.
Por lo antes mencionado, queda claro que a la correcta realización analítica de la IFx se suma la necesidad de contar para su interpretación con los datos del paciente. Esto será lo que permita discernir si los resultados emitidos tienen valor diagnóstico, valor pronóstico, si estamos en momentos de evaluar RC de la enfermedad ante una terapia recibida o si estamos frente a la ocurrencia de una recaída bioquímica de la enfermedad. Además, podemos estar advirtiendo respecto de la presencia de BO en pacientes con MM (parámetro de buen pronóstico tardío post-TAMO) o detectando interferencias, sean éstas producidas por anticuerpos monoclonales terapéuticos o las observadas en épocas de la pandemia por COVID-19.
Bibliografía
1. Keren DF, Bocsi, G, Billman BL et al. Laboratory Detection and Initial Diagnosis of Monoclonal Gammopathies Guideline From the College of American Pathologists in Collaboration With the American Association for Clinical Chemistry and the American Society for Clinical Pathology. Arch Pathol Lab Med. 2022;146:575-590.
2. Bradwell AR, Carr-Smith HD, Mead GP et al. Highly sensitive, automated immunoassay for immunoglobulin free light chains in serum and urine. Clin Chem. 2001;47(4):673-680.
3. Oliveros Conejero, R, Pascual Usandizaga, P, Garrido Chércoles, A. Optimización de flujos de trabajo y paneles de cribado para la detección de gammapatias monoclonales malignas. Adv Lab Med/Av Med Lab. 2020;1:2019-0028.
4. Kyle RA, Larson DR, Therneau TM et al. Long-term follow-up of monoclonal gammopathy of undetermined significance. N Engl J Med. 2018;378(3):241-249.
5. Sackmann F, Pavlovsky MA, Corrado C, Pizzolato M, Alejandre M, Pavlovsky S. Prognostic factors in monoclonal gammopathy of undetermined significance. Haematologica. 2008;93(1):153-154.
6. Rajkumar SV, Dimopoulos MA, Palumbo A et al. International Myeloma Working Group updated criteria for the diagnosis of multiple myeloma. Lancet Oncol. 2014;15(12):e538-e548.
7. Hernandez MT, Giraldo P, De la Rubia J et al. Lenalidomide plus dexamethasone for high-risk smoldering multiple myeloma. N Engl J Med. 2013;369(5):438-447.
8. Molina Garrido MJ, Guillén Ponce C, Guirado-Risueño M, Martínez y Sevila C, Carrato Mena A. Diagnóstico diferencial de las gammapatías monoclonales. Anales de Medicina Interna. 2006;23(11):546-551.
9. Keren David F. y Schroeder Lee. Challenges of measuring monoclonal proteins in serum. Clin Chem Lab Med. 2016;54(6):947-961.
10. Keren David F. Capítulo 2. Techniques for protein electrophoresis. Protein Electrophoresis in Clinical Diagnosis. Edward Arnold (Publishers) Ltd. (2003).
11. García M, Madalena L, Gasparini S, Bresciani P, Alejandre M, Facio ML. Módulo 2: Buenas prácticas en el Laboratorio de Proteínas. Proceso analítico. Métodos de fraccionamiento electroforético. El laboratorio de proteínas: conceptos sobre calidad analítica y buenas prácticas. Editorial Eudeba. 2017.143-168.
12. Bossuyt X, Bogaerts A, Schiettekatte G, Blanckaert N. Serum protein electrophoresis by CZE 2000 Serum protein electrophoresis and immunofixation by a semiautomated electrophoresis system. Clin Chem. 1998;44(5):944-9.
13. García M, Madalena L, Bragantini G y col. Electroinmunofijación de orinas sin concentrar por coloración con metales pesados. Acta Bioquím Clín Latinoam. 1996;30(3):215-20.
14. Whicher JT. Immunofixation on cellulose acetate is more efficient than immunoelectrophoresis for detection of paraproteins. Clin Chem. 1983;29(2):402-3.
15. Hutchison CA, Batuman V, Behrens J et al. The pathogenesis and diagnosis of acute kidney injury in multiple myeloma. Nat Rev Nephrol. 2011;8(1):43-51.
16. Alejandre M. Tesis doctoral Mieloma Múltiple y trasplante autólogo de medula ósea, Gammapatia Monoclonal de Significado Incierto. Parámetros bioquímicos: factores de pronóstico, evolución y riesgo. Facultad de Farmacia y Bioquímica. Universidad de Buenos Aires. Argentina. 2011.
17. Alejandre ME, Madalena LB, Pavlovsky MA et al. Oligoclonal bands and immunoglobulin isotype switch during monitoring of patients with multiple myeloma and autologous hematopoietic cell transplantation: a 16-year experience. Clin Chem Lab Med. 2010;48(5):727-31.
18. Gurmukh S. Oligoclonal Pattern/Abnormal Protein Bands in Post-Treatment Plasma Cell Myeloma Patients: Implications for Protein Electrophoresis and Serum Free Light Chain Assay Results. J Clin Med Res. 2017 Aug;9(8):671-679.
19. Alejandre ME, Pavlovsky MA, Remaggi G et al. Serum free light chains and Oligoclonal Bands in patients with Multiple Myeloma and Autologous Bone Marrow Transplantation. Clin Chem Lab Med. 2012;50(6):1093-1097.
20. Murata K, McCash S, Carroll B et al. Treatment of multiple myeloma with monoclonal antibodies and the dilemma of false positive M-spikes in peripheral blood. Clin Biochem. 2018 Jan;51:66-71.
21. Van de Donk NVD, Otten H, El Haddad O et al. Interference of daratumumab in monitoring multiple myeloma patients using serum immunofixation electrophoresis can be abrogated using the daratumumab IFE reflex assay (DIRA). Clin Chem Lab Med. 2016 Jun 1;54(6):1105-9.
22. Dispenzieri A, Larson DR, Rajkumar SV et al. N-glycosylation of monoclonal light chains on routine MASS-FIX testing is a risk factor for MGUS progression. Leukemia. 2020 Oct;34(10):2749-2753.
23. Puig, ASCO 2020. TBS-MS to guide the optimal timing for BM MRD assessment?