Experiencia con plerixafor para la movilización de progenitores hematopoyéticos en trasplante autólogo de médula ósea en un periodo de 11 años.
Experience with plerixafor for the mobilization of hematopoietic progenitors in autologous bone marrow transplantation over a period of 11 years.
Perdomo S1, Bove J1, Menyou A1, Alvez M1, Lipschutz J1, Rocca A1, Isaurralde H1, Topolansky L1, Stevenazzi M1, Grille S1, Diaz L1
1Servicio Médico Integral Centro de Trasplante de Médula Ósea
Luis Alberto de Herrera 2275 C.P 11600, Montevideo, Uruguay
Palabras claves: plerixafor,
movilización,
leucoaféresis de gran volumen.
Keywords: plerixafor,
mobilization,
large volume leukapheresis
Resumen
El trasplante de progenitores hematopoyéticos (TPH) autólogo es una alternativa terapéutica para pacientes con mieloma múltiple y linfomas. Su éxito depende del número de células progenitoras adecuadamente movilizadas, cosechadas e infundidas. En los pacientes pobres movilizadores no se logra obtener un número adecuado de células con la estimulación clásica con factor estimulante de colonias de granulocitos (G-CSF). Con la incorporación de plerixafor se ha logrado superar esta dificultad y reducir el número de movilizaciones. El objetivo de nuestro trabajo es evaluar y describir la efectividad y seguridad de la movilización con G-CSF y plerixafor con leucoaféresis de gran volumen, en 71 pacientes pobres movilizadores para posterior autotrasplante. Esta estrategia logró en el 100% de los pacientes valores adecuados de CD34+ en periferia y en la cosecha de células madre se obtuvo una mediana de 4,6 (rango 3,4 - 6,2) x 106/kg de células CD34+. El injerto fue adecuado, con una mediana de recuperación post trasplante, de neutrófilos > 500/ µL de 11 días (rango 10 - 11), y de plaquetas > 20.000/ µL de 13 días (rango, 12 - 15). Con G-CSF y plerixafor se logró trasplantar a pacientes pobres movilizadores con buenos resultados.
Abstract
Hematopoietic stem cell transplantation (HSCT) autologous is a therapeutic alternative for patients with multiple myeloma and lymphoma. Its success depends on the number of mobilized progenitor cells, harvested and infused. Poor stem cell mobilizers patients fails to obtain an adequate number of cells with classical stimulation with granulocyte colony stimulating factor (G-CSF). Treatment with plerixafor can overcome this difficulty and avoid re-mobilizations. The aim of our study was to evaluate and describe the effectiveness and safety of mobilization with G-CSF and plerixafor with large volume leukapheresis in 71 poor mobilizers patients. This strategy achieved suitable values of CD34+ in peripheral blood in 100% of patients and stem cell harvest was obtained with a median of 4,6 (range, 3,4 - 6,2) x 106/ kg of CD34+ cells. The engraftment was adequate and the median post stem cell transplantation of neutrophils recovery > 500 / uL was 11 days (range, 10 - 11), and platelets recovery > 20.000 / uL was 13 days (range, 12 - 15). With G-CSF and plerixafor, it was possible to transplant poor mobilizer patients with good results.
Introducción
A pesar de la práctica generalizada y establecida, las estrategias de movilización actuales varían entre los centros y difieren en términos de resultado. Son considerados malos movilizadores, aproximadamente el 15 % de los pacientes que se movilizan para obtener progenitores hematopoyéticos en trasplante autologo(1). Los pobres movilizadores se definen como pacientes con menos de 2 × 106 células CD34+/kg recolectadas o pacientes que movilizan menos de 10 - 20 células CD34+/mm3 en sangre periférica, luego de 4 días de estimulación con C-GSF(2). Los factores conocidos de riesgo de pobre movilizador están descriptos en múltiples estudios, tales como edad mayor de 60 años, estado avanzado de enfermedad, múltiples líneas de quimioterapia previas, agentes como fludarabina o lenalidomida, radioterapia previa, plaquetopenia, compromiso de médula ósea o médula ósea hipo celular, entre otros(3). El conocimiento progresivo de los mecanismos implicados en la movilización de progenitores hematopoyéticos desde el estroma medular a la sangre periférica, ha hecho posible el desarrollo de nuevas dianas terapéuticas claves en este proceso. Dentro de estos se ha desarrollado plerixafor, agente que ha permitido un gran avance terapéutico para pacientes pobres movilizadores. Es un inhibidor que bloquea en forma reversible la unión del receptor CXCR4 presente en la membrana de la célula madre con el factor de la matriz medular SDF-1, permitiendo la salida de la célula madre a la periferia. Plerixafor está aprobado por la Food and Drugs Administration (FDA) y por la European Medicines Evaluation Agency (EMA) para esta indicación(3). En Uruguay, el Ministerio de Salud Pública ha aprobado su uso para la misma indicación.
Existen diferentes modalidades de administrar plerixafor. Una en forma preventiva de acuerdo al nivel de CD34+ en periferia después de 4 días de administración de G-CSF, otra de rescate ante una cosecha insuficiente del día 5.
El objetivo de nuestro trabajo fue evaluar y describir la efectividad y seguridad del tratamiento con plerixafor en pacientes sometidos a movilización para posterior TPH autólogo en nuestro Centro Integral de Trasplante de Médula Osea (CITMO).
Material y métodos
Se realizó un trabajo descriptivo, corte transversal. Se incluyeron pacientes sometidos a trasplante autólogo de progenitores hematopoyéticos que requirieron utilizar plerixafor.
Fueron trasplantados 246 pacientes en 11 años, 71 fueron pobres movilizadores (28,8%) y requirieron plerixafor. Mieloma múltiple (MM) n=26, linfoma no Hodgkin (LNH) n= 33 y linfoma Hodgkin (LH) n=12. Se tuvieron en cuenta los criterios de pobre movilizador internacionalmente aceptados(2).
Régimen de movilización. En 66 pacientes se administró G-CSF y plerixafor en forma preventiva y en 5 pacientes en forma de rescate en los primeros años de la utilización de plerixafor, al no obtener con las cosechas un número adecuado de progenitores. En los casos de rescate, el tiempo que pasó entre las cosechas fue aproximadamente 2 meses.
En todos los pacientes que fallo la movilización con G-CSF se utilizó plerixafor.
La movilización en forma preventiva se realizó con G-CSF (12 μg/kg/día) por 4 días seguido de recuento de CD34+ en sangre periférica. El criterio para la utilización de plerixafor (0,24 mg/kg) fue cuando el valor de CD34+/mm3 fue ≤ 15 - 20. En esta serie 21 pacientes requirieron más de una dosis de plerixafor.
En nuestro trabajo los factores pronósticos que consideramos de pobre movilizador fueron: diagnóstico de LNH, edad avanzada (> 60 años), radioterapia previa, uso de fármacos de riesgo (análogos de las purinas y lenalidomida > 4 series), número de planes de quimioterapia recibidos, compromiso de la médula ósea al debut o presentar una médula ósea hipocelular, presencia de plaquetopenia (<170.000/µ L), recuento de leucocitos (< 5.000/µL), valor de hemoglobina < 8 gr/dL al momento de la cosecha así como enfermedad refractaria y falla a una movilización previa(3).
Aféresis. Se realizó la cosecha de progenitores hematopoyéticos por aféresis, a través de catéter Hickman doble lumen 13,5 F, por medio de leucaféresis de gran volumen (4 - 6 volemias) con equipo COBE SPECTRA y OPTIA, iniciada entre las 9 y 12 horas luego de la dosis de plerixafor. Se anticoaguló con solución ACD (ácido cítrico, citrato trisódico y dextrosa) y heparina 3.000 a 5.000 UI por procedimiento. Se realizaron leucaféresis de gran volumen, una en 50 pacientes, dos en 16 y tres en 5. En algunos pacientes se administró calcio vía oral y/o intravenoso dependiendo de la sintomatología vinculada a la hipocalcemia por citrato toxicidad. No observamos otras complicaciones vinculadas a la aféresis.
Los productos obtenidos fueron concentrados por centrifugación a la mitad del volumen original con el objetivo de lograr una concentración de células nucleadas entre 2 - 4x108/mL a los efectos de evitar perdida de viabilidad(4-5-6).
Luego son criopreservados con DMSO (dimetilsulfóxido) al 10% con descenso programado de temperatura con nitrógeno líquido con equipo Nicool Plus y Thermo Scientific y conservado en un tanque de nitrógeno líquido.
Los productos fueron descongelados en baño María a 37ºC inmediatamente antes de la infusión y con control de viabilidad celular utilizando el colorante vital azul de tripán (se obtuvieron valores en torno a 80 - 90% de viabilidad).
Se utilizaron métodos de estadística descriptiva e inferencial. Se utilizaron medidas de resumen (mediana) y dispersión (rango intercuartil) y frecuencias relativas. Para evaluar las diferencias estadísticas entre el recuento de CD34+ previo y posterior a la administración de plerixafor se utilizó el test no paramétrico de Wilcoxon para muestras pareadas. Se consideró como significativo un valor de p menor a 0,05. Los datos estadísticos utilizados para la evaluación de los resultados fueron analizados con SPSS21.
Este trabajo contó con la aprobación del Comité de Ética del Instituto Nacional de Donación y Trasplante de Células, Tejidos y Órganos, de la Universidad de la República, Uruguay.
Además se deja constancia que se obtuvo en cada paciente el consentimiento informado por escrito y el protocolo de estudio se realizó conforme a las normas éticas de la Declaración de Helsinki 1975.
Resultados
Características de los pacientes. Durante el período de trabajo en nuestro centro se realizaron 246 trasplantes de progenitores hematopoyéticos (TPH) autólogos, en 71 pacientes (28,8%) se utilizó plerixafor con el protocolo de movilización como fue mencionado.
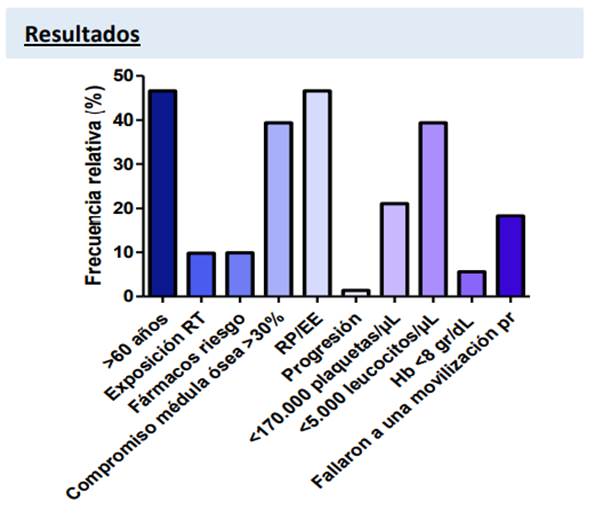
En los pacientes que requirieron plerixafor, la presencia de factores predictores de pobre movilizador fueron: 46,6% >60 años, 9,8% recibieron radioterapia, todos los pacientes recibieron quimioterapia previa con una mediana de ciclos de 8 (6 - 10), 9,9% estuvieron expuestos a fármacos de riesgo (lenalidomida, melfalán, carmustina o fludarabina), 39,4% compromiso de médula ósea >30% al debut, 43,6% remisión parcial (RP) al momento del TPH, 1,4% enfermedad progresiva; del hemograma previo a la movilización, 21,1% tenían <170.000 plaquetas/µL, 39,4% <5.000 leucocitos/µL, 5,6% Hb <8 gr/dL y 18,3% fallaron a una movilización previa.
Todos los pacientes presentaban al menos un criterio de pobre movilizador (Figura 1).
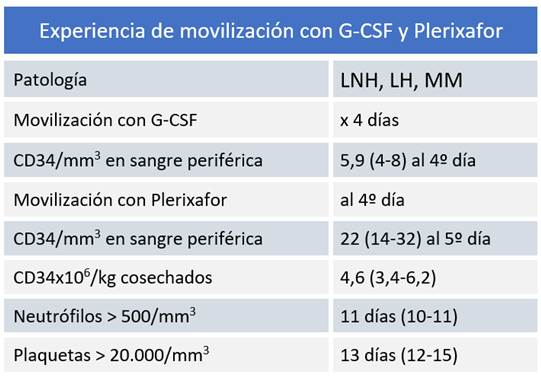
Movilización con plerixafor. Con la movilización con G-CSF por 4 días se obtuvieron 5,9 (4 - 8) CD34/mm3 al día 4 y al utilizar Plerixafor, estos se incrementaron a 22 al día 5 (14 - 32), (p=0,001). Plerixafor permitió obtener un número adecuado de CPH en el 100% de los casos. El número de CD34 cosechadas fue de 4,6 (3,4 - 6,2) x106/Kg con 1 (1 - 2) aféresis promedio. El período de neutropenia ≤ 500/mm3 fue 11 (10 - 11) días y plaquetopenia ≤ 20.000/mm3 13 (12 - 15) días. Tabla 1.
No se constataron reacciones adversas que limiten su uso.
Discusión
En el año 2008 plerixafor fue aprobado para su uso por la FDA en combinación con
G-CSF para la movilización de las células progenitoras hematopoyéticas en pacientes con linfomas y mieloma múltiple sometidos a altas dosis de quimioterapia y TPH. Plerixafor es un antagonista de CXCR4 en forma reversible, que permite la liberación de las células madre de la medula ósea mediante la interrupción de la interacción CXCR4 con su ligando SDF-1 (factor derivado del estroma tisular)(7). La administración de plerixafor junto con G-CSF aumenta la movilización de células CD34+ en sangre periférica con un efecto máximo a las 9 horas después de administrado, lo cual habilita el comienzo de las aféresis(7). Se ha reportado, que la población de células madre movilizadas de esta forma, difieren de las movilizadas solamente con G-CSF. Tienen una mayor proporción de células en fase de crecimiento CD34+ CD38- primitivas, células progenitoras de células dendríticas y células natural killer(8-9-10). Hay un aumento de la expresión en la célula madre del CXCR4 y VLA-4 así como los genes que promueven la adhesión celular, la motilidad celular, el ciclo celular y la anti-apoptosis(8-11). Estas características sugieren que los productos movilizados con plerixafor tienen una mayor capacidad de repoblar la medula ósea y reconstituir el sistema inmune en comparación con injertos movilizados solamente con G-CSF, confirmado en fase experimental en ratones y primates(12).
Plerixafor es una droga bien tolerada, con efectos adversos mínimos. Dentro de los más frecuentes se destacan: fatiga, malestar, sequedad en la boca, reacciones en el sitio de inyección tales como inflamación, eritema, induración, hematoma, irritación, prurito, entre otros(13).
La depuración de plerixafor se encuentra reducida en la insuficiencia renal y se correlaciona con la depuración de creatinina (CLCR). Se deberá reducir la dosis en un tercio (0,16 mg/kg) en los pacientes con insuficiencia renal moderada y severa (CLCR ≤ 50 mL/min)(13).
Actualmente esta droga nos permite realizar TPH a pacientes que de otra forma no recibirían el tratamiento adecuado a su patología. Teniendo en cuenta las recomendaciones actuales, el objetivo a seguir es lograr un producto con un número óptimo de 3 a 5 x 106/kg de CD34+ para asegurar una rápida recuperación de neutrófilos y plaquetas. El beneficio de infundir dosis mayores para minimizar la duración de las citopenias sigue siendo materia de debate(14). En pobres movilizadores se acepta el valor de 2,5 x 106/kg en una sola aféresis, antes de prolongar la realización de mayor número de aféresis y reiterar plerixafor (15). La mayoría de los autores concuerdan en que una dosis mínima de 2 a 2,5 x 106 células CD34+/kg de peso del paciente es apropiada para asegurar una recuperación hematológica no tardía(14-16-17).
La valoración entre el peso real y el ideal es otro valor a tener en cuenta, sobre todo en paciente obesos en los cuales el logro del valor óptimo puede ser difícil de alcanzar. Si bien no hay estudios fehacientes al respecto, se podría llegar a utilizar el valor del peso corregido o IMC (índice de masa corporal) o similar, el IMC es un factor importante que afecta la respuesta del donante a la movilización y, en consecuencia, el rendimiento de progenitores hematopoyéticos. Este efecto puede deberse a una dosis relativamente alta de G-CSF administrada a donantes con un IMC más alto o debido a la presencia de factores intrínsecos desconocidos que afectan la movilización que se correlacionan con la cantidad de tejido adiposo en cada donante(18).
Con respecto a las aféresis, se requiere un acceso venoso central adecuado que además será de utilidad para todas las etapas del trasplante. La leucaféresis de gran volumen, 4 a 6 volemias, asegura una mayor colecta de CD34+ por aféresis, y un menor número de procedimientos, lo que resulta indicado en los pobres movilizadores(15). Aumentan los riesgos de toxicidad por citrato, compensado con la administración de Calcio vía oral y/o intravenoso en pocos casos. Otra complicación es la plaquetopenia post procedimiento (disminución del 40 - 50%) lo que exige un monitoreo pre y post aféresis clínico y paraclínico(19). Por este motivo en algunas oportunidades es necesario una trasfusión de plaquetas en forma previa a una nueva aféresis, a los efectos de lograr estabilidad en la capa de recolección. Destacamos que no siempre se puede predecir el resultado de la pobre movilización. Pacientes que no están catalogados como pobres movilizadores fallan en la movilización clásica y otros pacientes considerados pobres movilizadores, responden adecuadamente(3).
Sumado a los factores de riesgo para la pobre movilización (Figura1) en los últimos tiempos se van agregando otros factores como diabetes y tabaquismo(20-21).
En nuestra población de pobres movilizadores, con plerixafor fue posible en todos los casos obtener un número adecuado de células CD34+ y realizar el trasplante.
No existen trabajos al momento actual sobre implicancia de plerixafor en la sobrevida de los pacientes y de efectos adversos a largo plazo, teniendo en cuenta que es un fármaco de baja toxicidad que se utiliza con diferentes estrategias en diferentes Centros y con resultados similares.
Por otro lado es un fármaco de alto costo. Se debe tener en cuenta realizar el menor número de aféresis, evitar una segunda movilización, lograr un periodo más corto de internación, así como realizar el menor número de transfusiones, todo lo cual logra un costo beneficio adecuado(22). Por estas razones consideramos necesario realizar una adecuada selección de candidatos a recibir plerixafor y protocolizar la utilización del mismo.
En conclusión, a los pacientes que fallaron a la movilización con G-CSF (4 días), se les administró plerixafor, lográndose un número adecuado de progenitores hematopoyéticos en sangre periférica para realizar la cosecha por aféresis. La administración de G-CSF y plerixafor en conjunto es una estrategia efectiva y segura para los pacientes que fallaron inicialmente en la movilización y fueron catalogados como pobres movilizadores, quienes sin su utilización no contarían con la terapéutica del trasplante. Se logró en el 100% de los pacientes resultados clínicos similares a los observados en los pacientes no pobres movilizadores.
Bibliografía
1 Wuchter P, Ran D, Bruckner T y col. Poor mobilization of hematopoietic stem cells-definitions, incidence, risk factors, and impact on outcome of autologous transplantation. Biol. Blood Marrow Transplant. 2010;16:490-499.
2. Olivieri A, Marchetti M, Lemoli R y col. Proposed definition of ‘poor mobilizer’ in lymphoma and multiple myeloma: an analytic hierarchy process by ad hoc working group Gruppo Italiano Trapianto di Midollo Osseo. Bone Marrow Transplant. 2012;47:342-351.
3. Giralt S, Costa L, Schriber J y col. Optimizing autologous stem cell mobilization strategies to improve patient outcomes: consensus guidelines and recommendations. Biol Blood Marrow Transplant. 2014;20:295-308.
4. Fernyhough L, Buchan V, McArthur L y col. Relative recovery of haematopoietic stem cell products after cryogenic storage of up to 19 years. Bone Marrow Transplant. 2013;48:32-35.
5. McCullough J, Haley R, Clay M y col. Long-term storage of peripheral blood stem cells frozen and stored with a conventional liquid nitrogen technique compared with cells frozen and stored in a mechanical freezer. Transfusion. 2010;50:808-819.
6. Spurr E, Wiggins N, Marsden K y col. Cryopreserved human haematopoietic stem cells retain engraftment potential after extended (5–14 years) cryostorage. Cryobiology. 2002;44:210-217.
7. Harvey RD, Kaufman JL, Johnson HR y col. Temporal changes in plerixafor administration and hematopoietic stem cell mobilization efficacy: results of a prospective clinical trial in multiple myeloma. Biol. Blood Marrow Transplant. 2013;19:1393-1395.
8. Larochelle A, Krouse A, Metzger M y col. AMD3100 mobilizes hematopoietic stem cells with long-term repopulating capacity in nonhuman primates. Blood. 2006;107:3772-3778.
9. Varmavuo V, Mäntymaa P, Kuittinen T y col. Blood graft lymphocyte subsets after plerixafor injection in non-Hodgkin’s lymphoma patients mobilizing poorly with chemotherapy plus granulocyte-colony-stimulating factor. Transfusion. 2012;52:1785-1791.
10. Gazitt Y, Freytes CO, Akay C y col. Improved mobilization of peripheral blood CD34+ cells and dendritic cells by AMD3100 plus granulocyte-colony-stimulating factor in non-Hodgkin’s lymphoma patients. Stem Cells Dev. 2007;16:657-666.
11. Fruehauf S, Seeger T, Maier P y col. The CXCR4 antagonist AMD3100 releases a subset of G-CSF-primed peripheral blood progenitor cells with specific gene expression characteristics. Exp. Hematol. 2006;34:1052-1059.
12. Hess DA, Bonde J, Craft TP y col. Human progenitor cells rapidly mobilized by AMD3100 repopulate NOD/SCID mice with increased frequency in comparison to cells from the same donor mobilized by granulocyte colony stimulating factor. Biol. Blood Marrow Transplant. 2007;13:398-411.
13. SlaterPlerixafor.J Adv Pract Oncol. 2012; 3: 49-54.
14. Hübel K. Mobilization and Collection of HSC. The EBMT Handbook Hematopoietic Stem Cell Transplantation and Cellular Therapies. E Carreras, C Dufour, M Mohty, N Kröger 2019, p 117-122. 7 th Edition, Springer, Cham (Zug).
15. Gasová Z, Marinov I, Vodvárková S y col. PBPC collection techniques: standard versus large volume leukapheresis (LVL) in donors and in patients. Transfus. Apher. Sci. 2005;32:167-176.
16. Haas R, Mohle R, Fruhauf S y col. Patient characteristics associated with successful mobilizing and autografting of peripheral blood progenitor cells in malignant lymphoma. Blood. 1994;83:3787-3794.
17. Ketterer N, Salles G, Raba M y col. High CD34+ cell counts decrease hematologic toxicity of autologous peripheral blood progenitor cell transplantation. Blood 1998;91:3148-3155.
18. Chen J, Burns K, Babic A y col. Donor body mass index is an important factor that affects peripheral blood progenitor cell yield in healthy donors after mobilization with granulocyte–colony-stimulating factor. Transfusion. 2014;54:203-210.
19. Cassens U, Barth IM, Baumann C y col. Factors affecting the efficacy of peripheral blood progenitor cells collections by large-volume leukaphereses with standardized processing volumes. Transfusion. 2004;44:1593-1602.
20. Ferraro F, Lymperi S, Méndez-Ferrer S y col. Diabetes impairs hematopoietic stem cell mobilization by altering niche function. Sci Transl Med. 2011;3:104ra101.
21. Livingston D, Motlagh D, Debelak J y col. Phase 2 study of intramyocardial injection of autologous CD34+ cells to treat subjects with refractory chronic myocardial ischemia (CMI): factors influencing mobilization and apheresis. Blood. 2009;114:3227.
22. Martin AP, Richards S, Haycox A y col. Evaluating the use of plerixafor in stem cell mobilisation - an economic analysis of the PHANTASTIC trial. J Clin Apher. 2016;31:434-442.