Comparación de perfiles multiméricos del factor de von Willebrand obtenidos mediante un ensayo electroforético comercial y electroforesis local con geles de agarosa 1%
Comparison of von Willebrand factor multimer profiles obtained through a commercial electrophoretic test and home-made electrophoresis with 1% agarose gels
López MS1, Paiva J2, Woods AI3, Saez MS1, Barrera LH1, Privitera V4, Chuliber F4, Villagra Iturre M2,4, Penchasky D4, Sorroche P1, Martinuzzo ME1, Sánchez Luceros A2,3.
1 Secciones de Hematología-Hemostasia y Proteínas del Laboratorio Central del Hospital Italiano de Buenos Aires, Argentina
2 División Química, Instituto de Investigaciones Hematológicas, Academia Nacional de Medicina, Hemostasia y Trombosis, Buenos Aires, Argentina
3 Laboratorio de Hemostasia y Trombosis, IMEX-CONICET-Academia Nacional de Medicina, Laboratorio de Hemostasia y Trombosis, Buenos Aires, Argentina
4 Servicio de Hematología del Hospital Italiano de Buenos Aires, Argentina
Dirección de e-mail: lopezmarinasol@gmail.com
Palabras claves: factor von Willebrand,
multímeros del factor von Willebrand,
enfermedad de von Willebrand.
Keywords: von Willebrand factor,
von Willebrand factor multimers,
von Willebrand disease.
Resumen
La evaluación de multímeros del factor de von Willebrand (VWF) es parte esencial del diagnóstico de algunas variantes de la enfermedad de von Willebrand (VWD). Mediante técnicas electroforéticas adecuadas se pueden estimar los multímeros de peso molecular bajo (LMWM), intermedio (IMWM), alto (HMWM) y ultra-alto (UHMWM).
El objetivo del presente trabajo es determinar si el perfil multimérico obtenido mediante electroforesis en gel de agarosa seguido de inmunofijación en sistema semiautomático (Hydragel 5) y el obtenido mediante el método de referencia son comparables. Se analizaron 24 muestras: 4 de pacientes con síndrome de von Willebrand adquirido (AVWS) secundarios a síndrome mieloproliferativo con trombocitosis (MPS-T), 18 de pacientes con VWD de diferente tipo y 2 de pacientes con púrpura trombocitopénica trombótica (PTT).
Se realizó la medición con dos metodologías diferentes:
- Multímeros por método semiautomático: electroforesis SDS-agarosa seguida de inmunofijación usando Hydragel 5 von Willebrand Multimers kit en el instrumento Hydrasys 2 (Sebia), analizado mediante programa Phoresis.
- Multímeros por método de referencia: electroforesis SDS-agarosa seguida de inmunofijación usando anticuerpos policlonales: anti-VWF humana desarrollado en conejo, anti IgG de conejo desarrollado en cerdo/biotinilado, avidina peroxidasa y reveladas con 4Cl-1-Naftol. Perfil multimérico: analizado mediante ImageQuant TL 8.1 (GE Healthcare).
Las muestras de pacientes con AVWS mostraron una disminución de HMWM. Aquéllas con VWD tipo 1 mostraron un perfil multimérico normal. Se detectaron UHMWM en las muestras de pacientes con PTT.
Con respecto a las muestras de pacientes con VWD tipo 2, 2A, 2B y 2M, se obtuvo buena concordancia entre ambos métodos.
El método semiautomático parece ser útil y apropiado como tamizaje de perfiles multiméricos de VWF en laboratorios clínicos de Hemostasia, analizados por profesionales con alta experiencia en el diagnóstico de VWD.
Introducción
La enfermedad de von Willebrand (VWD) es el desorden hemorrágico congénito más frecuente y se produce por la deficiencia y/o alteración del factor von Willebrand (VWF). El VWF es una glicoproteína multimérica que se sintetiza en las células endoteliales y megacariocitos y se almacena en las organelas de depósito: los cuerpos de Weibel Palade en las células endoteliales y los α-gránulos plaquetarios. Además, este factor circula en el plasma unido al factor VIII, protegiéndolo de la proteólisis mediada por inhibidores fisiológicos(1). La unidad funcional está conformada por un monómero, que luego dimeriza, a través de uniones S-S en el dominio VWF-CK, en el extremo C-terminal. Luego de sucesivos pasos de O- y N-glicosilación, se produce la unión de los dímeros en multímeros, mediante uniones S-S entre el dominio VWF-D3. Los multímeros de VWF incluyen formas de peso molecular bajo (LMWM), intermedio (IMWM), alto (HMWM) y formas de peso molecular ultragrandes (UHMWM). El VWF almacenado en las organelas de depósito y posteriormente liberado por la vía secretoria es rico en UHMWM, mientras que el VWF plasmático secretado constitutivamente presenta multímeros pequeños, intermedios y grandes(2). Los UHMWM son altamente trombogénicos y son degradados, una vez liberados, por la metaloproteasa plasmática ADAMTS13, enzima que cliva específicamente al VWF entre los residuos Tyr1605-Met1606 localizados en el dominio VWF-A2(1).
Una de las funciones del VWF es participar de la hemostasia primaria, dada por su capacidad de unión al colágeno subendotelial (principalmente a través del dominio VWF-A3), propiciando la adhesividad plaquetaria a través de la unión a la glicoproteína 1bα (GPIbα) que forma parte del complejo Ib-IX-V, a través del dominio VWF-A1. También participa en la hemostasia secundaria, al transportar al FVIII:C y protegerlo de la proteólisis por sus inhibidores naturales. Además, favorece la agregación plaquetaria mediante su capacidad de unión a la integrina α2b-β3 a través del péptido Arg-Gly-Asp en el dominio VWF-C4. La actividad adhesiva del VWF depende del tamaño de sus multímeros(2) y la organización multimérica es fundamental para la funcionalidad del VWF(3).
La VWD se clasifica en: variantes cuantitativas y variantes cualitativas. Las variantes cuantitativas son: VWD tipo 1 y tipo 3; el tipo 1 es la deficiencia leve, mientras que el tipo 3 es severo. Las variantes cualitativas, el tipo 2, se subclasifican a su vez en: VWD 2A, 2B, 2M y 2N.
La historia personal y familiar de sangrado, ya sea espontáneo o debido a trauma, cirugía, post parto, etc.(1) en conjunto con los resultados de laboratorio son importantes para arribar al diagnóstico en cada paciente individual y a una correcta clasificación de la enfermedad.
Por otro lado, para varios subtipos cualitativos se requiere realizar un diagnóstico diferencial con otras alteraciones que pueden cursar con la misma clínica y que, además, pueden presentar resultados similares de ciertas pruebas de laboratorio.
Las pruebas generales de laboratorio, como tiempo de protrombina, APTT, tiempo de trombina y fibrinógeno, no confirman ni excluyen VWD, ya que no tienen la suficiente sensibilidad. Las pruebas específicas, como la medición de VWF (funcional e inmunológico) y del factor VIII, son necesarias para el diagnóstico, mientras que las pruebas complementarias, como la agregación plaquetaria con ristocetina (RIPA) a bajas dosis y la determinación de multímeros del VWF, permiten clasificar a la VWD en diferentes tipos(1). Recientemente se ha publicado una guía diagnóstica basada en evidencia, consensuada entre 4 sociedades científicas: Sociedad Americana de Hematología, Sociedad Internacional de Trombosis y Hemostasia, Fundación Nacional de la Hemofilia de Estados Unidos y la Federación Mundial de la Hemofilia, que recomienda los pasos a seguir para el diagnóstico de los diferentes tipos de VWD(3).
El ensayo para evaluar los multímeros del VWF es parte importante en el diagnóstico de la VWD. A través del mismo se puede estimar todo el perfil multimérico (LMWM, IMWM, HMWM y UHMWM) cuali y cuantitativamente. No sólo se evalúa la presencia o ausencia de una fracción multimérica, sino que también se puede evaluar la intensidad de las bandas que conforman los diferentes multímeros, dato importante en el caso de proteólisis alterada del VWF.
Esta prueba se puede utilizar para distinguir el tipo 2A y 2B VWD del tipo 2M (o tipo 1) y del AVWS. Sin embargo, el análisis multimérico actualmente sólo se realiza en un número limitado de laboratorios especializados por ser técnicamente largo, laborioso y de difícil estandarización.
Sus dificultades metodológicas pueden llevar a resultados erróneos en la interpretación de las variantes de la enfermedad(4,5) y eso lo transforma en una metodología utilizada en segunda línea en el diagnóstico de VWD.
En los últimos años se diseñó un kit denominado Hydragel 5 von Willebrand Multimers (Sebia) destinado a la detección y análisis de la distribución de los multímeros del VWF del plasma humano mediante electroforesis e inmunofijación en gel de agarosa en el sistema semiautomático Hydrasys 2.
El análisis se realiza en 2 etapas:
- electroforesis en gel de agarosa para separar las proteínas del plasma,
- inmunofijación con un antisuero anti-VWF y un anticuerpo marcado con peroxidasa que, al ser presentados ante el sustrato en presencia de peróxido de hidrógeno, pondrá en evidencia el perfil multimérico correspondiente.
El kit provee los geles ya preparados y el sistema semiautomático Hydrasys 2 realiza todas las etapas necesarias para obtener geles listos para su interpretación(6).
Este kit se presenta como una técnica más simplificada para evaluar el perfil multimérico del VWF con respecto a la técnica tradicional y de referencia que es la electroforesis en SDS-PAGE(7).
Por lo tanto, el objetivo de este trabajo es determinar si los perfiles multiméricos obtenidos mediante electroforesis en gel de agarosa seguido de inmunofijación en sistema semiautomático (Hydragel 5) son comparables a los obtenidos mediante el método tradicional realizado en un centro de referencia para la VWD.
Materiales y métodos:
Se analizaron un total de 24 muestras. 4 con diagnóstico de síndrome de von Willebrand adquirido (AVWS) secundarios a síndrome mieloproliferativo con trombocitosis (MPS-T), mientras que 18 muestras presentaban algún tipo de VWD: 6 tipo 1, 9 tipo 2 (confirmados mediante biología molecular), 1 probable tipo 2N, 2 tipo 2 por discordancia entre actividad y niveles antigénicos de VWF no clasificado, y 2 púrpura trombocitopénica trombótica (PTT).
Las muestras fueron analizadas por dos metodologías diferentes para determinar el perfil multimérico:
- multímeros por método semiautomático: electroforesis SDS-Agarosa seguida de inmunofijación usando Hydragel 5 von Willebrand Multimers kit en el instrumento Hydrasys 2 (Sebia), analizado mediante el programa Phoresis.
- multímeros por método de referencia: electroforesis SDS-agarosa seguida de inmunofijación usando anticuerpos policlonales: anti-VWF humana desarrollado en conejo, anti IgG de conejo desarrollado en cerdo/biotinilado, avidina peroxidasa y reveladas con 4Cl-1-naftol. Perfil multimérico: analizado mediante ImageQuant TL 8.1 (GE Healthcare)(8).
Estudios genotípicos: el DNA genómico fue extraído de leucocitos de sangre periférica. El exón 28 del gen de VWF, que abarca los dominios VWF-A1 y A2, fue amplificado por PCR en Perkin-Elmer Thermocycler 2400. Existe un pseudogen localizado en el cromosoma 22 que tiene alta homología con el VWF entre los exones 23 al 34; por lo tanto, los cebadores se diseñaron evitando la amplificación del mismo. Dado el gran tamaño del exón 28, se estudió por fragmentos, mediante técnica de PCR anidada. Se realizó la secuenciación directa del DNA amplificado por la técnica automatizada de Sanger en el secuenciador automático ABI Prism 310 Genetic Analyzer (Applied Biosystems, Foster City, CA)(9,10). Para confirmar la presencia de variantes genotípicas causales de la enfermedad (VGCE) se secuenció la cadena complementaria.
La determinación del nivel antigénico y de actividad del VWF se realizó mediante técnicas inmunoturbidimétricas automatizadas para coagulómetros foto-ópticos.
Debido a que se trataba de muestras de descarte, ya informadas, que fueron almacenadas con fines educativos y académicos, y por el tipo de diseño del estudio establecido en el protocolo que fue aprobado por el comité de ética (CEPI), no se solicitó firma de consentimientos a los pacientes cuyas muestras fueron utilizadas.
La técnica comercial no presenta controles de calidad en el kit. Sin embargo, la muestra de pool normal que se corre en cada gel, podría funcionar como un control normal además de ser usado como perfil comparativo para el resto de las muestras largadas en ese mismo gel.
Resultados
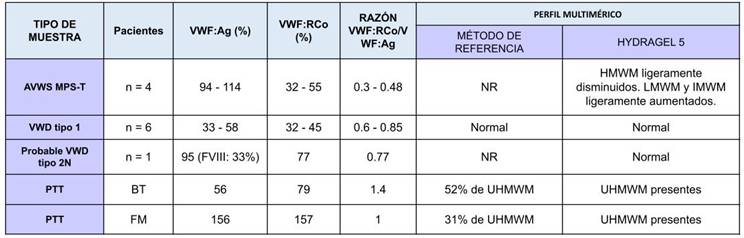
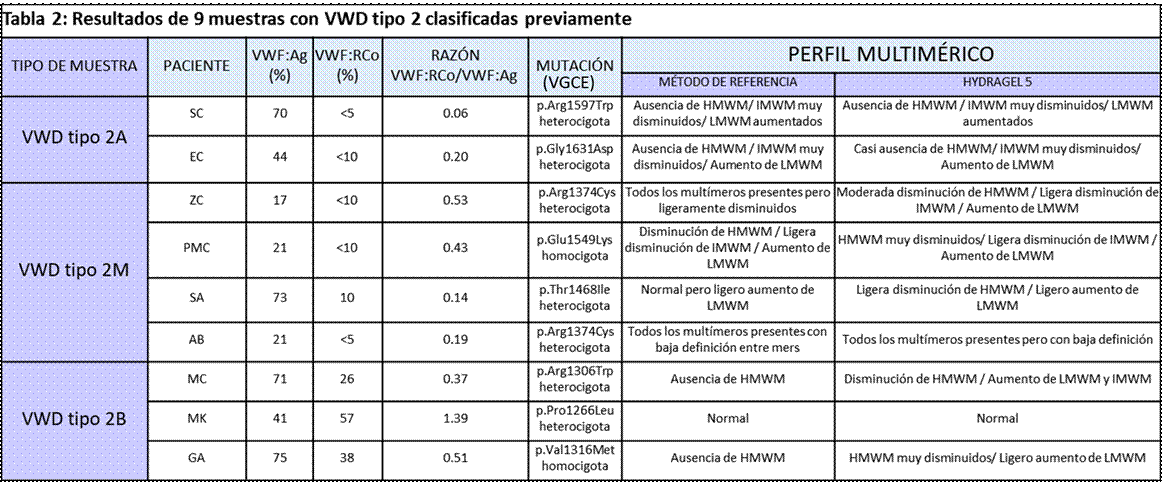
Los perfiles multiméricos obtenidos con ambas metodologías junto con las VGCE detectadas para cada muestra se detallan en las tablas 1 y 2, así como los valores de VWF antigénico (VWF:Ag), su actividad (VWF:RCo) y el cociente VWF:RCo/VWF:Ag.
Cada gel fue procesado en una jornada laboral, lo que se traduce en menores tiempos de procesamiento, a diferencia de la técnica local, que requiere habitualmente dos jornadas laborales. En los escaneos de densitometría realizada del gel a través del programa Phoresis se consideró de izquierda a derecha LMWM picos 1 a 3, IMWM picos 4 a 7, HMWM picos 7 en adelante, según las recomendaciones del fabricante.
Al evaluar los diferentes geles obtenidos en las jornadas laborales notamos que aquellas muestras compatibles con AVWS en pacientes con síndromes mieloproliferativos crónicos con trombocitosis presentaron cocientes VWF:RCo/VWF:Ag entre 0,3-0,48 y mostraron una disminución de los HMWM con aumento de IMWM y LMWM (Figura 1).
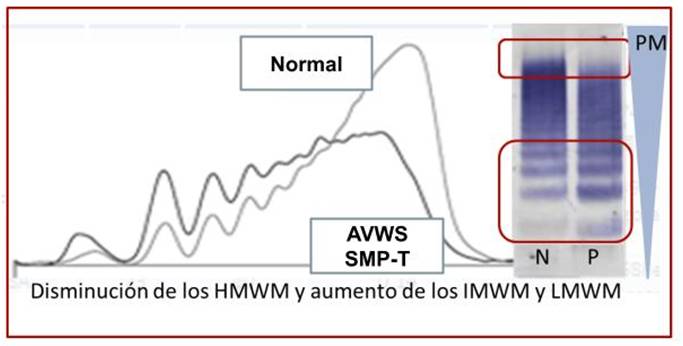
Figura 1. Perfil multimérico obtenido mediante la técnica Hydragel 5 von Willebrand multimers, para una muestra con AVWS. El gráfico designado con la letra N corresponde al pool normal que se corre junto con las muestras elegidas a analizar para esa corrida. El mismo sirve como patrón comparativo para el resto de las muestras. P= muestra de paciente; N= pool normal.
El perfil multimérico obtenido de las muestras con VWD tipo 1 fue normal, es decir, se visualizaron todos los picos correspondientes a los diferentes multímeros. La diferencia entre este perfil multimérico con el del pool normal es la altura alcanzada por dichos picos, ya que la misma va a depender del nivel de VWF (Figura 2).
En el caso de las muestras con PTT, se detectaron UHMWM. (Figura 3).
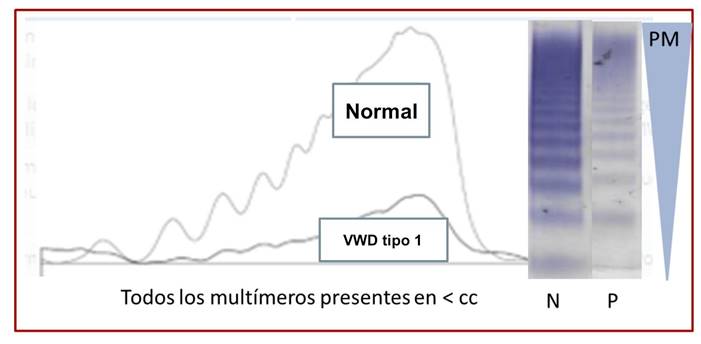
Figura 2. Perfil multimérico obtenido mediante la técnica Hydragel 5 von Willebrand multimers, para una muestra con VWD tipo 1. P= muestra de paciente; N= pool normal.
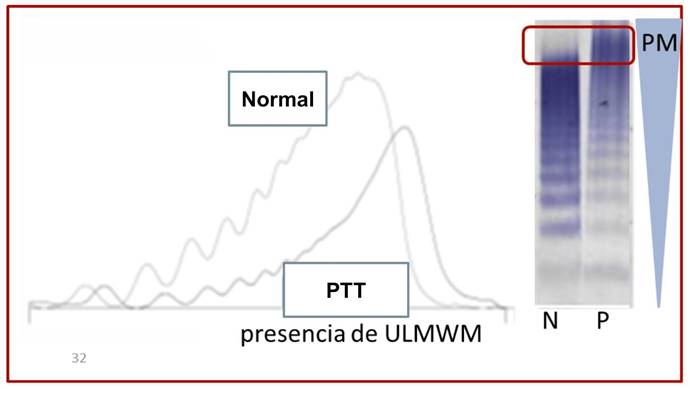
Figura 3. Perfil multimérico obtenido mediante la técnica Hydragel 5 von Willebrand multimers, para una muestra con PTT. P=Paciente; N= pool normal
En las muestras con VWD tipo 2 se obtuvo buena concordancia entre ambos métodos:
- VWD 2A: los resultados de los cocientes VWF:RCo/VWF:Ag eran muy bajos y se evidenció ausencia de HMWM, IMWM muy disminuidos y aumento de LMWM en ambos casos por ambos métodos (Tabla 2). En la figura 4 se presentan los perfiles multiméricos obtenidos por el método semiautomático de los dos pacientes con VWD 2A evaluados que presentan distintas VGCE.

Figura 4. Perfil multimérico obtenido mediante la técnica Hydragel 5 von Willebrand multimers, para 2 muestras con VWD 2A. P=paciente; N= pool normal
- VWD 2B: dos de las muestras de pacientes con las variantes genotípicas p.Val1316Met (homocigota) y p.Arg1306Trp (heterocigota) presentaron razones VWF:RCo/VWF:Ag disminuidas, observándose perfiles multiméricos con disminución de HMWM y aumento de IMWM y LMWM (Figura 5a), siendo los perfiles coincidentes entre las técnicas de referencia y semiautomática. No obstante, en una muestra de un paciente heterocigota para la mutación p.Pro1266Leu se obtuvo un cociente VWF:RCo/VWF:Ag normal y perfiles multiméricos conservados a través de las dos técnicas evaluadas. (Figura 5 b).

Figura 5. Perfiles multiméricos obtenidos mediante la técnica Hydragel 5 von Willebrand multimers, para 2 muestras con VWD 2B con patrones multiméricos diferentes. P=paciente; N= pool normal
- VWD 2M: se observó la presencia de todos los multímeros, pero con baja definición del perfil debido a un nivel muy bajo antigénico y de actividad del VWF (se presenta como ejemplo una muestra heterocigota para la mutación p.Arg1374Cys) (Figura 6a).En otras dos, sin embargo, se evidenció una disminución ligera o marcada de HMWM y de IMWM, y aumento de LMWM (se presenta como ejemplo la muestra de un paciente homocigota para la mutación p.Glu1549Lys) (Figura 6b).
- VWD probable 2N: se obtuvo un perfil multimérico normal.
- VWD tipo 2 sin clasificar: se observó presencia de todos los multímeros en una de las muestras, y ligera disminución de los HMWM en la otra.
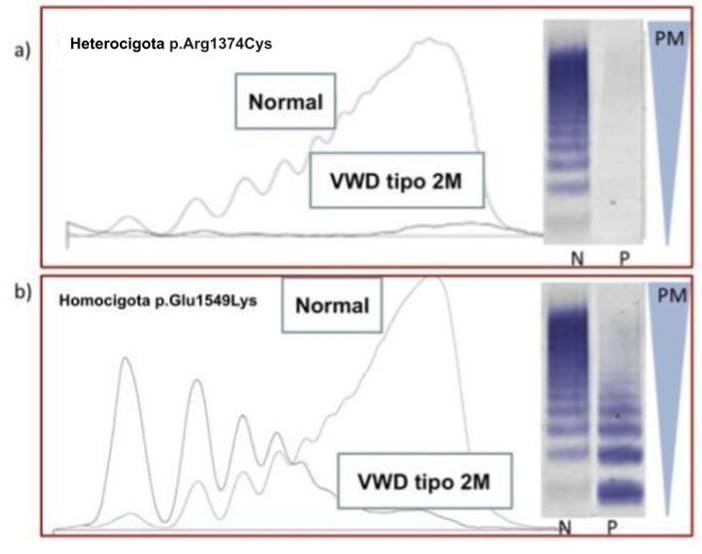
Figuran 6. Perfil multimérico obtenido mediante la técnica Hydragel 5 von Willebrand multimers, para muestras con VWD tipo 2M.
a) se observa un perfil normal pero de baja intensidad y definición de los multímeros.
b) patrón que presenta disminución de HMWM y de IMWM, y aumento de LMWM.
Discusión
El algoritmo diagnóstico de las últimas guías internacionales(3) ubica al análisis de los multímeros en el puesto número 7, sugiriendo su utilidad en aquellos pacientes con VWF menor a 30% o entre 30 y 50% con historia de sangrado en los que la prueba funcional de VWF asociada a una actividad de unión a plaquetas arroje un resultado significativamente menor al nivel antigénico (relación actividad/antígeno < 0.7), es decir para la identificación del tipo de VWD 2. Si bien la determinación de multímeros de VWF es una de las técnicas que se pueden utilizar a la hora de determinar subtipos de VWD, la metodología habitual es laboriosa, y requiere de personal especializado para su correcta interpretación. Debido a esto, la aparición de un kit comercial semi automatizado plantea una alternativa para que más laboratorios de Hemostasia puedan llevar a cabo el ensayo, como fue demostrado en un estudio preliminar publicado(11).
Con respecto a las muestras analizadas pudimos observar que aquéllas que correspondían a pacientes con SMP-T y AVWS presentaron disminución de HMWM, lo que concuerda con lo publicado en AVWS asociado a síndromes mieloproliferativos crónicos (trombocitemia esencial y policitemia vera) en los que se observan cocientes VWF:RCo/VWF:Ag <0,7, presentando un fenotipo de VWD 2 con disminución de HMWM. El mecanismo de esta alteración ha sido postulada como adsorción del VWF a GPIb aberrante expresada en las plaquetas en SMP JaK-2 positivo y mecanismos de proteólisis, correlacionando la disminución de los HMWM junto con la disminución de la actividad del VWF dependiente de su unión a plaquetas de manera negativa y moderada con el recuento plaquetario(12).
Aquellas muestras que pudieron ser evaluadas con ambas técnicas, como fueron las correspondientes a VWD tipo 1, 2A, 2B, 2M y PTT, presentaron total concordancia del perfil multimérico con ambas metodologías. En las muestras VWD 2A los perfiles multiméricos de ausencia de HMWM fueron coincidentes con lo esperable en estas variantes. En las muestras de VWD 2M también hubo concordancia, aún en una muestra con un perfil multimérico inusual, la muestra homocigota p.Glu1549Lys, VGCE ya descripta por autores del presente trabajo en los que se postula un mecanismo no conocido, probablemente con disminución de sobrevida del VWF(9). Sólo en una muestra de un paciente heterocigota para una mutación p.Arg1374Cys se observó una estimación semicuantitativa de los HMWM ligeramente diferente.
En los pacientes con VWF 2B el método semiautomático demostró buena concordancia con el de referencia, aún en la muestra de un paciente con la mutación p.Pro1266Leu en heterocigosis en el que el patrón multimérico está conservado. Este patrón hallado en la posición Pro1266 ha sido descripto en la literatura como variante 2B con menor tasa de formas circulantes que pegan GP1b, menor tasa de trombocitopenias y menor sangrado(13).
Pikta y col. analizaron muestras de pacientes con distintos tipos de VWD, alcanzando perfiles similares a los observados en nuestro estudio(11).
Se ha publicado un análisis exhaustivo más reciente de este método semiautomatizado en un gran número de muestras (>400) de pacientes ya diagnosticados previamente con distintos tipos de VWD de acuerdo a pruebas estándares: VWF:Ag, VWF:RCo, capacidad del VWF de unir colágeno (VWF:CB), cocientes de actividad/antígeno y agregación inducida por ristocetina a baja concentración para detectar hiperagregabilidad plaquetaria a dicha concentración del agonista(14). Además, se han estudiado muestras tomadas durante las pruebas de desmopresina en pacientes con VWD, muestras de pacientes con AVWS, con PTT y controles de calidad externo llevado a cabo en un período de 3 años. En el mismo se demostró que los patrones obtenidos mostraron alta coincidencia con los esperables para el subtipo provisional asignado(14).
En un estudio realizado en 2 laboratorios europeos que analizaron individuos normales, VWD tipo 1, 2A, 2B, 2M, 2N, PTT y AVWS, así como muestras post desmopresina, obtuvieron una concordancia del 91% entre los realizados por el método desarrollado local (“in house”) y el método semiautomático Hydragel 11 (Hydrasys), con algunas discordancias en pacientes con VWD 2 con más de una mutación y en un 20% de los pacientes con AVWS(15). Destacan la utilidad de la densitometría para poder mejorar la apreciación de los geles con respecto de la inspección visual. En ese estudio 2 muestras con VWD 2M en pacientes relacionados con la mutación p.Arg1374Cys demostraron disminución de los HMWM con la técnica semiautomática, pero no con la técnica tradicional local, resultado que está en concordancia con los resultados en la muestra discordante descriptos en el presente estudio.
Los estudios mencionados han planteado ventajas del método, como son la estandarización de la técnica, el menor tiempo y la menor complejidad de procesamiento, así como la baja variabilidad interensayo observada y la intra e interensayo relatada(15). Como desventajas se postula el hecho de que no se discriminan los tripletes debido a que usan una sola concentración de agarosa 2%.
Si bien se considera a la técnica de VWF:CB como un subrogante de la presencia de HMWM, se ha demostrado que los resultados del ensayo no sólo dependen del tipo de colágeno utilizado sino, además, del dominio en el que se localiza la VGCE, y se postula que el VWF:CB no reemplaza al análisis de multímeros y que ambos ensayos deben realizarse para lograr una clasificación diagnóstica correcta de VWD(16).
La debilidad de nuestro estudio está dada por aquellas muestras que sólo fueron evaluadas por el método semiautomatizado, como es el caso de las que presentaron diagnóstico de AVWS, así como dos muestras con VWD tipo 2 sin clasificar y una probable VWD tipo 2N, además del reducido número de muestras analizadas. Por otro lado, la fortaleza del trabajo está dada por la evaluación de muestras con VWD tipo 1 y tipo 2, que fueron estudiadas en un centro de referencia con amplia experiencia en el diagnóstico y tratamiento de la VWD, no sólo con un método de detección de multímeros ampliamente validado, sino también con VGCE detectadas.
Concluimos que el método semicuantitativo-semiautomático evaluado, Hidragel 5, es útil y postulamos que el método semiautomático parece apropiado como tamizaje de perfiles multiméricos de VWF en laboratorios clínicos de Hemostasia.
Bibliografía
1. Woods AI, Blanco AN, Kempfer AC y col. Factor von Willebrand y Enfermedad de von Willebrand: nuevos enfoques diagnósticos. Acta Bioquím Clín Latinoam. 2016;50:273-289.
2. Stockschlaeder M, Schneppenheim R, Budde U. Update on von Willebrand factor multimers: focus on high molecular-weight multimers and their role in hemostasis. Blood Coagul Fibrinolysis. 2014, 25:206-216.
3. James PD, Connell NT, Ameer B y col. ASH ISTH NHF WFH 2021 guidelines on the diagnosis of von Willebrand disease. Blood Adv. 2021; 12:280-300.
4. Ledford-Kraemer MR. Analysis of von Willebrand factor structure by multimer analysis. Am J Hematol. 2010;85(7):510-514.
5. Favaloro EJ, Pasalic L, Curnow J. Laboratory tests used to help diagnose von Willebrand disease: an update. Pathology. 2016;48:303-318.
6. Oliver S, Edwin Lau KK, Chapman K, Favaloro EJ. Laboratory Testing for Von Willebrand Factor Multimers. Methods Mol Biol. 2017;1646:495-511.
7. Favaloro EJ, Oliver S. Evaluation of a new commercial von Willebrand factor multimer assay. Haemophilia. 2017;23:e373-e7.
8. Farías C, Kempfer AC, Blanco A, Woods A, Lazzari MA. Visualization of the multimeric structure of von Willebrand factor by immunoenzymatic stain using avidin-peroxidase complex instead of avidin-biotin peroxidase complex. Thromb Res. 1989;53(5):513-518.
9. Woods AI, Paiva J, Primrose DM, Blanco AN, Sánchez-Luceros A. Type 2A and 2M von Willebrand Disease: Differences in Phenotypic Parameters According to the Affected Domain by Disease-Causing Variants and Assessment of Pathophysiological Mechanisms. Semin Thromb Hemost. 2021;47:862-874.
10. Woods AI, Kempfer AC, Paiva J y col. Phenotypic Parameters in Genotypically Selected Type 2B von Willebrand Disease Patients: A Large, Single-Center Experience Including a New Novel Mutation. Semin Thromb Hemost. 2017;43: 92-100.
11. Pikta M, Zemtsovskaja G, Bautista H y col. Preclinical evaluation of a semi-automated and rapid commercial electrophoresis assay for von Willebrand factor multimers. J Clin Lab Anal. 2018;32:e22416.
12. Franchini M, Mannucci PM. Acquired von Willebrand Syndrome: focused for hematologists. Haematologica. 2020;105:2032-2037.
13. Federici AB, Mannucci PM, CastamanG y col. Clinical and molecular predictors of thrombocytopenia and risk of bleeding in patients with von Willebrand disease type 2B: a cohort study of 67 patients. Blood. 2009;113:526-534.
14. Oliver S, Vanniasinkam T, Mohammed S, Vong R, Favaloro EJ. Semi- automated von Willebrand factor multimer assay for von Willebrand disease: Further validation, benefits and limitations. Int J Lab Hematol. 2019;41:762-771.
15. Bowyer AE, Goodfellow KJ, Seidel H y col. Evaluation of a semi-automated von Willebrand factor multimer assay, the Hydragel 5 von Willebrandmultimer, by two European Centers. Res Pract Thromb Haemost. 2018;2:790-799.
16. Woods AI, Paiva J, Primrose DM, Blanco AN, Sanchez-Luceros A. Von Willebrand disease type 2M: Correlation between genotype and phenotype: Comment from Woods et al. J Thromb Haemost. 2022;20:1022-1023.