Emicizumab e inmunotolerancia en paciente con hemofilia A e inhibidores: reporte de caso en Ecuador.
Emicizumab and immunotolerance induction in a patient with hemophilia A and inhibitors: a case report in Ecuador
Chiang H1; González MC2; Rodríguez G3; Ullauri V1; Villa E1
1 Unidad de Hematología, Hospital Regional José Carrasco Arteaga, Cuenca, Ecuador.
2 Unidad de Reumatología, Hospital Regional José Carrasco Arteaga, Cuenca, Ecuador.
3 Área de Enfermería del Centro de Biológicos y Terapia Autoinmune, Hospital Regional José Carrasco Arteaga, Cuenca, Ecuador.
Palabras claves: emicizumab,
inmunotolerancia,
hemofilia.
Keywords: emicizumab,
immunotolerance,
hemophilia.
Resumen
Presentamos el caso de un niño de 9 años con hemofilia A e inhibidores de alto título, con criterios de respuesta posterior a inmunotolerancia (ITI) asociado a emicizumab. Esta estrategia contribuyó a un mejor control de los sangrados, permitió intensificar el régimen de fisioterapia y favoreció en su calidad de vida.
En el Ecuador la realización de la inmunotolerancia conlleva una serie de dificultades: costos elevados, provisión del factor de forma ininterrumpida, conformación de un equipo multidisciplinario, laboratorios que se encarguen de la titulación de inhibidores, o la autorización para el uso de fármacos que no se encuentran en el cuadro nacional de regulación.
Debemos establecer cuál es el mejor perfil clínico de aplicación y el impacto económico de estas terapias innovadoras (emicizumab, concizumab, fitusiran), sobre todo en nuestro medio, en el que la accesibilidad a los fármacos es compleja y la optimización de recursos es la norma.
Abstract
We present the case of a 9-year-old boy with hemophilia A and high titer inhibitors, with post-immunotolerance induction response criteria (ITI) associated with emicizumab. This strategy contributed to a better control of bleeding, allowed to intensify the physical rehabilitation regimen and notably favored his quality of life.
In Ecuador, carrying out immunotolerance entails a series of difficulties: high costs, uninterrupted provision of the factor, formation of a multidisciplinary team, laboratories that are responsible for the titration of inhibitors, or the authorization for the use of drugs that are not in the national regulatory framework.
We must establish the best clinical application profile and the economic impact of these innovative therapies (emicizumab, concizumab, fitusiran);
especially in our environment, in which accessibility to drugs is complex and optimization of resources is the norm.
Introducción
Tomando como referencia el Informe del Sondeo Mundial Anual 2020 de la Federación Mundial de Hemofilia (WFH) publicado en octubre 2021, en el Ecuador, con una población de 17.643.060 de habitantes, existen 1708 casos con hemofilia, 99 casos con enfermedad de von Willebrand y 7 casos con otros trastornos de la coagulación. Dentro del grupo de hemofilia A, 21 pacientes se encuentran con inhibidores activos, y existe un registro de 2 nuevos casos de inhibidores en relación a la notificación previa.
En el Ecuador la realización de la inmunotolerancia en los pacientes con hemofilia e inhibidores conlleva una serie de dificultades: costos elevados, provisión del factor de forma ininterrumpida, conformación de un equipo multidisciplinario, laboratorios que se encarguen de la titulación de inhibidores, o la autorización para el uso de fármacos que no se encuentran en el cuadro nacional de regulación.
El advenimiento de las terapias no factor está suscitando una reevaluación de conceptos en hemofilia en sus diversos ámbitos, a tal grado de cuestionarnos si la ITI es útil y aplicable, o si es el fin de la era de los concentrados de factor(5,8). Justamente en los pacientes con hemofilia A e inhibidores que fracasan o no se someten a ITI, la WFH recomienda la profilaxis con emicizumab sobre los agentes bypass(6).
Uno de los argumentos a favor de erradicar el inhibidor se basa en que los pacientes que reciben emicizumab son requirentes en algún momento de tratamiento hemostático, bien sea para el control de hemorragias, traumatismos o cirugías(1,3).
Emicizumab es un anticuerpo monoclonal biespecífico, humanizado, que une el FIX activado y el factor X (FX), dando como resultado la generación de FX activado (FXa), que luego cataliza la formación de trombina a partir de la protrombina(1,4).
La FDA y la EMA, fundamentados en los ensayos clínicos HAVEN 1-4, aprobaron el uso de emicizumab como profilaxis en hemofilia A (con y sin inhibidores), tanto en adultos/adolescentes (>12 años) como en pediátricos (<12 años)(2). En los análisis primarios como en el seguimiento a largo plazo, emicizumab generó reducciones estadística y clínicamente significativas en las tasas de hemorragia anuales, comparado con la profilaxis con factor VIII (en pacientes sin inhibidores) y con agentes bypass (en pacientes con inhibidores). Estos ensayos excluyeron pacientes en ITI.
Caso clínico
Niño de 9 años con hemofilia A con inhibidores de título alto con el siguiente historial:
- Diagnóstico de hemofilia A severa a los 8 meses de edad (por presencia de hematomas en la ingle de aparición espontánea).
- Profilaxis con factor VIII plasmático: 25 UI/Kg 2-3 veces por semana (de forma escalonada) al año de edad aproximadamente.
- Detección de inhibidor: 239 UB (marzo 2014) a los 2 años de edad.
- Antecedentes familiares: ninguno
Examen físico (valoración por Reumatología/Fisiatría):
- Arco cervical conservado, rangos conservados en cintura escapular. EVA dolor 10/10. Presencia de sinovitis en rodilla izquierda y articulaciones tibioastragalinas (bilateral). DAS28: 4,26 (actividad moderada). HAQ: 1.50 (capacidad funcional afectada severamente). Marcha asistida con muleta axilar derecha (se desplazaba en silla de ruedas). Escala funcional IV.
- Rodilla izquierda: en flexión con amplitudes articulares, flexión 105 grados/extensión -35 grados. Deformidad en flexión de la rodilla izquierda de 20 grados.
- Rodilla derecha: flexión 120 grados/extensión 0 grados, dolor a la palpación en rodilla izquierda y en tobillo izquierdo, con flexión dorsal de 10 grados y plantar de 10 grados.
- Articulaciones diana: rodilla izquierda.
- Puntaje de salud articular para la hemofilia (HJHS): 33.
- Puntaje de Independencia Funcional en Hemofilia (FISH): 14.
Evolución previo a inicio de inmunotolerancia:
1) Sangrados articulares con requerimiento hospitalario: 4-8 sangrados por año con manejo con factor VIIa recombinante (rFVIIa) a dosis de 90 ug/Kg cada 2-3 horas hasta control del evento.
2) Manejo de vías: cámara implantable venosa (2015) con retiro por infección por K. pneumoniae, cámara implantable venosa (2016) con retiro por infección por Haemophilus haemolyticus. Port a Cath (2016 hasta la actualidad).
3) Internación en UCI pediátrico por neumonía de la comunidad con criterios de severidad (2016).
4) Se realizó radiosinoviortesis (2 en la rodilla izquierda, y 1 en el tobillo izquierdo) en Brasil.
Inmunotolerancia:
- Fecha de inicio: marzo 2019 (edad: 6 años).
- Tipo de producto: factor VIII plasmático.
- Esquema de ITI: 100 UI/Kg/día (3 veces por semana).
- Título de inhibidor (pico histórico) previo al inicio de ITI: 239 UB (marzo 2014).
- Título de inhibidor previo al inicio de ITI: 3.60 UB.
- Tiempo desde la detección del inhibidor hasta el inicio de ITI: 5 años.
- Vía de acceso inicial: Port a Cath.
Evolución durante la ITI:
1) Se generó una reacción anamnésica al inicio, con una titulación de inhibidores de 153 UB con posterior descenso (Figura 1).
2) Presentó 3 episodios de hemartrosis con internación hospitalaria con manejo con factor VIIa recombinante VIIa (rFVIIa) a dosis de 90 ug/Kg cada 2-3 horas hasta control del evento.
En junio del 2021 bajo autorización ministerial se inició el tratamiento con emicizumab:
- Presentación: ampollas 30 mg/ml, ampollas 105 mg/0.7 cc.
- Dosis de carga: 3 mg/Kg cada semana por 4 semanas.
- Dosis de mantenimiento: 3 mg/kg c/15 días.
- Reacción: eritema.
Figura 1
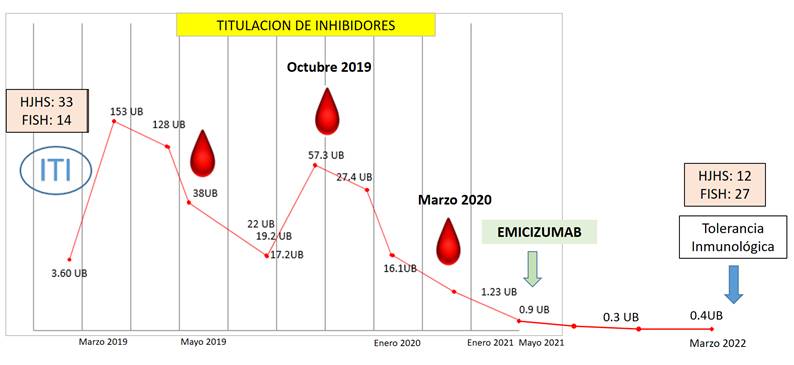
Resultados de laboratorio posterior a inicio de emicizumab:
- Inhibidores o anticuerpos anti-factor VIII cromogénico: 0.4 UB (0-0-6 UB) (enero 2022).
- Inhibidores o anticuerpos anti-factor VIII cromogénico: 0.3 UB (0-0-6 UB) (marzo 2022).
- Dosificación factor VIII cromogénico bovino: 53.2 UI/dL (60 - 168 UI/dL) (marzo 2022) (valoración farmacocinética).
Discusión
Nuestro paciente, previo a la ITI, exhibió factores predictivos de alto riesgo y de pobre pronóstico(3). A día de hoy las recomendaciones son de establecer la ITI apenas se detecte el inhibidor independientemente del título(6).
En marzo del 2019 se comenzó el tratamiento con el mismo producto con el cual se desarrollaron los inhibidores, presentando reducciones cercanas al 20% en las titulaciones realizadas en cada período de 3-6 meses, pero con repuntes posteriores a cada episodio de hemartrosis.
Los cuadros emergentes se manejaron con factor VIIa recombinante (rFVIIa), con el impedimento de su uso para profilaxis.
En junio del 2021, bajo autorización ministerial, se incorporó emicizumab a la ITI. Durante las dosis de carga presentó eritema en la zona de aplicación con resolución posterior, y el intervalo en la dosis de mantenimiento se instauró en base al peso y a la presentación de las ampollas, con la finalidad de optimizarlas. Esta estrategia contribuyó a un mejor control de los sangrados, lo que permitió intensificar el régimen de fisioterapia (HJHS: 12) y, por ende, favoreció su calidad de vida (FISH: 27).
El Protocolo Atlanta fue uno de los primeros trabajos que implementó la profilaxis de emicizumab asociado a ITI a bajas dosis(5), esquema aplicable a nuestros sistemas sanitarios por las ventajas que nos puede otorgar (reducción de costos, limitación en el uso de catéteres venosos centrales), pero requirente de trabajos a mayor escala para corroborar sus resultados. Entre los estudios en curso se encuentra MOTIVATE e INHIBIT.
Emicizumab interfiere tanto en la medición del FVIII:C como del inhibidor del factor VIII, aconsejándose el análisis de Bethesda cromogénico del factor VIII bovino. En el Ecuador estamos desprovisto de esta metodología, por lo que las muestras fueron procesadas en Colombia(6).
En marzo del 2022 nuestro paciente cumplimentó criterios de respuesta completa de tolerancia inmunológica. El enfoque tradicional posterior es la reducción gradual del factor VIII, tanto en la dosis como en frecuencia, pero en el escenario suscitado, nos conlleva a plantear las siguientes interrogantes:
- ¿Se debe mantener la profilaxis con emicizumab?
- ¿Se debe mantener la profilaxis con emicizumab y factor VIII a bajas dosis?
- ¿Puede generarse la recurrencia del inhibidor al suprimirse la administración del factor VIII(7)?
Existen trabajos en progreso, como el PRIORITY, que aleatoriza pacientes con inhibidor de alto título que hayan respondido a ITI a recibir emicizumab solo o emicizumab más FVIII semanal (50 U/Kg). Al igual que propuestas como la del grupo FIT, que sugiere conservar el emicizumab con el factor VIII con un mínimo de infusiones con frecuencia semanal al menos por 6 meses; y posteriormente de manera quincenal por otros 6 meses(3).
Dado la carencia de evidencia al respecto, proseguimos con el emicizumab y establecimos disminuir las dosis de factor VIII hasta una pauta intermedia de profilaxis (15-25 UI/Kg), asociada a la menor frecuencia posible (1-2 veces por semana), quedando pendiente precisar la duración de la estrategia.
Conclusión
Emicizumab y los fármacos rebalanceadores de la hemostasia están revolucionando el ámbito de hemofilia, lo que ha ampliado el margen de escenarios clínicos y, por ende, resulta que tenemos muchas preguntas sin respuestas de certeza (al menos hasta que los estudios en desarrollo y la evidencia acumulada nos suministren mejores directrices).
Debemos establecer cuál es el mejor perfil clínico de aplicación y el impacto económico de estas terapias, sobre todo en nuestro medio, en el que la accesibilidad a los fármacos es compleja y la optimización de recursos es la norma.
Conflictos de interes: Los autores declaran no poseer conflictos de interes.
Agradecimientos:
-Al personal de enfermería del Centro de Biológicos y Terapia Autoinmune, del Hospital Regional José Carrasco Arteaga de Cuenca, Ecuador.
-A la Unidad de Hematología del Hospital Pediátrico Baca Ortiz de Quito, Ecuador.
-A los siguientes profesionales: Dr. Saturnino Haya Guaita (Hematología-España), Dra. Katherine Estévez (Pediatría-Endocrinología), Dra. Gloria Ramos (Bacteriología-Colombia), Dra. Verónica Goyo (Farmacología).
- A todos los hematólogos y personal sanitario que colaboraron previamente en el manejo del paciente.
Bibliografía
1. Alvarez Roman M. Guías Españolas para el manejo de la hemophilia. 2022, 1-190.
2. Callaghan M, Negrier C, Paz-Priel I, Chang T, Chebon S y col. Long-term outcomes with emicizumab prophylaxis for hemophilia A with or without FVIII inhibitors from the HAVEN 1-4 studies. Blood. 2021;137(16):2231-2242.
3. Carcao M, Escurriola C, Santagostina E, Oldenburg J, Liesner R y col. The changing face of immune tolerance induction in haemophilia A with the advent of emicizumab. Haemophilia. 2019;25:676-684.
4. Ellsworth P, Ma A. Factor-mimetic and rebalancing therapies in hemophilia A and B: the end of factor concentrates? Hematology Am Soc Hematol Educ Program. 2021, Dec 10;2021(1):219-225.
5. Holstein K, Le Quellec S, Klamroth R, Batorova A y col. Immune tolerance induction in the era of emicizumab – still the first choice for patients with haemophilia A and inhibitors? Haemophilia. 2022 Mar;28(2):215-222.
6. Srivastava A, Santagostino E, Dougall A, Kitchen S, Sutherland M y col. WFH Guidelines for the Management of Hemophilia, 3rd edition. Haemophilia. 2020 Aug;26 Suppl 6:1-158.
7. Young G. Implementing emicizumab in hemophilia inhibitor management: emicizumab should be prescribed after tolerance. Blood Advances. 2018;2:2780-2782.
8. Young G. Management of children with hemophilia A: How emicizumab has changed the landscape. Journal of Thrombosis and Haemostasis. 2021 Jul;19(7):1629-1637.