Estudio comparativo de 4 métodos de dímero D en una serie de muestras de pacientes COVID-19
Comparative study of 4 D-dimer methods in a samples serie of COVID-19 patients
Rosa C1, Zirpoli M1, Sueldo E2, Arias M2, Ceresetto J3, Duboscq C3
1. Laboratorio del Hospital Universitario Austral. Pilar. Argentina.
2. Laboratorio de la Unidad Asistencial Dr. César Milstein. CABA. Argentina.
3. Laboratorio del Servicio de Hematología del Hospital Británico. CABA. Argentina.
Mail de contacto: crosa@cas.austral.edu.ar
Palabras claves: dímero D,
COVID-19,
SARS-CoV-2.
Keywords: D-dimer,
COVID-19,
SARS-CoV-2.
Resumen
El objetivo del trabajo fue evaluar la correlación de los resultados de dímero D (DD) obtenidos en una serie de muestras de pacientes COVID-19 por los 4 métodos utilizados en 3 laboratorios. Población: 39 pacientes consecutivos con rt-PCR positiva para COVID-19, ingresados al Hospital Universitario Austral (HUA) y Hospital Solidario COVID Austral, en octubre 2020; 22 hombres y 17 mujeres. Edad: 12-82 años, con una media de 52 años. Las 46 muestras de plasma citratado obtenidas fueron procesadas inmediatamente en el centro 1 (HUA), alicuotadas y congeladas a -70°C para su derivación a los otros centros. Determinación de DD: Centro 1: VIDAS® DEX2, equipo VIDAS 3 (BioMérieux) (Método A). Centro 2: Innovance D-dimer, equipo CS 2500 (Siemens) (Método B). En el centro 3 fueron procesadas por Liatest DDi plus, equipo STA Compact Max (Stago) (Método C) y por HemosIL D dimer, equipo ACL TOP 500 (Instrumentation Laboratory) (Método D). Para el análisis estadístico se utilizó el EP Evaluator®: comparación de múltiples instrumentos y comparación de 2 instrumentos. Los niveles de DD encontrados para el método A: media 3833 ng/ml FEU (rango: 170-34.390); método B: media: 4567 ng/ml FEU (180-36.910); método C: media: 3916 ng/ml FEU (189-28.520); método D: media: 3429 ng/ml FEU (230-15.046) (se convirtió el resultado obtenido en unidades DD a unidades FEU utilizando un factor de conversión 2). La prueba de comparación de múltiples instrumentos, utilizando un Error Total permitido (ETa) de 34.53%, calculado por variabilidad biológica mínima para el método A (considerado de referencia), mostró que las diferentes metodologías no eran comparables. Al comparar cada una de las metodologías B, C y D vs A, la comparación VIDAS® DEX2 vs Liatest DDi plus mostró un coeficiente de correlación: (R) 0,9501, pendiente: 0,941 (0,850-1,031), intercepto: 310,1 (-375,5-995,8). El resto de las comparaciones mostraron coeficientes de correlación menores de 0.86. Si bien hubo una coincidencia del 80% (37/46) entre las diferentes metodologías cuando se compararon pacientes con valores mayores al nivel de corte (500 ng/ml FEU), la proporción del aumento de DD respecto al límite superior normal (LSN) fue diferente para cada método. Por lo tanto, en nuestra serie de muestras de pacientes COVID-19, los 4 métodos para la determinación cuantitativa de DD no son comparables, coincidiendo con lo descripto en la bibliografía para otras patologías. Por este motivo no se deberían extrapolar valores de corte absolutos o en función del LSN entre los diferentes métodos.
Abstract
The aim of this study was to evaluate the correlation of D-Dimer (DD) results obtained in a series of samples from COVID-19 patients by 4 methods used in 3 laboratories. Population: 39 consecutive patients with positive rt-PCR for COVID-19, admitted to Hospital Universitario Austral (HUA) and Hospital Solidario COVID Austral, in October 2020; 22 men and 17 women. Age: 12-82 years, with an average of 52 years. The 46 citrated plasma samples obtained were immediately processed in center 1 (HUA), aliquoted and frozen at -70 ° C for their referral to the other centers. Determination of DD: Center 1: VIDAS® DEX2, VIDAS 3 unit (BioMérieux) (Method A). Center 2: Innovance D-dimer, in CS 2500 (Siemens) (Method B). In center 3, they were processed by Liatest DDi plus, in STA Compact Max (Stago) (Method C) and by HemosIL D dimer, in ACL TOP 500 (Instrumentation Laboratory) (Method D). The EP Evaluator® was used for statistical analysis: comparison of multiple instruments and comparison of 2 instruments. The levels of DD found for method A: mean 3833 ng / ml FEU (range: 170-34,390); method B: mean: 4567 ng / ml FEU (180-36,910); method C: mean: 3916 ng / ml FEU (189-28,520); method D: mean: 3429 ng / ml FEU (230-15.046) (the result obtained in DD units was converted to FEU units using a conversion factor of 2). The multiple instrument comparison test, using a Total Allowable Error (TEa) of 34.53%, calculated by minimal biological variability for method A (considered as reference), showed that the different methodologies were not comparable. When comparing each of the methodologies B, C and D vs A, the comparison VIDAS® DEX2 vs Liatest DDi plus showed a correlation coefficient: (R) 0.9501, slope: 0.941 (0.850-1.031), intercept: 310, 1 (-375.5-995.8). The rest of the comparisons showed correlation coefficients less than 0.86. Although there was an 80% (37/46) agreement between the different methodologies when comparing patients with values greater than cut off (500 ng / ml FEU), the proportion of the increase in DD with respect to the upper limit of normal (ULN) was different for each method. Therefore, in our series of COVID-19 patient samples, the 4 methods for the quantitative determination of DD are not comparable, coinciding with what is described in the bibliography for other pathologies. For this reason, absolute or ULN cutoff values should not be extrapolated between the different methods.
Introducción
El dímero D (DD) es un marcador de activación de la coagulación y de la fibrinólisis. El mismo se produce a partir del fibrinógeno, por la acción secuencial de la trombina, el factor XIII activado (FXIIIa) y la plasmina. Como resultado se obtienen un conjunto heterogéneo de productos de degradación de la fibrina, con distintos pesos moleculares y que contienen por lo menos un enlace entre dos dominios D de dos moléculas de fibrinógeno(1-2). El ensayo de DD es una herramienta del laboratorio útil para excluir enfermedad tromboembólica venosa en pacientes con probabilidad clínica baja o moderada, según índices de Wells o Ginebra, en donde la determinación de DD tiene un alto valor predictivo negativo(3). Debido a la importancia de esta prueba de laboratorio en la toma de decisiones clínicas, un número considerable de diferentes ensayos de DD han sido desarrollados por la industria de diagnóstico. Los mismos varían desde inmunoensayos enzimáticos clásicos y avanzados a inmunoensayos con látex, y también se han desarrollado métodos de tipo “Point Of Care Test” (POCT). Los ensayos de última generación son fáciles de realizar y se pueden adaptar en la rutina de los autoanalizadores de laboratorio. De acuerdo con los resultados de la encuesta sobre DD en Latinoamérica realizada por el Subcomité de Alteraciones de la Fibrinólisis del Grupo Cooperativo Latinoamericano de Hemostasia y Trombosis (Grupo CLAHT), presentados en el XXVI Congreso del Grupo CLAHT de Costa Rica en 2019, los ensayos de laboratorio más utilizados son los inmunoturbidimétricos (62%) y enzimoinmunoensayos con fluorescencia ELFA (Enzyme-Linked Immunofluorescence Assay) (14%)(4). Los ensayos para el antígeno DD utilizan anticuerpos monoclonales que reaccionan con los epitopes encontrados en el fragmento DD de la fibrina, pero no con el dominio D del fibrinógeno u otros productos de degradación del fibrinógeno. Los anticuerpos reaccionan con los epitopes conformacionales generados por el enlace inducido por el FXIIIa de los dominios D adyacentes dentro de un polímero de fibrina. Para algunos anticuerpos monoclonales, la degradación de la fibrina reticulada por la plasmina es un requisito adicional para la generación del epitope. En muestras clínicas de plasma, los ensayos detectan una variedad de compuestos de degradación de la fibrina de diferentes pesos moleculares, incluido el fragmento DD, así como productos de degradación de fibrina de mayor peso molecular y oligómeros X de la fibrina. Debido a las diferencias en la reactividad del epitope, la armonización de los ensayos de DD sólo se puede lograr con calibradores que contengan una variedad similar de productos derivados de la fibrina reticulada. Aunque los diferentes ensayos de DD son ampliamente utilizados con éxito, la falta de comparabilidad entre los diferentes métodos ha sido observada tanto en estudios clínicos como en los resultados de los programas de evaluación externa de la calidad. Esto dificulta el intercambio de resultados del mismo paciente entre diferentes laboratorios utilizando diferentes métodos, así como la comparación de los resultados de diferentes estudios clínicos. Esta variación numérica en los resultados de las pruebas se debe principalmente a la heterogeneidad de los productos de degradación de la fibrina en muestras de pacientes y la diferente especificidad de los distintos anticuerpos utilizados en los ensayos disponibles comercialmente para DD. Aunque este problema es complejo, existe la necesidad de lograr la comparabilidad de los resultados de las pruebas del DD. Aunque se han hecho numerosos esfuerzos, hasta el momento no se ha logrado estandarizar ni tampoco armonizar los resultados de estos ensayos(5-7).
En los distintos ensayos se utilizan dos tipos de calibradores y, en consecuencia, existen dos tipos de unidades en que se expresan los resultados de DD: las unidades equivalentes de fibrinógeno (FEU en inglés), y las unidades dímero D (DDU en inglés). Las unidades DDU expresan el peso del fragmento de DD propiamente dicho, en cambio las unidades FEU expresan el peso del fragmento en términos del fibrinógeno convertido en fibrina, de la cual el DD proviene. Además los resultados se expresan en distintas unidades de concentración: ng/mL, mg/L, μg/mL y otras. El Clinical and Laboratory Standards Institute (CLSI) es una organización sin fines de lucro que promueve el desarrollo y el uso de normas y pautas de consenso de laboratorio. Según la guía CLSI H59: “A Quantitative D-dimer for the Exclusion of Venous Thromboembolic Disease”, los resultados deben informarse en las unidades que especifica el fabricante y no deben convertirse(8).
Dímero D y COVID-19. Los pacientes con la infección moderada o severa por el SARS-CoV-2 pueden presentar en su evolución una coagulopatía asociada al COVID-19 o CAC, que se caracteriza por un estado protrombótico. El DD ha sido propuesto como un marcador de laboratorio de utilidad pronóstica al ingreso y durante la internación como marcador de severidad de la enfermedad. Diferentes estudios han encontrado niveles de DD elevados de forma significativa en pacientes con COVID-19 grave, en comparación con aquéllos cuyos síntomas fueron más leves y con los sujetos sanos: Lippi y Plebani(9) informaron que el DD estuvo aumentado en un 36-43% de los pacientes según diferentes reportes. Guan y col(10), presentaron en New England Journal of Medicine un estudio retrospectivo con 1099 pacientes de 552 hospitales de China, en donde analizaron las características clínicas de la enfermedad provocada por el COVID-19. Los niveles de DD se encontraron elevados en el 46% de todos los pacientes, en el 60% de los pacientes que presentaron enfermedad severa y en el 69% de los pacientes que alcanzaron el punto final primario compuesto: admisión en unidad de cuidados intensivos (UCI), requerimiento de ventilación mecánica o muerte. En un metaanálisis de 23 artículos publicado en junio del 2020 por Bao y col(11), el DD estuvo aumentado en un 29%, 534 de 1845 pacientes. En los casos severos el DD estuvo elevado 2.74 veces, con respecto a los no severos (1.29 vs 0.47 mg/L). En un análisis "pooleado" realizado a partir de 4 estudios y publicado por Lippi y Favaloro(12), propusieron que un DD de 3.0 mg/L o 6 veces el límite superior normal (LSN) podría ser considerado como valor de corte de severidad de la enfermedad. Zhou y col(13) analizaron el curso clínico y los factores de riesgo para mortalidad en un estudio de cohorte retrospectivo con 191 pacientes internados con COVID-19 en China. Encontraron que en un análisis multivariado los pacientes con un DD >1 ug/ml al ingreso o 2 veces el LSN tenían 18 veces más riesgo de mortalidad, con un p valor significativo (p=0.0033). En abril 2020, Zhang y col(14), en los 343 pacientes analizados, encontraron que la mortalidad hospitalaria fue significativamente mayor (HR: 51.5, p<0.001) en pacientes con DD ≥ 2.0 μg/ml o 4 veces el LSN al ingreso, que en aquéllos que tenían DD < 2.0 μg/ml al ingreso. Hasta este momento la recomendación de los expertos de monitorizar los niveles de DD al ingreso y cada 24-48h, como herramienta en la evaluación del pronóstico y de la progresión de la enfermedad tuvo una fuerza de recomendación débil a favor(15). En otro estudio retrospectivo presentado por Lodigiani y col(16), pudimos observar la evolución de los valores de dímero D de 388 pacientes durante la internación en un hospital académico de Milán, comparando los resultados obtenidos en distintos escenarios en los pacientes sobrevivientes y no sobrevivientes (Tabla 1).
Tabla 1. Medianas e intervalos (Q1-Q3) de dímero D en pacientes internados sobrevivientes y no sobrevivientes, expresados en ng/ml FEU(16).

Adaptado de Lodigiani et al. Thrombosis Research 191 (2020):9-14.
Otro trabajo sobre el valor pronóstico del DD en pacientes hospitalizados con COVID-19, fue publicado en agosto 2020 por Berger y col(17), en el que estudiaron 2377 pacientes adultos en un sistema hospitalario de New York. El 76% tuvo valores mayores al punto de corte del método al ingreso (DD>230 ng/ml DDU). Los pacientes que presentaron valores de DD elevados al ingreso tuvieron 2.4 veces (aOR) más probabilidad de tener enfermedad crítica que aquéllos con DD normal al ingreso (p<0.001). Los resultados de este estudio reforzaron el concepto de que el COVID-19 es una condición coagulopática y que el DD representaba un vínculo directo entre la infección por SARS-CoV-2 y el mal pronóstico.
La International Society of Thrombosis and Haemostasis (ISTH) en su guía interina para el manejo de la coagulopatía asociada al COVID-19, en donde propuso al DD como el marcador de laboratorio más importante para el seguimiento, declararon que si bien no es posible establecer un valor de corte, 3 a 4 veces el LSN del método puede considerarse como un aumento significativo al ingreso(18).
Un metaanálisis publicado por Nopp y col en setiembre de 2020 demostró que los pacientes que desarrollaron tromboembolismo venoso (TEV) mostraron niveles más elevados de DD(19). En lo que respecta a la utilidad del DD en predecir TEV en pacientes COVID-19 sobrevivientes no mecánicamente ventilados, Nauka y col encontraron que a mayor nivel del biomarcador al ingreso, aumentaba el riesgo de desarrollar TEV y con DD mayor a 5 ug/ml al ingreso los pacientes tuvieron 10.7 veces más riesgo(21).
La guía de diagnóstico, prevención y tratamiento de TEV en COVID-19 del consenso de expertos de la ISTH con respecto a DD declaró que puede NO ser un predictor confiable de TEV, sino más bien un marcador de mal pronóstico. NO recomienda el tamizaje de rutina de TEV basado en niveles elevados de DD. En cuanto a la profilaxis de TEV en pacientes hospitalizados COVID-19 NO internados en UCI, el DD mayor a 6 veces el LSN o DD >6 x LSN, parece ser un predictor consistente de eventos trombóticos y de mal pronóstico. En cuanto a la profilaxis de TEV en pacientes hospitalizados COVID-19 en UCI el DD >6 x LSN, el índice de coagulopatía inducida por sepsis (CIS) ≥4, proteína C reactiva, troponina y otros marcadores del índice de CID, tendrían un valor pronóstico. En lo que respecta a tratamiento de TEV en pacientes hospitalizados COVID-19, no se recomienda cambiar los regímenes de tratamiento basándose únicamente en el DD(21).
Desde el inicio de la pandemia de COVID-19 se han publicado numerosos estudios utilizando diferentes métodos y reactivos de DD y expresando los resultados con diferentes unidades, si bien persiste el problema de la falta de estandarización y armonización de este ensayo. El objetivo de nuestro trabajo fue evaluar si hay correlación de los resultados de DD obtenidos en una serie de muestras de pacientes COVID-19, por 4 métodos utilizados en 3 diferentes laboratorios.
Materiales y métodos
Población: 39 pacientes consecutivos con rt-PCR positiva para COVID-19 ingresados al Hospital Universitario Austral y Hospital Solidario COVID Austral durante el mes de octubre 2020: 22 hombres y 17 mujeres. Edad: entre 12-82 años, con una media de 52 años. Las 46 muestras de plasma citratado de descarte fueron procesadas con el tubo primario en el laboratorio del Hospital Universitario Austral (centro 1). Luego las mismas fueron alicuotadas y congeladas a -70°C para su posterior derivación a los otros centros. La determinación de DD en el centro 1 se realizó con el método VIDAS® DEX2 en equipo VIDAS 3 (BioMérieux) (Método A). En el laboratorio de la Unidad Asistencial Dr. César Milstein (centro 2) se utilizó el método Innovance D-dimer en un equipo CS 2500 (Siemens) (Método B). En el laboratorio del Servicio de Hematología del Hospital Británico (centro 3), fueron procesadas por el método Liatest DDi plus en un coagulómetro STA Compact Max (Stago) (Método C) y también por el método HemosIL D dimer en un coagulómetro ACL TOP 500 (Instrumentation Laboratory) (Método D). En la tabla 2 se resumen los diferentes métodos utilizados en los 3 centros, sus fundamentos y los reactivos y equipos utilizados.
Tabla 2. Métodos y equipamiento utilizados en cada centro.
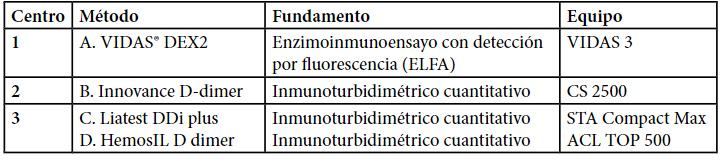
Para el análisis estadístico se utilizó el programa informático EP Evaluator®: comparación de múltiples instrumentos y comparación de 2 instrumentos.
Resultados
En la tabla 3 podemos observar los valores de DD obtenidos por los 4 métodos diferentes, expresados en ng/ml FEU. Los resultados obtenidos en unidades DDU por el método D se convirtieron a unidades FEU utilizando un factor de conversión igual a 2.
Tabla 3. Resultados de DD de los pacientes COVID-19 expresados en ng/ml FEU.
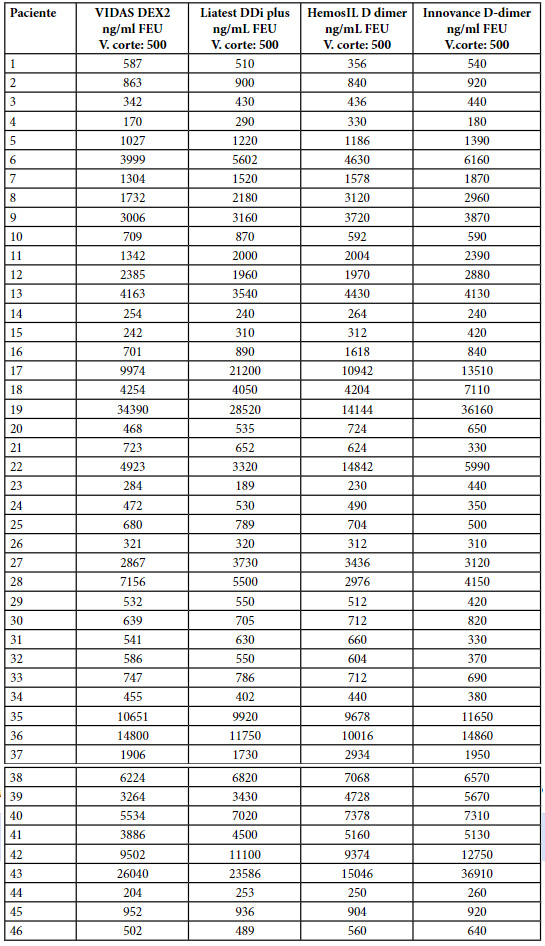
En la tabla 4 se resumen los valores medios calculados y los rangos de DD para los 4 ensayos.
Tabla 4. Valores de DD medios, mínimos y máximos obtenidos por los 4 métodos.

La prueba de comparación de múltiples instrumentos, utilizando un Error Total permitido (ETa) de 34.53%, calculado por variabilidad biológica mínima para el método A (considerado de referencia) mostró que las diferentes metodologías no eran comparables. En la figura 1 podemos ver el gráfico con el índice de error por instrumento.
Figura 1. Indice de error por instrumento en la comparación entre los 4 métodos utilizando EP Evaluator®.
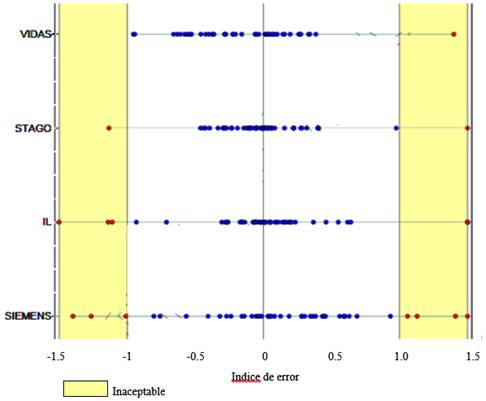
En la figura 2 vemos la curva de regresión de Deming para la comparación de múltiples instrumentos.
Figura 2. Gráfico de comparación entre los 4 métodos utilizando EP Evaluator®.
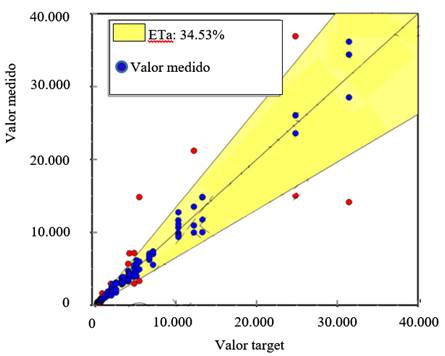
Si bien hubo una coincidencia del 80% (37/46) entre las diferentes metodologías cuando se compararon pacientes con valores mayores al nivel de corte (500 ng/ml FEU), la proporción del aumento de DD respecto al LSN fue diferente para cada método.
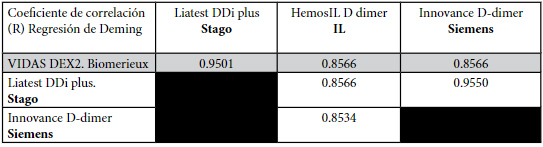
Luego al comparar por pares cada una de las metodologías B, C y D vs A como referencia, el ensayo VIDAS® DEX2 vs Liatest DDi plus mostró un coeficiente de correlación: (R) 0,9501, con una pendiente: 0,941 (0,850 a 1,031), y un intercepto: 310,1 (-375,5 a 995,8). El resto de las comparaciones mostraron coeficientes de correlación menores de 0.86. En la tabla 5 podemos ver los resultados de la comparación entre 2 instrumentos.
Tabla 5. Resultados de los coeficientes de correlación de la regresión de Deming aplicando el método de comparación de 2 instrumentos con el EP Evaluator®.
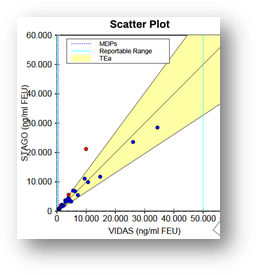
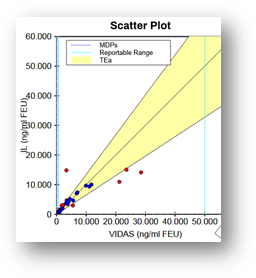
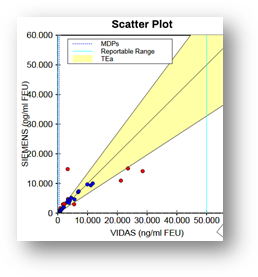
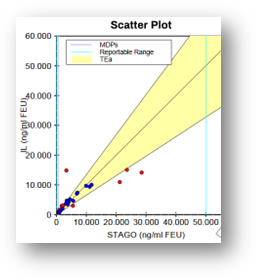
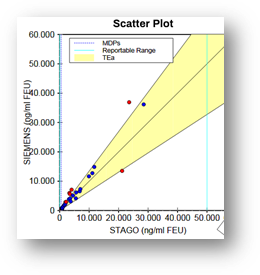
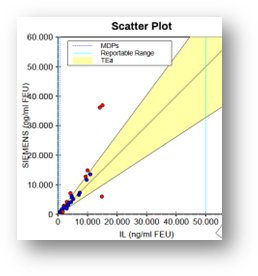
Además en la figura 3 podemos ver los gráficos de la regresión de Deming que surgen de la comparación entre 2 métodos.
Figura 3. Gráfico de comparación entre 2 métodos utilizando EP Evaluator®.
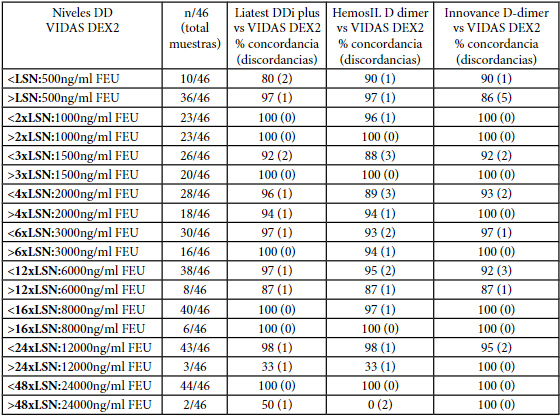
En la tabla 6 se muestran los porcentajes de concordancia entre 2 ensayos y el número de casos de discordancias entre los valores obtenidos por los mismos, en distintos niveles de DD expresados como n veces el LSN.
Tabla 6. Porcentaje de concordancia y número de casos de discordancia de los ensayos por pares en diferentes niveles de DD, tomando como referencia el método VIDAS DEX2.
Discusión
La degradación de la fibrina da como resultado la formación de productos de degradación de diferentes pesos moleculares que incluyen al DD. Los ensayos comerciales reconocen la presencia en las muestras clínicas de múltiples formas de productos de degradación de la fibrina, con diferentes especificidades. Como resultado, la ausencia de un calibrador internacional para DD y la marcada discrepancia en los valores de DD en las mismas muestras medidos por ensayos de diferentes fabricantes se han convertido en los principales problemas de la determinación del DD. Un ensayo que utilice un anticuerpo monoclonal con igual especificidad para todas las formas de productos de degradación de la fibrina, independientemente de sus pesos moleculares, podría ayudar a resolver este problema(22). El análisis de los porcentajes de concordancia entre pares de métodos nos mostró que podemos tener discordancias en todos los niveles de DD. En el punto de corte >500 ng/ml FEU encontramos 5 casos en que el método 2 arrojó un valor por debajo del LSN con respecto al método 1 tomado como referencia. En los niveles >2 x LSN o 1000 ng/ml FEU y >4 x LSN o 2000 ng/ml FEU, no se encontraron discordancias entre los pares de ensayos. En los valores más elevados, por encima de 16 x LSN o 8000 ng/ml FEU, si bien los porcentajes de concordancia fueron muy bajos, hay que tener en cuenta que la cantidad de muestras analizadas en ese rango fue menor. Esta observación está en línea con los reportes de las encuestas de control de calidad externo en los que son notables las discordancias que se observan en los resultados de las muestras que tienen niveles muy elevados de DD procesadas por los diferentes métodos utilizados por los participantes.
Durante la pandemia surgieron numerosas publicaciones en donde se proponen diferentes puntos de corte para utilizar el DD por su valor pronóstico al ingreso a la internación de los pacientes, pero dado que los métodos no son comparables no deberíamos extrapolar los valores absolutos o en función del LSN si utilizamos otro método diferente al de los autores del estudio. Por otra parte en numerosas publicaciones no se especificaba el reactivo y equipamiento utilizado e incluso se han reportado errores en los informes de las unidades en que se expresaron los resultados obtenidos de DD.
Conclusiones
En la serie de muestras de pacientes COVID-19 analizadas, los 4 métodos para la determinación cuantitativa de DD no son comparables, coincidiendo con lo descripto en la bibliografía para otras patologías. Por este motivo no se deberían extrapolar valores de corte absolutos o en función del LSN entre los diferentes métodos.
Agradecimientos. Los autores agradecen a Siemens Healthcare Argentina por proveer un equipo de Innovance D-dimer para la realización de este estudio.
Conflictos de interés. Los autores declaran no poseer conflictos de interés
Bibliografía
1. Linkins LA, Takach Lapner S. Review of D-dimer testing: Good, Bad, and Ugly. Int J Lab Hematol. 2017 May;39 Suppl 1:98-103.
2. Johnson ED, Schell JC, Rodgers GM. The D-dimer assay. Am J Hematol. 2019 Jul;94(7):833-839.
3. Duboscq C, Ceresetto J, Martinuzzo M y col. Uso y limitaciones del dímero D en la exclusión del tromboembolismo venoso. Hematología. 2019; 22(1), 55-65.
4. Privitera V, Rosa C. Dímero-D en COVID-19: utilidad clínica y costo-efectividad. Hematología. 2021;25(Número Extraordinario XXV Congreso Argentino de Hematología):321-333.
5. Dempfle CE. Validation, calibration, and specificity of quantitative D-dimer assays. Semin Vasc Med. 2005 Nov;5(4):315-20.
6. Meijer P, Kluft C. The harmonization of quantitative test results of different D-dimer methods. Semin Vasc Med. 2005 Nov;5(4):321-7.
7. Longstaff C, Adcock D, Olson JD, Jennings I, Kitchen S, Mutch N, Meijer P, Favaloro EJ, Lippi G, Thachil J. Harmonisation of D-dimer - A call for action. Thromb Res. 2016 Jan;137:219-220.
8. CLSI Quantitative D-dimer for the Exclusion of Venous Thromboembolic Disease, approved guidelines 1st Edition, CLSI documents H59 A Wayne PA: Clinical Laboratory Standards Institute 2011.
9. Lippi G, Plebani M. Laboratory abnormalities in patients with COVID-2019 infection. Clin Chem Lab Med. 2020 Jun 25;58(7):1131-1134.
10. Guan WJ, Ni ZY, Hu Y y col; China Medical Treatment Expert Group for Covid-19. Clinical Characteristics of Coronavirus Disease 2019 in China. N Engl J Med. 2020 Apr 30;382(18):1708-1720.
11. Bao J, Li C, Zhang K, Kang H, Chen W, Gu B. Comparative analysis of laboratory indexes of severe and non-severe patients infected with COVID-19. Clin Chim Acta. 2020 Oct;509:180-194.
12. Lippi G, Favaloro EJ. D-dimer is Associated with Severity of Coronavirus Disease 2019: A Pooled Analysis. Thromb Haemost. 2020 May;120(5):876-878.
13. Zhou F, Yu T, Du R y col. Clinical course and risk factors for mortality of adult inpatients with COVID-19 in Wuhan, China: a retrospective cohort study. Lancet. 2020 Mar 28;395(10229):1054-1062. Erratum in: Lancet. 2020 Mar 28;395(10229):1038.
14. Zhang L, Yan X, Fan Q, Liu H, Liu X, Liu Z, Zhang Z. D-dimer levels on admission to predict in-hospital mortality in patients with Covid-19. J Thromb Haemost. 2020 Jun;18(6):1324-1329.
15. Moreno G, Carbonel R, Bodí M, Rodríguez A. Revisión sistemática sobre la utilidad pronóstica del dímero-D, coagulación intravascular diseminada y tratamiento anticoagulante en pacientes graves con COVID-19. Med Intensiva. 2020. https://doi.org/10.1016/j.me-din.2020.06.006.
16. Lodigiani C, Iapichino G, Carenzo L y col; Humanitas COVID-19 Task Force. Venous and arterial thromboembolic complications in COVID-19 patients admitted to an academic hospital in Milan, Italy. Thromb Res. 2020 Jul;191:9-14.
17. Berger JS, Kunichoff D, Adhikari S y col. Prevalence and Outcomes of D-Dimer Elevation in Hospitalized Patients With COVID-19. Arterioscler Thromb Vasc Biol. 2020 Oct;40(10):2539-2547.
18. Thachil J, Tang N, Gando S y col. ISTH interim guidance on recognition and management of coagulopathy in COVID-19. J Thromb Haemost. 2020 May;18(5):1023-1026.
19. Nopp S, Moik F, Jilma B, Pabinger I, Ay C. Risk of venous thromboembolism in patients with COVID-19: A systematic review and meta-analysis. Res Pract Thromb Haemost. 2020 Sep 25;4(7):1178-91.
20. Nauka PC, Baron SW, Assa A y col. Utility of D-dimer in predicting venous thromboembolism in non-mechanically ventilated COVID-19 survivors. Thromb Res. 2021 Mar;199:82-84.
21. Spyropoulos AC, Levy JH, Ageno W y col; Subcommittee on Perioperative, Critical Care Thrombosis, Haemostasis of the Scientific, Standardization Committee of the International Society on Thrombosis and Haemostasis. Scientific and Standardization Committee commu-nication: Clinical guidance on the diagnosis, prevention, and treatment of venous thromboembolism in hospitalized patients with COVID-19. J Thromb Haemost. 2020 Aug;18(8):1859-1865.
22. Kogan AE, Mukharyamova KS, Bereznikova AV, Filatov VL, Koshkina EV, Bloshchitsyna MN, Katrukha AG. Monoclonal antibodies with equal specificity to D-dimer and high-molecular-weight fibrin degradation products. Blood Coagul Fibrinolysis. 2016 Jul;27(5):542-50.