Reacción leucoeritroblástica en pacientes con enfermedad por COVID-19
Leukoerythroblastic reaction in patients with Coronavirus disease
Osycka V, Sepe L, Cicchini S, Domínguez Pose L, López I
Servicio de Hematología, Hospital B.A. Houssay, Vicente López, Buenos Aires, Argentina CP 1638
hematologia.houssay@gmail.com
Palabras claves: RLE,
COVID-19,
citocinas.
Key words: LER,
COVID-19,
cytokines.
Resumen
Desde el brote de coronavirus en 2019 (COVID-19) numerosos estudios se han puesto en marcha para conocer su fisiopatología. Los pacientes críticamente enfermos constituyen un 5% del total y tienen una mortalidad del 1-4% por neumonía y fallo multiorgánico. Estos pacientes desarrollan shock por liberación de citocinas, llamada “tormenta de citoquinas”. El objetivo de la presentación es describir el hallazgo de reacción leucoeritroblástica (RLE) en tres pacientes internados en nuestro hospital, de los cuales sólo uno tuvo enfermedad severa por COVID-19.
Abstract
Since Coronavirus 19 SARS-CoV2 outbreak, numerous studies were turned on to launch its pathophysiology. Critically ill patients, who are 5% of the total, have 1-4% of mortality, due to pneumonia and multiorgan failure. Those patients develop shock related to cytokines release, named ¨cytokine storm¨. Our purpose is to describe the finding of leukoerythroblastic reaction (LER) in three patients admitted to our hospital, while only one had severe COVID disease
Introducción
La infección causada por el CoronaVirus-19 se expresa con cuadro leve de vías aéreas superiores o cuadro grave con neumonía, y, en casos severos, con síndrome respiratorio agudo severo (SARS). Los estudios hematológicos pusieron enfoque en los trastornos trombóticos asociados a la lesión inflamatoria causada por COVID-19. También, en menor medida, ha sido reportada en la literatura la observación en sangre periférica (SP) de reacción leucoeritroblástica (RLE) en 3 publicaciones(1-3). El término RLE se introdujo para describir la presencia de elementos inmaduros de estirpe mieloide y células eritroides nucleadas en SP(4). El mecanismo fisiopatológico preciso de la RLE aún no está descripto en detalle(5). En este artículo presentamos el hallazgo de estos precursores en SP en tres pacientes internados en nuestro hospital, que cursaron infección por COVID-19.
Casos clínicos
A. Paciente masculino de 23 años que consulta al hospital por presentar petequias. En el hemograma presenta Hb 13.1 g/dl, glóbulos blancos (GB) 9.300/mm3 con relación neutrófilos linfocitos (RNL) 9.09, recuento de plaquetas menor a 10.000/mm3, PCR negativa y COVID-19 positivo. Recibe meprednisona 1 mg/kg/día, sin cuadro infeccioso bacteriano u otro cuadro viral asociado
No presenta antecedentes de enfermedades previas. Al 5º día de internación presenta GB 15.100/mm3 con RNL 10.4 y plaquetas 21.000/mm3. Al 9º día GB 35.100/mm3 y presencia de blastos 5% con RNL 24.
Se realizan estudios de citometría de flujo y biopsia de MO, con resultados normales.
Al 12º día de internación se normalizan los GB, como así también la RNL.
El diagnóstico es PTI por COVID-19, Continúa en tratamiento ambulatorio con meprednisona y eltrombopag 50 mg día. Recibe alta con plaquetas 52.000/mm3.
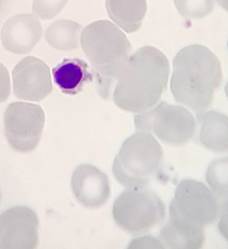
Dos meses después mantiene plaquetas 100.000/mm3 sin volver a repetir presencia de blastos en SP (Figura 1).
B. Paciente masculino de 34 años que se presenta en hospital con fiebre persistente y disnea. Laboratorio Hb 14 g/dl. GB 8500/mm3 y RNL 8.7. Rx de tórax infiltrado bilateral, neumonía y PCR COVID-19 positivo. En internación recibe dexametasona, enoxaparina y soporte de O2.. A los 7 días presenta GB 17.100/mm3 con blastos 2%, al día siguiente GB 22.800/mm3 con blastos 1% y progresa a GB 25.500/mm3 con 2% blastos y 2% de eritroblastos. Alta al día 14 de internación sin sobreinfección bacteriana. Control post alta a los 9 días, GB 6.900/mm3 con RNL 2.78 sin blastos (Figuras 2 y 3).
C. Paciente femenina de 78 años con antecedentes de EPOC (ex tabaquista), COVID-19 positivo, que ingresa por dificultad respiratoria. Rx tórax: infiltrados bilaterales en vidrio esmerilado. Neumonía severa. Se indica dexametasona y HBPM. Al ingreso GB 9.800/mm3 con RNL 1.77.
A las 48 hs pasa a UTI. Al 12º día presenta GB 30.600/mm3 con blastos 8% y 3% de eritroblastos. El nivel de GB se mantiene por 7 días más, con presencia sostenida de blastos en SP. La paciente evoluciona con un neumotórax y a los 35 días de su ingreso fallece por un paro cardiorrespiratorio. Los últimos controles de laboratorio registran GB 9.500/mm3 sin blastos (Figuras 4 y 5).
Figura 1.
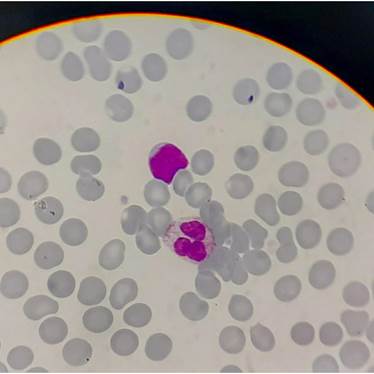
Figura 2.
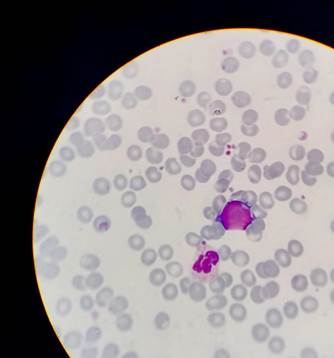
Figura 3.
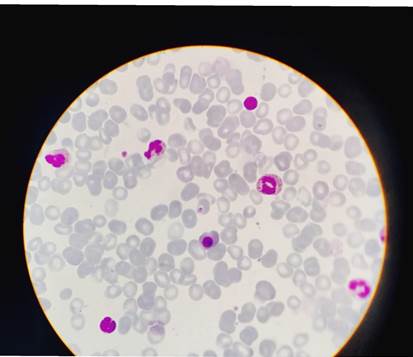
Figura 4.
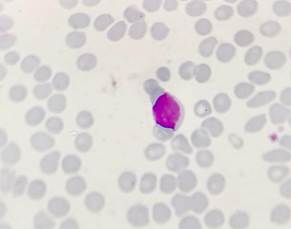
Figura 5.
Discusión
Se desconoce el mecanismo exacto de la RLE. Se presenta en diferentes escenarios, siendo entre los más relevantes la manifestación en pacientes con neoplasias sólidas (40.1%), dada a la producción paraneoplásica de factor estimulante de colonias (G-CSF y GM-CSF) y otras citoquinas como IL-6 o IL-17. Se describe su correlación al pronóstico del tumor(6). El resto de las etiologías donde puede presentarse RLE son neoplasias hematológicas (22.5%), trastornos hemolíticos (7.6%), hemorragias (1.2%) e infecciones severas bacterianas y causas virales descritas que pueden producir RLE (CMV, EBV y parvovirus, H1N1, etc. que, además, generan linfopenia) (9,3%). Dentro del 19.2% restante está la secundaria a fármacos, que es idiosincrática, por ejemplo, los corticoides(7). Fisiopatológicamente se describe la hipoperfusión de áreas de la médula ósea (MO) generada por anemia hemolítica o shock (séptico, anafiláctico, cardiogénico) que interrumpe el microambiente generando la salida desordenada de células precursoras.
Hasta el momento se sabe que la glicoproteína S de la espícula de la superficie viral se une a la enzima ACE2 para ingresar a las células, y que ACE2 se expresa también en los glóbulos rojos y diversos precursores eritroides, así como también en células pulmonares y endoteliales(8). Esta unión recluta monocitos, macrófagos y células dendríticas. Este enlace virus-receptor induce la generación de IL6 y otras citoquinas (TNF alfa, IL1, GCSF, IFN gamma, proteína quimiotáctica de monocitos, proteína inflamatoria de macrófagos), pudiendo generar la salida de precursores a SP.
Conclusión
Presentamos en este reporte tres pacientes con COVID-19, con o sin neumonía severa, que exhiben RLE en SP. Sólo uno presentó cuadro compatible con sepsis y/o falla multiorgánica secundaria a neumonía. Los tres casos recibieron corticoides. La duración de la presencia de blastos en SP no fue superior a una semana en ningún caso. Los corticoides se continuaron como tratamiento específico del COVID-19 y comorbilidades asociadas, lo cual lleva a pensar que la RLE estuvo vinculada a la viremia del COVID-19 más que a otras causas. Las características de los blastos eran francamente aberrantes.
Consideramos de importancia la revisión del frotis en pacientes con COVID-19 y la necesidad de estudiar con prudencia la presencia de estos elementos para diferenciar leucocitosis reactiva con cuadro de RLE vs proliferación clonal leucémica, ya que no se vio como indicador de pronóstico ominoso (como en patologías oncológicas u otras causas).
La RLE es infrecuente en cuadros virales y secundarios a fármacos, lo cual motivó la descripción de casos de pacientes con este nuevo virus.
Agradecimientos
Farm. Laura Pérez, Bioq. Joana Fermoselle, Tec. Carola Trombetta, Tec. Antonella Chittaro
Bibliografía
1. Mitra A, Dwyre DM, Schivo M, Thompson GR 3rd, Cohen SH, Ku N, Graff JP. Leukoerythroblastic reaction in a patient with COVID-19 infection. Am J Hematol. 2020 Aug;95(8):999-1000.
2. Milanesio, M. Reacción leucoeritroblástica asociada a infección por COVID-19. Reporte de caso. Revista de la Facultad de Ciencias Médicas (Córdoba, Argentina) 2021, Marzo.78, 64-67-
3. Jones JR, Ireland R. Morphological changes in a case of SARS-CoV-2 infection. Blood. 2020 Jun 18;135(25):2324.
4. Retief, F. Leukoerythroblastosis in the adult. The Lancet. 1964 March 21;283:639.
5. Byard RW, Bormanis J, Jones TG. Leukoerythroblastosis: a much maligned phenomenon? CMAJ. 1987 Aug 1;137(3):191-2.
6. Hoffman, R. Hematology Basic Principles and Practice. Seventh Edition. Chapter 48.
7. Tabares Calvache E. Systematic review about etiologic association to the leukoerythroblastic reaction. Int J Lab Hematol. 2020;42: 495-500.
8. Shahbaz S. Erythroid precursors and progenitors suppress adaptive immunity and get invaded by SARS-CoV-2. Stem Cell Reports. 2021 May 11; 16 (5): 1165-1181.