Monitoreo de productos de vida media extendida en pacientes con hemofilia B
Monitoring extended half-life products in patients with hemophilia B
Arias M1, Sueldo E1
1Laboratorio de Hematología, Hemostasia y Citometría de Flujo, Hospital César Milstein
La Rioja 951, Ciudad Autónoma de Buenos Aires. C.P. 1221. Argentina
mirtaarias@yahoo.com.ar
Palabras claves: hemofilia B,
productos de vida media extendida,
ensayo coagulométrico en una etapa,
ensayo cromogénico,
factor IX
Keywords: hemophilia B,
extended half-life products,
one-stage clotting assay,
chromogenic assay,
factor IX
Resumen
El monitoreo de laboratorio de la terapia de reemplazo en hemofilia B consiste en la medición de la actividad del factor IX antes y después de la infusión. Se observaron discrepancias en el monitoreo de productos modificados (EHL) cuando son medidas por distintos métodos: coagulométrico en una etapa (OSA) o cromogénico (CSA) y aún dentro del mismo método. Se recomienda que cada centro de hemofilia tenga validado su ensayo para el producto utilizado en la infusión. Se deben utilizar los ensayos calibrados con un calibrador trazable contra un standard de la OMS. En el monitoreo de FIX se deben extremar los cuidados cuando se elige un ensayo debido a la gran variabilidad de resultados encontrada entre los distintos productos EHL.
Abstract
Laboratory monitoring of replacement therapy in hemophilia B consists of measuring factor IX activity before and after infusion. Discrepancies were observed in the monitoring of modified products (EHL) when they are measured by different methods: one-stage assay (OSA) or chromogenic assay (CSA) and still within the same method. It is recommended that each hemophilia center have its assay validated for the product used in the infusion. Assays calibrated with a traceable calibrator against a WHO standard should be used. In the monitoring of FIX, extreme care must be taken when choosing the assay due to the great variability of results found between the different EHL products.
Introducción
La hemofilia B es un defecto de coagulación hereditario ligado al cromosoma X que conduce a deficiencias del factor IX (FIX) en aproximadamente 1 cada 30000 varones nacidos vivos. En la hemofilia B la terapia de reemplazo del factor IX faltante constituye el pilar del tratamiento. El factor se administra a demanda para tratar las hemorragias agudas o de manera profiláctica. En la hemofilia B severa la hemorragia puede ser recurrente, típicamente en forma de hemorragias articulares y/o hematomas del músculo esquelético, dando como resultado una artropatía hemofílica progresiva, que eventualmente conduce a un daño articular irreversible, con discapacidad significativa y disminución de la calidad de vida a menos que se trate con concentrados de FIX. En personas con hemofilia B severa se recomienda como terapia óptima la profilaxis con infusiones endovenosas, de dos veces por semana si es con concentrados de vida media estándar, para mantener los niveles de factor > 1 UI/dl (1%). La llegada de los nuevos productos de vida media prolongada, que incluyen modificaciones en la molécula del factor, buscan disminuir la frecuencia de infusiones y/o lograr niveles valle más altos. Una combinación en la disminución de proteólisis en sangre periférica, eliminación renal y/o hepática y degradación lisosomal, resulta en una prolongación de la vida media del factor. Las estrategias para prolongar la vida media del FIX recombinante incluyen i) unión covalente del factor de coagulación al polietilenglicol (PEG; PEGilación), ii) integrar el factor de coagulación con la porción cristalizable fragmentada (Fc) de la molécula de inmunoglobulina G1 (IgG1), iii) combinar el factor de coagulación con albúmina recombinante.
Monitorear el tratamiento de personas con hemofilia B que reciben productos de vida media prolongada es un desafío para los laboratorios de coagulación, ya que pueden haber diferencias sustanciales entre los resultados obtenidos con el ensayo coagulométrico en una etapa (OSA) y el ensayo de sustrato cromogénico (CSA). La medición del factor tras la administración de ciertos tipos de concentrados puede presentar discordancias entre los diferentes ensayos, las modificaciones moleculares aplicadas para extender la vida media de los factores de coagulación conducen a interacciones nuevas y adicionales con los reactivos y crean nuevos desafíos para los laboratorios, especialmente aquéllos que utilizan ensayos de una etapa para evaluar la eficacia terapéutica. Según las recomendaciones deben utilizarse ensayos que estén calibrados con un calibrador, trazable contra un estándar internacional, y que cada centro de hemofilia tenga validado el ensayo recomendado por el fabricante del producto utilizado en la infusión. En el monitoreo de productos de vida media extendida de FIX se ha reportado que hay una gran variabilidad de resultados entre los distintos productos, por lo que se indican recomendaciones puntuales para la elección del método y/o reactivo a utilizar. Estas discordancias podrían llevar a una heterogeneidad en el seguimiento, asociada con una sobreestimación o subestimación clínicamente significativa de la concentración del factor, lo que podría tener un impacto adverso en el tratamiento de los pacientes y podría dar lugar, por ejemplo, a una búsqueda innecesaria de inhibidores(1).
Características pre-analíticas
La obtención de la muestra debe cumplir con las recomendaciones internacionales para los estudios de hemostasia(2): debe ser extraída en tubos de citrato de sodio 3.2% y con agujas de calibre preferentemente 21G. La aplicación del lazo debe ser no mayor a 1 minuto. Cargar los tubos hasta el enrase para mantener la relación anticoagulante/sangre recomendada (1+9), que deberá ajustarse cuando, por ejemplo, el hematocrito del paciente sea mayor a 55%. Luego realizar una doble centrifugación a 3500 rpm durante 10 min para obtener un plasma pobre en plaquetas (<10000 plq/mm3) y debe procesarse dentro de las 4 horas. En el caso que no se procese en el día puede guardarse la muestra alicuotada preferentemente en congelador -80ºC. Las muestras congeladas se deben descongelar 5 minutos a 37ºC y procesarlas dentro de las 2 horas.
Para realizar estudios de porcentaje de recuperación de factor y de farmacocinética se debe tener acceso a la siguiente información: fecha y hora exacta de la última aplicación del producto, tipo de concentrado de factor que recibió el paciente, y además la dosis total administrada y el peso en Kg. Se realizan dos extracciones, una pre y otra post infusión, ésta última a los 15 minutos según algunos autores, pero puede variar entre 15 minutos a 1 hora. La muestra post se debe recolectar preferentemente de otro sitio de punción, no utilizando la misma vía por la que se infundió el producto.
Características analíticas (Figura 1 y 2)(1)
La medición de la actividad del FIX:C en muestras post infusión con concentrados de vida media prolongada puede realizarse por método coagulométrico en una etapa (OSA), para el cual, dependiendo del concentrado infundido, hay recomendaciones puntuales de la Federación Mundial de la Hemofilia sobre que kits y qué reactivos utilizar. Los reactivos de APTT utilizados pueden variar en la cantidad y composición de fosfolípidos, y en sus activadores, que pueden ser sílica, ácido elágico, caolín o polifenoles. En el caso de que se utilicen equipos semi-automáticos, que se realice de forma manual o que las curvas de calibración no sean estables debe calibrase el ensayo en cada corrida analítica. El dosaje del FIX:C en la muestra debe realizarse en 3 diluciones, ya que esto disminuye el coeficiente de variación del ensayo y permite descartar la presencia de interferencias.
En cuanto al ensayo cromogénico (CSA), éste consta de dos etapas. Los más utilizados son los de marca Rossix e Hyphen.
Primera etapa: alta dilución de la muestra (1/80 o 1/100) mezclado con factor XI humano, factor VIII humano, factor X humano, calcio, fosfolípidos y un inhibidor de la polimerización de la fibrina.
Segunda etapa: factor II humano y factor V bovino (Rossix) o trombina humana (Hyphen, Biophen)
Tanto en el método coagulométrico en una etapa como en el método cromogénico se deben utilizar calibradores trazables contra un estándar internacional.
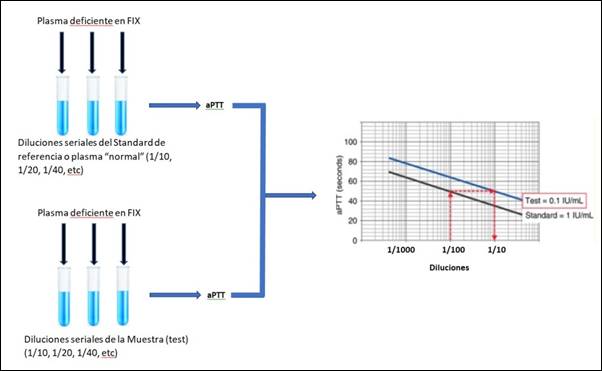
Figura 1. Esquema del ensayo de actividad de factor basado en aPTT. El estándar de referencia se diluye en forma seriada en buffer y se mezcla con volúmenes iguales de plasma deficiente en factor IX (el cual carece del factor IX pero tiene niveles normales de los demás factores, ej. >50%). Se realizan los aPTT para obtener los tiempos para cada dilución del calibrador y se construye una curva de calibración. Los tiempos de coagulación de las muestras se enfrentan con la calibración. Se muestra como ejemplo que si el plasma de referencia contiene 100% de FIX (1 UI/ml), una dilución de 1/100 es equivalente a una concentración de 10% y produce un aPTT de 50 segundos. La muestra que arroja un tiempo de 50 segundos es equivalente a 10% (0.1 UI/ml) del plasma de referencia y, por lo tanto, la muestra contiene 10% de actividad (0.1 UI/ml).

Figura 2. Esquema de ensayo coagulométrico (OSA) en una etapa y cromogénico (CSA)(2)

Calidad analítica
Para monitorear la terapia de reemplazo con eftrenonacog alfa (FIX recombinante fusionado con inmunoglobulina G1 humana [rFIXFc]; Alprolix®), la FMH (Fundación Mundial de Hemofilia) recomienda el uso de un ensayo de FIX cromogénico o un ensayo de FIX de una etapa basado en APTT con reactivos validados, incluyendo algunos reactivos con activador de ácido elágico. Para albutrepenonacog alfa (FIX recombinante fusionado con albúmina humana recombinante [rFIX-FP]; Idelvion®), la FMH recomienda el uso de un ensayo de FIX en una etapa basado en APTT con reactivos validados, incluidos algunos reactivos con sílica como activador. En el caso de nonacog beta pegol (FIX recombinante con un resto de polietilenglicol de 40 kDa [N9-GP]; Refixia® / Rebinyn®), la FMH recomienda el uso de un ensayo de FIX cromogénico o un ensayo de FIX en una etapa basado en APTT con reactivos validados, incluido algún reactivo con activador de ácido elágico o con polifenol(3). En este producto se observó que hay una conversión prematura de N9-GP a FIXa durante la fase de activación. lo que conduce a una sobreestimación de la actividad del FIX en el ensayo de OSA cuando se utiliza silica como activador(4) (Tabla 1).

En cada corrida analítica se deben procesar controles de calidad interno, en al menos dos niveles, y participar de programas de evaluación externa de calidad. Actualmente hay programas de control de calidad externo que tienen encuestas de desempeño para productos de vida media extendida, por ejemplo NEQAS y ECAT Foundation.
Utilidad clínica
El monitoreo de laboratorio es uno de los puntos más importantes en la evaluación y personalización del tratamiento en pacientes con hemofilia. El ingreso de los productos modificados es un desafío para los laboratorios, ya que los productos nuevos no son la misma molécula del factor con la que se calibran habitualmente los ensayos. En las muestras post infusión con productos de vida media prolongada, los métodos utilizados pueden diferir en sus resultados. El ensayo cromogénico de factor IX aún no está disponible en Argentina.
Conclusiones
El advenimiento de los factores de vida media prolongado ofrece varias ventajas para el tratamiento profiláctico de la hemofilia B, la más notable es la reducción de la frecuencia de infusiones en el tratamiento con mejores resultados para los pacientes. Sin embargo, el uso de éstos presenta desafíos en términos de monitoreo debido a la gran diversidad de resultados que presentan los distintos métodos, por lo que existen recomendaciones puntuales para la elección de qué método y/o reactivo utilizar. A su vez, no siempre es posible utilizar el método que el fabricante usó para determinar la potencia del producto. Las guías internacionales han enunciado directrices para reflejar los enfoques diagnósticos correctos para estas terapias(3). Actualmente los laboratorios deben seleccionar un ensayo cromogénico o de una etapa apropiado que haya sido validado para su uso con el tratamiento específico. Por tal razón, si bien se deben utilizar los ensayos calibrados con un calibrador trazable contra un estándar internacional, se recomienda, además, que cada centro de hemofilia tenga validado su ensayo para el producto utilizado en la infusión. Los ensayos cromogénicos presentan varios desafíos asociados con su implementación en la práctica clínica habitual, debido a la falta de disponibilidad del kit y de la metódica en cada región, para cada sistema reactivo-instrumento, además de un aumento del gasto económico, entre otros motivos. Nuevos tratamientos y, por lo tanto, nuevos desafíos nos convocan. En este contexto es fundamental una interacción interdisciplinaria fluida entre el médico tratante y el laboratorio.
Bibliografía
1. Peyvandi F et al. Laboratory testing in hemophilia: Impact of factor and non-factor replacement therapy on coagulation assays. JTH, 2020, 1242-1255.
2. Fundamentos para el manejo práctico en el laboratorio de Hemostasia Grupo CAHT 2da Edición.
3. WFH Guidelines for the Management of Hemophilia, 3rd edition, Chapter 3: Laboratory Diagnosis and Monitoring. Haemophilia, Vol 26, Issue S6, Agosto 2020.
4. Rosen P, Rosen S, Ezban M, Persson E. Overestimation of N-glycoPEGylated factor IX activity in a one-stage factor IX clotting assay owing to silica-mediated premature conversion to activated factor IX. J Thromb Haemost. 2016; 14: 1420-7.