Inhibidores de BTK de segunda generación: zanubrutinib.
Nuevo agente terapéutico para desórdenes linfoproliferativos B
Second generation BTK inhibitors: zanubrutinib.
New therapeutic agent for B- lymphoproliferative disorders.
Cugliari, María Silvana
Instituto de Oncología Ángel Roffo-Universidad de Buenos Aires. Argentina
mscugliari@institutoroffo.uba.ar; silvanacugliari@gmail.com
Palabras clave: zanubrutinib,
BTK,
inhibidores de BTK,
linfoma del manto,
leucemia linfática crónica.
Keywords: zanubrutinib,
BTK,
BTK inhibitors,
mantle cell lymphoma,
chronic lymphocytic leukemia.
Resumen
La tirosina kinasa de Bruton es una tirosina kinasa expresada en todo el linaje hematopoyético, excepto en los progenitores de células T, y cumple un papel esencial en la vía del BCR. La inhibición de la BTK ha probado ser una estrategia efectiva en algunos linfomas y en leucemia linfática crónica. Ibrutinib y acalabrutinib son inhibidores de BTK aprobados en Argentina. Zanubrutinib es un iBTK más específico, lo que explicaría algunas diferencias con los previamente desarrollados. Muchos estudios con zanubrutinib en diferentes síndromes linfoproliferativos B se encuentran en desarrollo o con diferente tiempo de seguimiento y demuestran una inhibición más selectiva por parte de zanubrutinib con ocupación más completa y sostenida de la BTK, lo que resultaría en mayores beneficios en eficacia y seguridad.
Abstract
Bruton's tyrosine kinase is a tyrosine kinase expressed in the entire hematopoietic lineage, except for T cell progenitors, and plays an essential role in the BCR pathway. Inhibition of BTK has proven to be an effective strategy in some lymphomas and chronic lymphocytic leukemia. Ibrutinib and acalabrutinib are BTK inhibitors approved in Argentina. Zanubrutinib is a more specific iBTK, which would explain some differences with those previously developed. Many studies with zanubrutinib in different B-lymphoproliferative syndromes are in development or with different follow-up and it demonstrate a more selective inhibition with more complete and sustained occupation of BTK, which would result in greater benefits in efficacy and safety.
Introducción. Mecanismo de acción
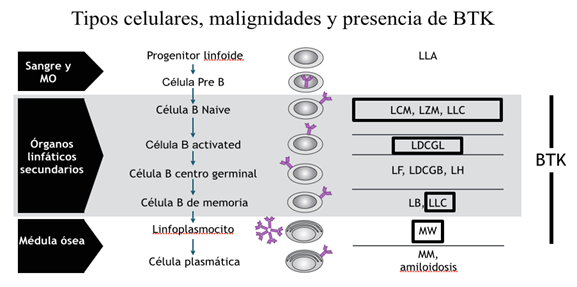
La patogénesis de los síndromes linfoproliferativos y el rol de la vía del receptor de célula B (BCR) en esa patogénesis, se ha ido comprendiendo mejor en los últimos años (Figura 1). La tirosina kinasa de Bruton (BTK) es una tirosina kinasa expresada en todo el linaje hematopoyético, excepto en las células progenitoras T, y cumple un papel esencial en la vía del BCR: la BTK activada, fosforila y activa a la PLCγ2, liberando depósitos de calcio intracelular, lo que deriva en el aumento de factores de transcripción, incluyendo el NFκB. Esto inicia la activación de integrinas, la migración mediada por quemoquinas y la proliferación de células B(1) (Figura 2).
El rol central de la BTK en la supervivencia del linfocito B es evidente en la agammaglobulinemia ligada al X, un síndrome en el que las mutaciones de pérdida de función de la BTK derivan en una casi ausencia de células B y en una inmunodeficiencia humoral profunda(13).
La inhibición de la BTK ha probado ser una estrategia efectiva en algunos linfomas y en leucemia linfática crónica (LLC). Los inhibidores de BTK (iBTK) se clasifican en covalentes o irreversibles (ibrutinib, acalabrutinib, zanubrutinib) y no covalentes o reversibles (vecabrutinib, ARQ-531, fenebrutinib y pirtobrutinib, conocido previamente como LOXO-305), de acuerdo a su forma de unión a la BTK. Los iBTK que han demostrado efectividad clínica y han sido aprobados por la US Food and Drug Administration (FDA) son el ibrutinib, el acalabrutinib y, más recientemente, el zanubrutinib. Ibrutinib es un iBTK primero en su clase, aprobado en Argentina para LLC y otras malignidades de células B(2). En LLC ha demostrado beneficio en sobrevida libre de progresión (SLP) tanto en primera línea (1L) como en pacientes recaídos/refractarios (R/R). Sin embargo, a pesar de su robusta eficacia clínica, muchos pacientes discontinúan ibrutinib debido a toxicidad, incluyendo fibrilación auricular, arritmia ventricular, sangrado mayor, hipertensión y artralgias/mialgias(3). La inhibición de kinasas fuera de blanco o kinasas off-target, que incluye a la familia de kinasas TEC, al receptor de factor de crecimiento epidérmico (EGFR) y a la kinasa de célula T inducible por interleucina-2 (ITK), ha sido implicada como la posible etiología para estos efectos adversos(4).
Los iBTK de segunda generación han sido diseñados con mayor especificidad por la BTK, en un esfuerzo por minimizar los efectos colaterales fuera de diana. Acalabrutinib es un iBTK de segunda generación y se encuentra aprobado en Argentina para el tratamiento de la LLC basado en los datos de los estudios clínicos ELEVATE-TN y ASCEND y para el tratamiento del linfoma de células del manto (LCM) en pacientes recaídos, basado en los resultados del estudio ACE-LY-004(5-8).
Zanubrutinib es un iBTK altamente específico, uniéndose en forma covalente a Cys481 en el bolsillo de ATP de la BTK. Debido a modificaciones estequiométricas que han permitido aumentar la especificidad de zanubrutinib por la BTK (derivando en una menor inhibición de otras kinasas tales como EGFR, HER2, ITK, JAK3, TEC, BMX y BLK) podrían explicarse algunas diferencias entre los iBTK(1). Por ejemplo, ibrutinib (pero no zanubrutinib) provoca el cambio de las GP1bα y GPIX de la superficie plaquetaria por un mecanismo dependiente de ADAM17, reduce la formación del complejo GP1b-IX y la expresión de superficie de la integrina αIIbβ3, y disminuye la formación de trombos bajo flujo arterial(9). Estos efectos podrían explicar las diferencias en el mecanismo de sangrado entre ambas drogas.
Figura 1. Traducido y adaptado de Burger J y Wiestner A. Targeting B cell receptor signalling in cancer: preclinical and clinical advances. Nat Rev Cancer 18, 148–167 (2018).
Zanubrutinib también presenta otras características distintivas. A diferencia de acalabrutinib, la absorción de zanubrutinib no es afectada por la co-administración de agentes reductores del ácido gástrico, como los inhibidores de la bomba de protones(36). Zanubrutinib no prolonga el QTc significativamente(1).Además, a diferencia de ibrutinib, no inhibe la ITK y, por ello, no inhibiría la citotoxicidad celular NK(10). Esto podría llevar a un menor antagonismo con los anticuerpos monoclonales anti CD20 y otorgaría el racional para más estudios de estas combinaciones(1).
Figura 2. Mecanismo de acción de inhibidores de BTK. Adaptado de Marini BL, Samanas L y Perissinotti AJ. Expanding the armamentarium for chronic lymphocytic leukemia: A review of novel agents in the management of chronic lymphocytic leukemia. Journal of Oncology Pharmacy Practice. 2016;23(7),502–517.

Farmacocinética
En el primer estudio fase 1 en humanos con malignidades hematológicas de células B, la administración oral de zanubrutinib provocó una concentración sérica máxima (Cmax) aproximadamente 2 horas luego de la administración, con una vida media de 4 horas para ambas dosificaciones: 160 mg/dos veces al día y 320 mg/día. La ocupación nodal de BTK fue >95% en 89% de los pacientes en la cohorte de 160 mg/2 veces por día comparado con 50% en la cohorte de 320 mg/día. Por lo que ambas dosificaciones fueron exploradas en estudios clínicos subsiguientes(11).
Como otros BTKi, zanubrutinib es primariamente metabolizado por el citocromo CYP3A. Interacciones con inhibidores fuertes del citocromo puede llevar a la necesidad de reducción de dosis o interrupciones del tratamiento con ibrutinib. Sin embargo, el impacto de inhibidores del CYP como itraconazol, voriconazol y ketoconazol en el metabolismo de zanubrutinib es significativamente menor, comparado con ibrutinib(12).
Perfil de seguridad
Los perfiles de seguridad de los iBTK parecen ser variables y los iBTK más selectivos estarían asociados a menor incidencia de algunos eventos adversos, incluyendo los cardiovasculares(14). En los primeros estudios con zanubrutinib, los eventos adversos (EA) más frecuentemente reportados fueron: infección del tracto respiratorio superior (39%), equimosis (36%), tos (27%) y diarrea (27%)(11).
Un metanálisis de 6 estudios clínicos con pacientes con linfomas no Hodgkin B tratados con zanubrutinib reporta los siguientes EA más frecuentes: diarrea (18%), tos (19%), equimosis (19%) y erupción (18%). Los EA grado ≥3 reportados en ≥3% fueron neutropenia (14%), anemia (8%), trombocitopenia (4%), neumonía (9%) e hipertensión arterial (3%). Las tasas de hemorragia mayor son bajas, similares a las de ibrutinib, y la fibrilación auricular fue reportada en un 2%(14). Los resultados futuros con mayor seguimiento de estudios comparativos entre zanubrutinib, acalabrutinib e ibrutinib serán importantes en diferenciar el perfil de seguridad del iBTK y guiar a una adecuada selección terapéutica.
Zanubrutinib en linfoma de células del manto (LCM):
Zanubrutinib fue aprobado por la FDA a fines de 2019 en LCM R/R en base a la tasa de respuesta global (TRG) combinada de 84% en un total de 118 pacientes de dos estudios clínicos multicéntricos: BGB-3111-AU-003 y BGB-3111-206. La duración de respuesta (DdR) fue de 14-18 meses. El 57% de los pacientes desarrolló EA colaterales grado 3-4 incluyendo anemia, neumonía y neutropenia, sólo el 8% discontinuó tratamiento sugiriendo que la monoterapia con zanubrutinib fue muy bien tolerada(15,16,19).
El estudio fase 2 BGB-3111-206 cuenta con resultados de mayor seguimiento presentados recientemente: con mediana de seguimiento de 3 años y una TRG de 83.7% (77.9% alcanzó la remisión completa-RC-). Los EA más frecuentes fueron neutropenia 46%, infección del tracto respiratorio superior 38% y erupción 36%. La tasa de hipertensión arterial grado ≥3 fue de 3.5%, al igual que la de sangrado grado ≥3. El seguimiento a largo plazo muestra que con zanubrutinib se obtiene SLP sostenida y casi la mitad de los pacientes se mantienen libres de progresión. (SLP a 36 meses: 47.6%)(17).
Los pacientes con tumores con mutación de TP53 tienen pronóstico pobre, con medianas de sobrevida global (SG) inferiores a 2 años luego de la primera línea de inmunoquimioterapia intensiva. Nuevas estrategias terapéuticas son necesarias para este grupo. En un estudio fase 2 de Song y col., que enroló pacientes con LCM R/R tratados con zanubrutinib 160 mg, 2 veces al día, esta droga demostró tasas altas de respuesta y DdR prometedora. Por ello, los autores plantean que la inhibición de BTK lograda por zanubrutinib supera parcialmente la resistencia mediada por la mutación de TP53. Se requieren mayores estudios para confirmar esta observación(12).
Otro estudio fase 3 en desarrollo compara zanubrutinib-rituximab con bendamustine-rituximab en pacientes con LCM no tratados previamente y no elegibles para trasplante autólogo. La combinación zanubrutinib-rituximab mejoraría la evolución de este grupo con escasas opciones terapéuticas(18).
Zanubrutinib en leucemia linfática crónica/linfoma linfocítico (LL/LLC)
Tres estudios clínicos han demostrado la eficacia y seguridad de zanubrutinib como monoterapia o en combinación en pacientes con LLC no tratados previamente y R/R, incluidos pacientes con deleción del cromosoma 17p (del17p) y/o mutación de TP53(11,21,22).
Se detallan los estudios con zanubrutinib en esta patología:
a) Fase 1/2: estudio BOVen (zanubrutinib, obinutuzumab y venetoclax en pacientes con LLC no previamente tratados, utilizando la enfermedad residual medible indetectable (en sangre periférica y en médula ósea) como criterio para determinar la discontinuación del tratamiento(23).
b) Fase 2: régimen secuencial, este ensayo evaluará una citorreducción con dos ciclos de bendamustina (sólo para pacientes con carga tumoral alta), seguido de una inducción y mantenimiento con obinutuzumab, zanubrutinib y venetoclax en pacientes con LLC R/R. (CLL2- trial BZAG del Grupo Alemán de Estudio de la LLC)(24).
c) Fase 2: zanubrutinib plus rituximab en LLC no tratados previamente(25).
d) Fase 2: zanubrutinib en LLC intolerante a ibrutinib o acalabrutinib, demostrando que el 75% de los EA que motivaron intolerancia a ibrutinib y acalabrutinib no recurren con zanubrutinib y, si recurren, lo hacen con menor severidad(26).
e) Fase 2: zanubrutinib en LLC R/R (estudio en China): fueron presentados recientemente los resultados de mayor seguimiento (34 meses) demostrando respuestas profundas y sostenidas, incluso en los subgrupos de alto riesgo. (TRG 87,9% con 67% RP). Se reportaron 51% de EA serios y 83% de EA grado ≥3 aunque sin nuevas señales de seguridad en este análisis(27).
f) Fase 3: el estudio internacional SEQUOIA, abierto, randomizado y multicéntrico, incluye 3 cohortes: zanubrutinib vs bendamustine-rituximab (cohorte 1, no incluye pacientes con del17p), zanubrutinib hasta toxicidad inaceptable o progresión (cohorte 2, no randomizada, para pacientes con del17p) y zanubrutinib-venetoclax (cohorte 3, para pacientes con del17p o mutación de TP53 que recibirán venetoclax hasta toxicidad inaceptable, progresión de enfermedad o por un máximo de 24 ciclos y zanubrutinib por un mínimo of 27 ciclos o hasta toxicidad inaceptable o progresión de enfermedad). El objetivo primario es SLP por comité independiente y los secundarios: TRG, SG, DdR y EA. Aún no se han publicado resultados de la cohorte 1. Sin embargo, la compañía tecnológica BeiGene, mediante un informe de prensa, ha anunciado el logro de su objetivo primario, con superioridad estadísticamente significativa de zanubrutinib sobre bendamustina-rituximab a una mediana de seguimiento de 25,8 meses con un perfil de toxicidad aceptable(28). Tampoco se han publicado aún los resultados preliminares de la cohorte 3(31). La cohorte 2 incluyó 109 pacientes con test centralmente confirmado para del(17p). Zanubrutinib resultó efectivo y bien tolerado. La mediana de SLP y SG no fue alcanzada en el análisis a 18,2 meses. La TRG fue de 94% y SLP estimada a 18 meses fue de 88%. Hubo 9 eventos de progresión con 4 pacientes con transformación a Richter confirmada histológicamente. Los EA más comunes fueron: equimosis (20,2%), infección del tracto respiratorio superior (19.3%), neutropenia (17.4%) y diarrea (16.5%). Tres pacientes desarrollaron fibrilación auricular y 5.5% de los pacientes tuvieron sangrado grado 3 o mayor(29,30).
g) Fase 3: estudio ALPINE. Este estudio multicéntrico randomizó 415 pacientes con LLC R/R a recibir zanubrutinib continuo vs ibrutinib continuo. La TRG, objetivo primario, demostró ser significativamente mayor con zanubrutinib (78% vs 62%, P=0.0006) y aun mayor en pacientes con del11q (83% vs 69%) y del17p (83% vs 53%). La SLP a 12 meses fue de 94.9% para zanubrutinib vs 84.0% para ibrutinib y la SG 97% vs 92%. La tasa de fibrilación auricular/aleteo fue significativamente más baja con zanubrutinib (2.5% vs 10.1%, P=0.0014) y la de sangrado mayor 2.9% vs 3.9%. La tasa de discontinuación debida a EA fue inferior para zanubrutinib. La tasa de neutropenia fue más alta con zanubrutinib (28.4% vs 21.7%), aunque las infecciones grado ≥3 fueron más bajas (12.7% vs 17.9%). Estos datos confirman una inhibición más selectiva por parte de zanubrutinib con ocupación de la BTK más completa y sostenida, resultando en mayores beneficios en eficacia y seguridad(32).
Zanubrutinib en macroglobulinemia de Waldenström (MW)
El estudio ASPEN comparó la eficacia y seguridad de ibrutinib con zanubrutinib en 201 pacientes con MW. Pacientes con MYD88L265P fueron randomizados 1:1 a tratamiento con ibrutinib o zanubrutinib. El objetivo primario era RC o muy buena remisión parcial (MBRP) evaluadas por un comité independiente. Ningún paciente alcanzó la RC. Veintinueve pacientes con zanubrutinib (28%) y 19 con ibrutinib (19%) alcanzaron una MBRP, una diferencia no estadísticamente significativa (P 5.09). Las TRM fueron 77% y 78%, respectivamente. La mediana de SLP no fue alcanzada, con 84% y 85% de los pacientes con ibrutinib y zanubrutinib libres de progresión a 18 meses. Fibrilación auricular, diarrea, edema periférico, sangrado y neumonía, al igual que los EA que provocaron la discontinuación, fueron menos frecuentes entre los pacientes que recibieron zanubrutinib. Estos resultados demuestran que zanubrutinib e ibrutinib son altamente efectivos en el tratamiento de la WM, pero zanubrutinib se asoció a una tendencia a mejor respuesta y menor toxicidad, particularmente cardiovascular(33).
También se presentó recientemente, una comparación indirecta con IQT donde zanubrutinib demostró SLP más prolongada que dexametasona-rituximab-ciclofosfamida, SLP y SG más prolongadas que bendamustina-rituximab y menor incidencia de neutropenia en pacientes con MW(34).
Zanubrutinib en otros linfomas no Hodgkin
Zanubrutinib se encuentra en estudio también en otros síndromes linfoproliferativos B:
• con lenalidomida+R-CHOP en linfoma difuso de células grandes B.
• con zandelisib en linfoproliferativos B R/R(19).
• con tislelizumab (anticuerpo monoclonal anti-PD-1) -NCT02795182-.
• fase 2 en linfoma de la zona marginal R/R (estudio Magnolia): se reportaron altas tasas de respuesta y control sostenido de la enfermedad (mediana de seguimiento 15,5 meses)(20).
Consideraciones regulatorias
A la fecha de este artículo, zanubrutinib no se encuentra aprobado en Argentina. Está aprobado por la FDA para el tratamiento del LCM y recomendado por las guías del National Comprehensive Cancer Network (NCCN) en diciembre de 2020 para pacientes con LLC en 1L (con del17p y/o mutación de TP53 que presentan contraindicación para otro iBTK) y en LLC R/R (para pacientes que presenten intolerancia o contraindicación a otro iBTK)(35).
Conclusiones
El desarrollo de los iBTK ibrutinib y acalabrutinib ha representado un cambio en el paradigma del tratamiento de algunos desórdenes linfoproliferativos B. Resultados prometedores y perfil de seguridad aceptable con zanubrutinib en LLC, LCM, MW y otros, están llevando a su consideración en el algoritmo terapéutico de dichas entidades, pero la falta de seguimiento prolongado no permite aun establecer con certeza la cinética o duración de la respuesta obtenida o su toxicidad a largo plazo. La inhibición más selectiva de la BTK, resultaría beneficiosa en términos de eficacia y seguridad pero se requiere mayor seguimiento de los estudios con zanubrutinib para saber si constituye o no el mejor iBTK para el manejo de síndromes linfoproliferativos B.
Conflictos de interés: la Dra. María Silvana Cugliari declara haber recibido honorarios de los Laboratorios Abbvie, Astra Zeneca, Genzyme, Janssen, Roche y Sandoz en concepto de conferencias, asesorías y actividades educativas.
Bibliografia
1- Rhodes J y Mato A. Drug Design, Development and Therapy. 2021:15 919-926
2- Administración Nacional de Medicamentos, Alimentos y Tecnología Médica (ANMAT) Disposición No 9440 (11/11/2015) y No 12655 (13/12/2017).
3- Mato AR, Nabhan C, Thompson MC y col. Toxicities and outcomes of 616 ibrutinib-treated patients in the US: a real-world analysis. Haematologica. 2018;103(5):874-879.
4- Stephens DM, Byrd JC. How I manage ibrutinib intolerance and complications in patients with CLL. Blood. 2019;133(12):1298-1307.
5- Sharman JP, Egyed M, Jurczak W y col. Acalabrutinib with or without obinutuzumab versus chlorambucil and obinutuzumab for treatment-naive CLL (ELEVATE TN): a randomized, controlled, phase 3 trial. Lancet. 2020 Apr 18;395(10232):1278-1291.
6- Ghia P, Pluta A, Wach M y col. ASCEND: Phase III, Randomized Trial of Acalabrutinib Versus Idelalisib Plus Rituximab or Bendamustine Plus Rituximab in R/R CLL. J Clin Oncol. 2020; 38:25, 2849-2861.
7- Wang M, Rule S, Zinzani PL et al. Acalabrutinib in R/R mantle cell lymphoma (ACE-LY-004): a single-arm, multicentre, phase 2 trial. Lancet. 2018;391(10121):659-667.
8- ANMAT Disposición No 3549 (22/05/2020) y 5732 (17/07/2019).
9- Dobie G, Kurini F, Omar M y col. Ibrutinib, but not zanubrutinib, induces platelet receptor shedding of GPIb-IX-V complex and integrin αIIbβ3 in mice and humans. Blood Adv. 2019; 3 (24): 4298-4311.
10- Flinsenberg TWH, Tromedjo CC, Hu N y col. Differential effects of BTK inhibitors ibrutinib and zanubrutinib on NK-cell effector function in patients with mantle cell lymphoma. Haematologica. 2020;105(2):e76-e79.
11- Tam CS, Trotman J, Opat S y col. Phase 1 study of the selective BTK inhibitor zanubrutinib in B-cell malignancies and safety and efficacy evaluation in CLL. Blood. 2019;134(11):851-859.
12- Song Y, Zhou K, Zou D y col. Treatment of Patients with R/R Mantle-Cell Lymphoma with Zanubrutinib, a Selective Inhibitor of Bruton's Tyrosine Kinase. Clin Cancer Res. 2020;26:4216-24.
13- Sawalha Y, Bond D, Alinari L. Evaluating the Therapeutic Potential of Zanubrutinib in the Treatment of R/R Mantle Cell Lymphoma: Evidence to Date. OncoTargets Ther. 2020; 13: 6573-6581.
14- Tam CS, Opat S, Zhu J y col. PS1159 pooled analysis of safety data from monotherapy studies of the BTK inhibitor, zanubrutinib (BGB-3111), in B-cell malignancies. HemaSphere. 2019;3(S1):526.
15- Weaver AN and Jimeno A. Zanubrutinib: a new BTK inhibitor for treatment of R/R mantle cell lymphoma. Drugs Today. 2020, 56(8): 531.
16- Tam C, Opat S, Simpson D y col. Zanubrutinib for the treatment of R/R mantle cell lymphoma. Blood Adv. 2021; 5 (12): 2577-2585.
17- Song Y y col. (EP789) Zanubrutinib in patients with R/R MCL: long term efficacy and safety results from a phase 2 study. 2021 European Hematology Association (EHA2021) Congress in June 2021. Available at EHA Open Access Library.
18- Dreyling M, Tam C, Wang M y col. A Phase III study of zanubrutinib plus rituximab versus bendamustine plus rituximab in transplant-ineligible, untreated mantle cell lymphoma. FutureOncol. (2021)17(3),255-262.
19- Soumerai J y col. (S214) tolerability and efficacy of the combination of PI3KΔ inhibitor zandelisib (ME-401) and BTK inhibitor zanubrutinib in patients with R/R B-cell malignancies: initial results. 2021 European Hematology Association (EHA2021) Congress in June 2021. Available at EHA Open Access Library.
20- Opat S y col (EP783) PHASE 2 Study of zanubrutinib in patients with r/r marginal zone lymphoma (MAGNOLIA study). 2021 European Hematology Association (EHA 2021) Congress in June 2021. Available at EHA Open Access Library.
21- Xu W, Yang S, Zhou K y col. Treatment of R/R SLL/CLL with the BTK inhibitor zanubrutinib: phase 2, single-arm, multicenter study. J Hematol Oncol. 2020;13(1):48.
22- Tam CS, Robak T, Ghia P et al. Efficacy and safety of zanubrutinib in patients with treatment-naive CLL or SLL with del(17p): initial results from arm C of the Sequoia (BGB-3111-304) trial.
23- https://clinicaltrials.gov/ct2/show/NCT03824483
24- https://clinicaltrials.gov/ct2/show/NCT04515238
25- https://clinicaltrials.gov/ct2/show/NCT04458610
26- Shadman M y col. (EP642) Preliminary results of the phase 2 study of zanubrutinib in patients with previously treated b-cell malignancies intolerant to ibrutinib and/or acalabrutinib. 2021 European Hematology Association (EHA 2021) Congress in June 2021. Available at EHA Open Access Library.
27- Xu W y col. (EP639) Zanubrutinib monotherapy in patients with R/R CLL: 34-month follow-up results. 2021 European Hematology Association (EHA2021) Congress in June 2021. Available at EHA Open Access Library.
29- Tam CS, Robak T, Ghia P y col. Zanubrutinib monotherapy for patients with treatment naïve CLL and 17p deletion. Haematologica. 2020 Oct13; Online ahead of print.
30- Brown JR, Robak T, Ghia P y col. Efficacy and safety of zanubrutinib in patients with Treatment-Naïve CLL/SLL with del (17p): follow-up results from arm C of the SEQUOIA (BGB-3111- 304) trial. Blood. 2020;136(Supplement 1):11-12.
31- Tam CS, Flinn IW, Tedeschi A y col. Zanubrutinib in combination with venetoclax for patients with treatment-naïve CLL/SLL and del(17p): arm D of the SEQUOIA (BGB-3111-304) trial. Blood. 2020;136(Supplement 1):24-25.
32- Hillmen P, Eichhorst B, Brown J y col. (LB1900) First interim analysis of ALPINE study: results of a phase 3 randomized study of zanubrutinib vs ibrutinib in patients with R/R CLL/SLL. 2021 European Hematology Association (EHA2021) Congress in June 2021. Available at EHA Open Access Library.
33- Tam C, Opat S, D´Sa S y col. A randomized phase 3 trial of zanubrutinib vs ibrutinib in symptomatic Waldenström Macroglobulinemia: the ASPEN study. Blood. 2020; 136 (18): 2038-2050.
34- Castillo, J. y col. (EP805) Efficacy and safety of zanubrutinib versus rituximab-based chemoimmunotherapy in Waldenström macroglobulinemia: matching-adjusted indirect comparisons. 2021 European Hematology Association (EHA2021) Congress in June 2021. Available at EHA Open Access Library.
35- NCCN CLL/SLL. Version 2.2021. https://www.nccn.org/professionals/physician_gls/pdf/cll.pdf. Published Dec 3, 2020. Accessed Jan 8, 2021.
36- Stephens D. Second-Generation BTK Inhibitors: Simply the Best Treatments for CLL?. Publicado en ascopubs.org/journal/jco on July 26, 2021.